Гистидин (обозначение His или H ) [2] — незаменимая аминокислота , которая используется в биосинтезе белков . Он содержит α-аминогруппу (которая в биологических условиях находится в протонированной форме –NH 3 + ), группу карбоновой кислоты (которая в биологических условиях находится в депротонированной форме –COO – ) и имидазольную боковую цепь (которая частично протонирован), классифицируя его как положительно заряженную аминокислоту при физиологическом pH . Первоначально считалось, что он необходим только для младенцев, но теперь, как показали долгосрочные исследования, он необходим и для взрослых. [3] Он кодируется кодонами CAU и CAC .
Гистидин был впервые выделен Альбрехтом Косселем и Свеном Густавом Хедином в 1896 году. [ 4 ] Он также является предшественником гистамина , жизненно важного воспалительного агента в иммунных реакциях. Ацильный радикал – гистидил .
Сопряженная кислота (протонированная форма) боковой цепи имидазола в гистидине имеет p K a примерно 6,0. Таким образом, при pH ниже 6 имидазольное кольцо в основном протонировано (как описано уравнением Хендерсона-Хассельбаха ). Образующееся имидазолиевое кольцо несет две связи NH и имеет положительный заряд. Положительный заряд одинаково распределен между обоими атомами азота и может быть представлен двумя одинаково важными резонансными структурами . Иногда для этой протонированной формы вместо обычного His используется символ Hip . [5] [6] [7] При pH выше 6 один из двух протонов теряется. Оставшийся протон имидазольного кольца может располагаться на любом азоте, образуя так называемые таутомеры N1-H или N3-H . Таутомер N3-H показан на рисунке выше. В таутомере N1-H NH находится ближе к основной цепи. Эти нейтральные таутомеры, также называемые Nδ и Nε, иногда обозначаются символами Hid и Hie соответственно. [5] [6] [7] Имидазольное/имидазолиевое кольцо гистидина является ароматическим при всех значениях pH. [8] При определенных условиях все три ионообразующие группы гистидина могут быть заряжены, образуя катион гистидиния. [9]
Кислотно-основные свойства боковой цепи имидазола имеют отношение к каталитическому механизму многих ферментов . [10] В каталитических триадах основной азот гистидина отрывает протон от серина , треонина или цистеина , чтобы активировать его как нуклеофила . В гистидиновом челноке протонов гистидин используется для быстрого переноса протонов. Он может сделать это, отделив протон от его основного азота, чтобы образовать положительно заряженный промежуточный продукт, а затем использовать другую молекулу, буфер, для извлечения протона из его кислого азота. В карбоангидразах гистидиновый протонный челнок используется для быстрого переноса протонов от молекулы воды, связанной с цинком , для быстрой регенерации активной формы фермента. В спиралях E и F гемоглобина гистидин влияет на связывание дикислорода, а также монооксида углерода . Это взаимодействие увеличивает сродство Fe(II) к O2, но дестабилизирует связывание CO, который связывается с гемоглобином лишь в 200 раз сильнее по сравнению с 20 000 раз сильнее со свободным геем .
Методом 15 N ЯМР-спектроскопии охарактеризованы таутомерия и кислотно-основные свойства боковой цепи имидазола . Два химических сдвига 15 N аналогичны (около 200 частей на миллион по отношению к азотной кислоте по сигма-шкале, где увеличение экранирования соответствует увеличению химического сдвига ). Спектральные измерения ЯМР показывают, что химический сдвиг N1-H падает незначительно, тогда как химический сдвиг N3-H падает значительно (около 190 против 145 м.д.). Это изменение указывает на то, что таутомер N1-H является предпочтительным, возможно, из-за водородных связей с соседним аммонием . Экранирование в N3 существенно снижается из-за парамагнитного эффекта второго порядка, который включает в себя разрешенное по симметрии взаимодействие между неподеленной парой азота и возбужденными π*-состояниями ароматического кольца . При pH > 9 химические сдвиги N1 и N3 составляют примерно 185 и 170 м.д. [11]


Гистидин образует комплексы со многими ионами металлов. Боковая цепь имидазола остатка гистидина обычно служит лигандом в металлопротеинах . Одним из примеров является аксиальное основание, прикрепленное к Fe в миоглобине и гемоглобине. Полигистидиновые метки (из шести или более последовательных остатков H) используются для очистки белков путем связывания с колонками с никелем или кобальтом с микромолярным сродством. [12] Было показано , что природные полигистидиновые пептиды, обнаруженные в яде гадюки Atheris sqamigera , связывают Zn(2+), Ni(2+) и Cu(2+) и влияют на функцию металлопротеаз яда. [13]
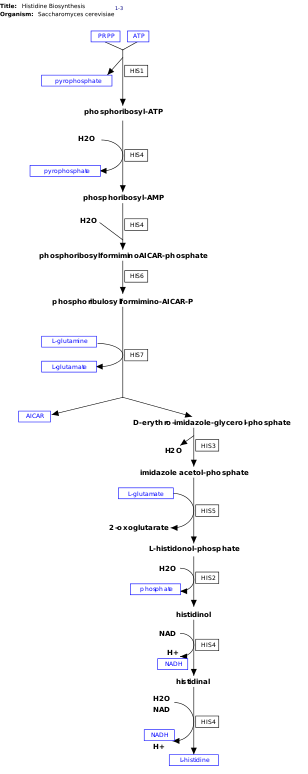
L -Гистидин — незаменимая аминокислота, которая не синтезируется de novo в организме человека. [14] Люди и другие животные должны потреблять гистидин или гистидинсодержащие белки. Биосинтез гистидина широко изучен у прокариот, таких как E. coli . Синтез гистидина в E. coli включает восемь генных продуктов (His1, 2, 3, 4, 5, 6, 7 и 8) и происходит в десять стадий. Это возможно, поскольку продукт одного гена способен катализировать более чем одну реакцию. Например, как показано на пути, His4 катализирует 4 различных этапа пути. [15]
Гистидин синтезируется из фосфорибозилпирофосфата (PRPP), который образуется из рибозо-5-фосфата под действием рибозо-фосфатдифосфокиназы по пентозофосфатному пути . Первой реакцией биосинтеза гистидина является конденсация PRPP и аденозинтрифосфата (АТФ) под действием фермента АТФ-фосфорибозилтрансферазы . АТФ-фосфорибозилтрансфераза обозначена на изображении His1. [15] Продукт гена His4 затем гидролизует продукт конденсации фосфорибозил-АТФ с образованием фосфорибозил-АМФ (PRAMP), что является необратимым этапом. Затем His4 катализирует образование фосфорибозилформиминоAICAR-фосфата, который затем преобразуется в фосфорибулозилформимино-AICAR-P с помощью продукта гена His6. [16] His7 расщепляет фосфорибулозилформимино-AICAR-P с образованием d -эритроимидазол-глицерин-фосфата. После этого His3 образует имидазолацетолфосфат, высвобождая воду. Затем His5 образует l -гистидинол-фосфат, который затем гидролизуется His2 с образованием гистидинола. His4 катализирует окисление l -гистидинола с образованием l -гистидиналя, аминоальдегида. На последнем этапе l -гистидиналь преобразуется в l -гистидин. [16] [17]
Путь биосинтеза гистидина изучен у гриба Neurospora crassa и обнаружен ген ( His-3 ), кодирующий мультиферментный комплекс , сходный с геном His4 бактерии E. coli . [18] Генетическое исследование мутантов гистидина N. crassa показало, что отдельные активности мультиферментного комплекса происходят в дискретных, смежных участках генетической карты His-3 , что позволяет предположить, что различные активности мультиферментного комплекса кодируются отдельно друг от друга. . [18] Однако были также обнаружены мутанты, у которых отсутствовали все три активности одновременно, что позволяет предположить, что некоторые мутации вызывают потерю функции комплекса в целом.
Так же, как животные и микроорганизмы, растениям для роста и развития необходим гистидин. [10] Микроорганизмы и растения схожи в том, что они могут синтезировать гистидин. [19] Оба синтезируют гистидин из биохимического промежуточного продукта фосфорибозилпирофосфата. В целом биосинтез гистидина у растений и микроорганизмов очень похож. [20]
Для своего существования этому пути требуется энергия, поэтому присутствие АТФ активирует первый фермент пути, АТФ-фосфорибозилтрансферазу (показана как His1 на изображении справа). АТФ-фосфорибозилтрансфераза — это фермент, определяющий скорость, который регулируется посредством ингибирования по обратной связи, что означает, что он ингибируется в присутствии продукта — гистидина. [21]
Гистидин — одна из аминокислот, которая может превращаться в промежуточные соединения цикла трикарбоновых кислот (ТСА) (также известного как цикл лимонной кислоты). [22] Гистидин, наряду с другими аминокислотами, такими как пролин и аргинин, принимает участие в дезаминировании — процессе, при котором удаляется его аминогруппа. У прокариот гистидин сначала превращается в уроканат под действием гистидазы. Затем уроканаза превращает уроканат в 4-имидазолона-5-пропионат. Имидазолонпропионаза катализирует реакцию образования формиминоглутамата (FIGLU) из 4-имидазолона-5-пропионата. [23] Форминогруппа переносится на тетрагидрофолат , а оставшиеся пять атомов углерода образуют глутамат. [22] В целом эти реакции приводят к образованию глутамата и аммиака. [24] Затем глутамат может быть дезаминирован глутаматдегидрогеназой или трансаминирован с образованием α-кетоглутарата. [22]

Совет по продовольствию и питанию (FNB) Института медицины США установил рекомендуемые диетические нормы (RDA) для незаменимых аминокислот в 2002 году. Гистидин для взрослых 19 лет и старше составляет 14 мг/кг массы тела в день. [29] Дополнительный гистидин исследуется на предмет использования при различных состояниях, включая неврологические расстройства, атопический дерматит, метаболический синдром, диабет, уремическую анемию, язвы, воспалительные заболевания кишечника, злокачественные новообразования и нарушение мышечной деятельности во время напряженных физических упражнений. [30]