Глиоксаль — органическое соединение с химической формулой OCHCHO. Это наименьший диальдегид (соединение с двумя альдегидными группами). Это кристаллическое твердое вещество, белое при низких температурах и желтое вблизи точки плавления (15 °C). Жидкость желтая, а пар зеленый. [2]
Чистый глиоксаль встречается нечасто, поскольку глиоксаль обычно обрабатывается как 40% водный раствор (плотность около 1,24 г/мл). Он образует ряд гидратов , включая олигомеры . Для многих целей эти гидратированные олигомеры ведут себя эквивалентно глиоксалю. Глиоксаль производится в промышленности как прекурсор многих продуктов. [3]
Глиоксаль был впервые получен и назван немецко-британским химиком Генрихом Дебусом (1824–1915) путем реакции этанола с азотной кислотой . [4] [5]
Коммерческий глиоксаль получают либо газофазным окислением этиленгликоля в присутствии серебряного или медного катализатора ( процесс Лапорта), либо жидкофазным окислением ацетальдегида азотной кислотой . [ 3]
Первый коммерческий источник глиоксаля был в Ламотте , Франция, запущен в 1960 году. Крупнейшим коммерческим источником является BASF в Людвигсхафене , Германия , с объемом около 60 000 тонн в год. Другие производственные площадки существуют также в США и Китае. Коммерческий глиоксаль в больших объемах производится и сообщается как 40% раствор в воде по весу [3] (приблизительное молярное соотношение глиоксаля к воде 1:5).
Глиоксаль может быть синтезирован в лаборатории путем окисления ацетальдегида селенистой кислотой [ 6] или путем озонолиза бензола . [7]
Безводный глиоксаль получают путем нагревания твердого гидрата(ов) глиоксаля с пентоксидом фосфора и конденсации паров в холодной ловушке . [8]
Экспериментально определенная константа закона Генри для глиоксаля равна:

Конечные продукты гликирования (AGE) — это белки или липиды, которые подвергаются гликированию в результате диеты с высоким содержанием сахара. [10] Они являются биомаркером, связанным со старением и развитием или ухудшением многих дегенеративных заболеваний , таких как диабет , атеросклероз , хроническая болезнь почек и болезнь Альцгеймера . [11]
Гуаниновые основания в ДНК могут подвергаться неферментативному гликированию глиоксалем с образованием аддуктов глиоксаля-гуанина. [12] Эти аддукты затем могут образовывать сшивки ДНК . Гликация ДНК также может приводить к мутации , разрывам ДНК и цитотоксичности . [13] У людей глиоксаль-гликированные нуклеотиды могут быть восстановлены белком DJ-1, также известным как Park7. [13]
В мелованной бумаге и текстильных отделках в качестве сшивающего агента для рецептур на основе крахмала используется большое количество глиоксаля . Он конденсируется с мочевиной, образуя 4,5-дигидрокси-2-имидазолидинон, который далее реагирует с формальдегидом, образуя бис(гидроксиметил)производное диметилолэтиленмочевину , которая используется для химической обработки одежды, устойчивой к складкам, т. е. для постоянного прессования. [3]
Глиоксаль используется в качестве солюбилизатора и сшивающего агента в химии полимеров .
Глиоксаль является ценным строительным блоком в органическом синтезе , особенно в синтезе гетероциклов, таких как имидазолы . [14] Удобной формой реагента для использования в лаборатории является его бис(полуацеталь) с этиленгликолем , 1,4-диоксан-2,3-диол. Это соединение коммерчески доступно.
Растворы глиоксаля также можно использовать в качестве фиксатора для гистологии , то есть метода консервации клеток для их исследования под микроскопом.
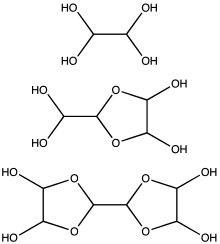
Глиоксаль обычно поставляется в виде 40% водного раствора. [3] Как и другие малые альдегиды , глиоксаль образует гидраты. Кроме того, гидраты конденсируются, образуя ряд олигомеров, некоторые из которых остаются с неопределенной структурой. Для большинства применений точная природа видов в растворе не имеет значения. По крайней мере, один гидрат глиоксаля продается в коммерческих целях, дигидрат тримера глиоксаля: [(CHO) 2 ] 3 ( H2O ) 2 (CAS 4405-13-4). Доступны и другие эквиваленты глиоксаля, такие как полуацеталь этиленгликоля 1,4-диоксан- транс -2,3-диол ( CAS 4845-50-5, т.пл. 91–95 °C).
Подсчитано, что при концентрациях менее 1 М глиоксаль существует преимущественно в виде мономера или его гидратов, т. е. OCHCHO, OCHCH(OH) 2 или (HO) 2 CHCH(OH) 2 . При концентрациях выше 1 М преобладают димеры. Эти димеры, вероятно, являются диоксоланами с формулой [(HO)CH] 2 O 2 CHCHO. Димеры и тримеры выпадают в осадок в виде твердых веществ из холодных растворов. [15]
Глиоксаль был обнаружен как следовый газ в атмосфере, например, как продукт окисления углеводородов. [16] Сообщалось о концентрациях в тропосфере от 0 до 200 ppt по объему, в загрязненных регионах до 1 ppb по объему. [17]
LD 50 (перорально , крысы) составляет 3300 мг/кг, [3] тогда как LD 50 поваренной соли составляет 3000 мг/кг. [18]
Man erhitzt nun das Glyoxal-Phosphorpentoxyd-Gemisch mit freier Flamme und beobachtet лысый, dass sich unter Schwarzfärbung des Kolbeninhalte ein flüchtiges grünes Gas bildet, welches sich in der gekühlten Vorlage zu schönen Krystallen von gelber kondens инертный. [Нагревают смесь (сырого) глиоксаля и P4O10
на
открытом
огне
и вскоре наблюдают, как почернело содержимое, подвижный зеленый газ, который конденсируется в охлажденной колбе в виде красивых желтых кристаллов.]