
В науке о поверхности двойной слой ( DL , также называемый двойным электрическим слоем , EDL ) — это структура, которая появляется на поверхности объекта, когда он подвергается воздействию жидкости . Объект может быть твердой частицей, газовым пузырем , каплей жидкости или пористым телом . DL относится к двум параллельным слоям заряда , окружающим объект. Первый слой, поверхностный заряд (положительный или отрицательный), состоит из ионов , которые адсорбируются на объекте в результате химических взаимодействий . Второй слой состоит из ионов, притягивающихся к поверхностному заряду силой Кулона , электрически экранирующих первый слой. Этот второй слой слабо связан с объектом. Он состоит из свободных ионов, которые движутся в жидкости под действием электрического притяжения и теплового движения , а не прочно закреплены. Поэтому его называют «диффузным слоем».
Межфазные DL наиболее очевидны в системах с большим отношением площади поверхности к объему , таких как коллоидные или пористые тела с частицами или порами (соответственно) в масштабе от микрометров до нанометров . Однако ДЛ важны для других явлений, таких как электрохимическое поведение электродов .
DL играют фундаментальную роль во многих повседневных веществах. Например, гомогенизированное молоко существует только потому, что капли жира покрыты слоем DL, который предотвращает их свертывание в масло . ДЛ существуют практически во всех гетерогенных жидкостных системах, таких как кровь, краска, чернила, керамический и цементный растворы .
ДЛ тесно связана с электрокинетическими явлениями и электроакустическими явлениями .

Когда электронный проводник контактирует с твердым или жидким ионным проводником (электролитом), появляется общая граница ( интерфейс ) между двумя фазами . Герман фон Гельмгольц [1] был первым, кто осознал, что заряженные электроды, погруженные в растворы электролитов, отталкивают коионы заряда, одновременно притягивая к своей поверхности противоионы. На границе раздела электрод-электролит образуются два слоя противоположной полярности . В 1853 году он показал, что двойной электрический слой (DL) по существу является молекулярным диэлектриком и сохраняет заряд электростатически. [2] Ниже напряжения разложения электролита накопленный заряд линейно зависит от приложенного напряжения.
Эта ранняя модель предсказывала постоянную дифференциальную емкость , независимую от плотности заряда и зависящую от диэлектрической проницаемости растворителя электролита и толщины двойного слоя. [3] [4] [5]
Эта модель, имеющая хорошую основу для описания интерфейса, не учитывает такие важные факторы, как диффузия/смешивание ионов в растворе, возможность адсорбции на поверхность и взаимодействие дипольных моментов растворителя и электрода.
Луи Жорж Гуи в 1910 году и Дэвид Леонард Чепмен в 1913 году заметили, что емкость не является постоянной величиной и зависит от приложенного потенциала и концентрации ионов. «Модель Гуи – Чепмена» внесла значительные улучшения за счет введения диффузной модели DL. В этой модели распределение заряда ионов в зависимости от расстояния от поверхности металла позволяет применить статистику Максвелла – Больцмана . Таким образом, электрический потенциал экспоненциально уменьшается по мере удаления от поверхности объема жидкости. [3] [6]
Слои Гуи-Чепмена могут иметь особое значение в биоэлектрохимии. Наблюдение межбелкового переноса электронов на большие расстояния через водный раствор [7] было приписано диффузной области между окислительно-восстановительными белками-партнерами ( цитохромами с и с1 ) , которая обеднена катионами по сравнению с объемом раствора, что приводит к к уменьшению экранирования , электрическим полям, простирающимся на несколько нанометров, и токам, уменьшающимся квазиэкспоненциально с расстоянием со скоростью ~1 нм -1 . Эта область называется «каналом Гуи-Чепмена» [7] и строго регулируется фосфорилированием , которое добавляет один отрицательный заряд к поверхности белка, что нарушает истощение катионов и предотвращает перенос заряда на большие расстояния. [8] Аналогичные эффекты наблюдаются в окислительно-восстановительном центре фотосинтетических комплексов . [9]
Модель Гуи-Чепмена не работает для DL с высоким зарядом. В 1924 году Отто Штерн предложил объединить модель Гельмгольца с моделью Гуи-Чепмена: в модели Штерна некоторые ионы прилипают к электроду, как предложил Гельмгольц, образуя внутренний слой Штерна, а некоторые образуют диффузный слой Гуи-Чепмена. [10]
Слой Штерна учитывает конечный размер ионов, и, следовательно, наименьшее приближение иона к электроду имеет порядок ионного радиуса. Модель Штерна имеет свои ограничения, а именно то, что она эффективно рассматривает ионы как точечные заряды, предполагает, что все существенные взаимодействия в диффузном слое являются кулоновскими , предполагает, что диэлектрическая проницаемость постоянна во всем двойном слое, и что вязкость жидкости является постоянной плоскостью. [11]

Д.С. Грэм модифицировал модель Штерна в 1947 году. [12] Он предположил, что некоторые ионные или незаряженные частицы могут проникать в слой Штерна, хотя ближайший подход к электроду обычно занят молекулами растворителя. Это может произойти, если ионы потеряют сольватную оболочку при приближении к электроду. Ионы, находящиеся в непосредственном контакте с электродом, он назвал «специфически адсорбированными ионами». Эта модель предполагала существование трех регионов. Внутренняя плоскость Гельмгольца (ВГП) проходит через центры специфически адсорбированных ионов. Внешняя плоскость Гельмгольца (ОНП) проходит через центры сольватированных ионов на расстоянии их наибольшего приближения к электроду. [13] Наконец, диффузный слой — это область за пределами OHP.
В 1963 году Дж. О'М. Бокрис , М.А.В. Деванатан и Клаус Мюллер [14] предложили модель двойного слоя BDM, включающую действие растворителя на границе раздела. Они предположили, что присоединенные молекулы растворителя, например воды, будут иметь фиксированное выравнивание по поверхности электрода. Этот первый слой молекул растворителя демонстрирует сильную ориентацию по отношению к электрическому полю в зависимости от заряда. Эта ориентация оказывает большое влияние на диэлектрическую проницаемость растворителя, которая меняется в зависимости от напряженности поля. ИГП проходит через центры этих молекул. В этом слое появляются специфически адсорбированные, частично сольватированные ионы. Сольватированные ионы электролита находятся вне ИГП. Через центры этих ионов проходят ОНП. Диффузный слой — это область за пределами ОНП.
Дальнейшие исследования двойных слоев пленок диоксида рутения в 1971 году, проведенные Серджио Трасатти и Джованни Буццанка, показали, что электрохимическое поведение этих электродов при низких напряжениях со специфическими адсорбированными ионами было похоже на поведение конденсаторов. Специфическая адсорбция ионов в этой области потенциала может также включать частичный перенос заряда между ионом и электродом. Это был первый шаг к пониманию псевдоемкости. [4]
Между 1975 и 1980 годами Брайан Эванс Конвей провел обширную фундаментальную и исследовательскую работу в области электрохимических конденсаторов на основе оксида рутения . В 1991 году он описал разницу между поведением «суперконденсатора» и «батареи» при электрохимическом хранении энергии. В 1999 году он ввел термин «суперконденсатор», чтобы объяснить увеличение емкости поверхностными окислительно-восстановительными реакциями с фарадеевским переносом заряда между электродами и ионами. [15] [16]
Его «суперконденсатор» хранил электрический заряд частично в двойном слое Гельмгольца, а частично в результате фарадеевских реакций с «псевдоемкостным» переносом заряда электронов и протонов между электродом и электролитом. Механизмами работы псевдоконденсаторов являются окислительно-восстановительные реакции, интеркаляция и электросорбция.
Физические и математические основы переноса заряда электроном в отсутствие химических связей, приводящего к псевдоемкости, были разработаны Рудольфом А. Маркусом . Теория Маркуса объясняет скорость реакций переноса электрона — скорость, с которой электрон может переходить от одного химического вида к другому. Первоначально он был сформулирован для рассмотрения реакций переноса электрона во внешней сфере , в которых два химических соединения изменяются только по своему заряду с перескоком электрона. Для окислительно-восстановительных реакций без образования или разрыва связей теория Маркуса заменяет теорию переходного состояния Генри Айринга , которая была выведена для реакций со структурными изменениями. За эту теорию Маркус получил Нобелевскую премию по химии в 1992 году. [17]
Подробные описания межфазной ДЛ есть во многих книгах по коллоидам и науке о границах раздела [18] [19] [20] и микромасштабному транспорту жидкости. [21] [22] Существует также недавний технический отчет IUPAC [23] по теме двойного межфазного слоя и связанных с ним электрокинетических явлений .
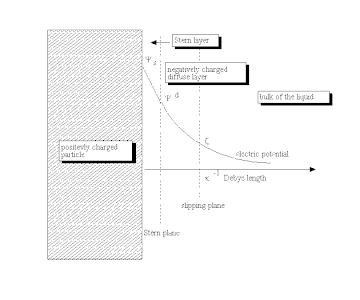
Как утверждает Ликлема, «...причиной образования «релаксированного» («равновесного») двойного слоя является неэлектрическое сродство зарядоопределяющих ионов к поверхности...» [ 24] Этот процесс приводит к накоплению электрического поверхностного заряда , обычно выражаемого в Кл/м 2 . Этот поверхностный заряд создает электростатическое поле, которое затем воздействует на ионы в объеме жидкости. Это электростатическое поле в сочетании с тепловым движением ионов создает встречный заряд и, таким образом, экранирует электрический поверхностный заряд. Суммарный электрический заряд в этом экранирующем диффузном слое равен по величине суммарному поверхностному заряду, но имеет противоположную полярность. В результате вся структура является электрически нейтральной.
Диффузный слой или, по крайней мере, его часть может перемещаться под действием касательных напряжений . Традиционно вводится плоскость скольжения, которая отделяет подвижную жидкость от жидкости, которая остается прикрепленной к поверхности. Электрический потенциал в этой плоскости называется электрокинетическим потенциалом или дзета-потенциалом (также обозначается как ζ-потенциал). [25] [26]
Электрический потенциал на внешней границе слоя Штерна относительно объемного электролита называется потенциалом Штерна . Разность электрических потенциалов между объемом жидкости и поверхностью называется электрическим поверхностным потенциалом.
Обычно дзета-потенциал используется для оценки степени заряда DL. Характерное значение этого электрического потенциала в ДЛ составляет 25 мВ с максимальным значением около 100 мВ (до нескольких вольт на электродах [22] [27] ). Химический состав образца, при котором ζ-потенциал равен 0, называется точкой нулевого заряда или изоэлектрической точкой . Обычно его определяют по значению pH раствора, поскольку протоны и гидроксильные ионы являются ионами, определяющими заряд для большинства поверхностей. [22] [24]
Дзета-потенциал можно измерить с помощью электрофореза , электроакустических явлений , потенциала потока и электроосмотического потока .
Характерной толщиной ДЛ является дебаевская длина κ −1 . Он обратно пропорционален квадратному корню из концентрации ионов C. В водных растворах она обычно составляет несколько нанометров, и толщина уменьшается с увеличением концентрации электролита.
Напряженность электрического поля внутри ДЛ может составлять от нуля до более 10 9 В/м. Эти крутые градиенты электрического потенциала являются причиной важности DL.
Теорию плоской поверхности и симметричного электролита [24] обычно называют теорией Гуи-Чепмена. Это дает простую связь между электрическим зарядом в диффузном слое σ d и потенциалом Штерна Ψ d : [28]
Не существует общего аналитического решения для смешанных электролитов, искривленных поверхностей или даже сферических частиц. Существует асимптотическое решение для сферических частиц с малозаряженными ДЛ. В случае, когда электрический потенциал на ДЛ меньше 25 мВ, справедливо так называемое приближение Дебая-Хюккеля. Это дает следующее выражение для электрического потенциала Ψ в сферической ДЛ в зависимости от расстояния r от центра частицы:
Существует несколько асимптотических моделей, которые играют важную роль в теоретических разработках, связанных с межфазным ДЛ.
Первый из них — «тонкий DL». Эта модель предполагает, что DL намного тоньше радиуса коллоидной частицы или капилляра. Это ограничивает значение дебаевской длины и радиуса частицы следующим образом:
Эта модель предлагает огромные упрощения для многих последующих приложений. Теория электрофореза – лишь один из примеров. [29] Другим примером является теория электроакустических явлений . [30]
Модель тонкой ДЛ справедлива для большинства водных систем, поскольку в таких случаях дебаевская длина составляет всего несколько нанометров. Он распадается только на наноколлоиды в растворе с ионной силой, близкой к воде.
Противоположная модель «толстого DL» предполагает, что длина Дебая больше радиуса частицы:
Эта модель может быть полезна для некоторых наноколлоидов и неполярных жидкостей, где дебаевская длина намного больше.
Последняя модель представляет «перекрывающиеся DL». [30] Это важно в концентрированных дисперсиях и эмульсиях, когда расстояния между частицами становятся сравнимыми с дебаевской длиной.
Двойной электрический слой ( ДЭС ) является результатом изменения электрического потенциала вблизи поверхности и оказывает существенное влияние на поведение коллоидов и других поверхностей в контакте с растворами или твердотельными проводниками быстрых ионов .
Основное отличие двойного слоя на электроде от слоя на границе раздела заключается в механизме образования поверхностного заряда . С помощью электрода можно регулировать поверхностный заряд, прикладывая внешний электрический потенциал. Однако такое применение невозможно в коллоидных и пористых двойных слоях, поскольку для коллоидных частиц нет доступа внутрь частицы для приложения разности потенциалов.
ДЭС аналогичны двойному слою в плазме .
У EDL есть дополнительный параметр, определяющий их характеристики: дифференциальная емкость . Дифференциальная емкость, обозначаемая C , описывается уравнением ниже:
где σ — поверхностный заряд , а ψ — электрический поверхностный потенциал .
Традиционно считалось, что в формировании двойного электрического слоя (ДЭС) полностью преобладают адсорбция и перераспределение ионов. Учитывая тот факт, что в контактной электрификации между твердым телом преобладает перенос электронов, Ван предполагает, что EDL формируется в результате двухэтапного процесса. [31] На первом этапе, когда молекулы в растворе впервые приближаются к чистой поверхности, не имеющей ранее существовавших поверхностных зарядов, возможно, что атомы/молекулы в растворе напрямую взаимодействуют с атомами на твердой поверхности, чтобы образуют сильное перекрытие электронных облаков. Перенос электронов происходит первым, чтобы «нейтральные» атомы на твердой поверхности стали заряженными, т. е. происходит образование ионов. На втором этапе, если в жидкости существуют ионы, такие как H+ и OH-, слабо распределенные отрицательные ионы в растворе будут притягиваться и мигрировать к ионам, связанным с поверхностью, из-за электростатических взаимодействий, образуя ДЭС. На границе раздела жидкость-твердое тело сосуществуют как перенос электронов, так и перенос ионов. [32]
