В химии и молекулярной физике флюксионные ( или нежесткие ) молекулы — это молекулы , которые подвергаются такой динамике, что некоторые или все их атомы меняют местами эквивалентные по симметрии положения. [1] Поскольку практически все молекулы в некоторых отношениях являются флюксиальными, например, вращение связей в большинстве органических соединений , термин флюксиальный зависит от контекста и метода, используемого для оценки динамики. Часто молекулу считают флюкционной, если ее спектроскопическая характеристика демонстрирует уширение линии (сверх того, что продиктовано принципом неопределенности Гейзенберга ) из-за химического обмена. [2] В некоторых случаях, когда скорости медленные, текучесть обнаруживается не спектроскопически, а с помощью изотопной маркировки и других методов. [3]
Многие металлоорганические соединения обладают текучестью. [4] Однако нестабильность широко распространена.
Зависимые от температуры изменения в спектрах ЯМР являются результатом динамики, связанной с потоковыми молекулами, когда эта динамика протекает со скоростью, сравнимой с разницей частот, наблюдаемой с помощью ЯМР. Эксперимент называется DNMR и обычно включает запись спектров при различных температурах. В идеальном случае низкотемпературные спектры можно отнести к «пределу медленного обмена», тогда как спектры, записанные при более высоких температурах, соответствуют молекулам на «пределе быстрого обмена». Обычно высокотемпературные спектры проще, чем спектры, записанные при низких температурах, поскольку при высоких температурах эквивалентные участки усредняются. До появления ДНМР кинетику реакций измеряли на неравновесных смесях, отслеживая приближение к равновесию.
Многие молекулярные процессы демонстрируют текучесть, которую можно исследовать во временной шкале ЯМР. [5] Помимо приведенных ниже примеров, другие классические примеры включают перегруппировку Коупа в буллвалене и инверсию стула в циклогексане .
Для процессов, которые слишком медленны для традиционного анализа ДНМР, применим метод переноса спинового насыщения (SST, также называемый EXSY для обменной спектроскопии). Этот метод переноса намагничивания дает информацию о скорости, при условии, что скорости превышают 1/ T 1 . [6]
Хотя это и менее распространено, некоторая динамика также наблюдается во временной шкале ИК-спектроскопии . Одним из примеров является перенос электрона в димере смешанной валентности металлических кластеров . Применение уравнения слияния двух сигналов, разделенных расстоянием 10 см -1, дает следующий результат: [7]
Очевидно, что процессы, вызывающие уширение линий в масштабе времени ИК, должны быть гораздо более быстрыми, чем случаи, которые обмениваются в масштабе времени ЯМР.
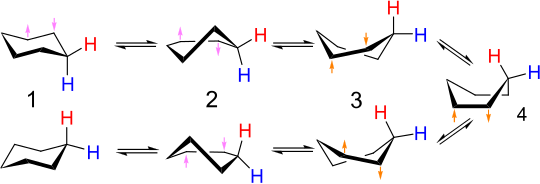
Взаимное превращение эквивалентных конформеров стула циклогексана (и многих других циклических соединений) называется переворачиванием кольца . Углеродно-водородные связи, осевые в одной конфигурации, становятся экваториальными в другой, и наоборот. При комнатной температуре две конформации стула быстро уравновешиваются . Спектры ЯМР протонов и углерода -13 циклогексана показывают только синглеты вблизи комнатной температуры. При низких температурах синглет в спектре ЯМР 1 Н декоалесцирует, но спектр ЯМР 13 С остается неизменным. [9]

Прототипом флюсивной молекулы является пентафторид фосфора . Его спектр ЯМР 19 F состоит из дублета, связанного с 31 P, что указывает на то, что экваториальные и аксиальные центры фтора быстро меняются местами в шкале времени ЯМР. Спектроскопия ЯМР фтора-19 даже при таких низких температурах, как -100 ° C, не позволяет отличить аксиальную среду фтора от экваториальной. Кажущаяся эквивалентность возникает из-за низкого барьера псевдовращения по механизму Берри , посредством которого аксиальные и экваториальные атомы фтора быстро меняют положения. [10] Пентакарбонил железа (Fe(CO) 5 ) следует схеме, установленной для PF 5 : в спектре ЯМР 13 С вблизи комнатной температуры наблюдается только один сигнал ), тогда как при низких температурах могут быть два сигнала в соотношении 2:3. решено. В тетрафториде серы (SF 4 ) наблюдается аналогичная картина, хотя у этого соединения всего четыре лиганда.
Хорошо изученным флюксионным ионом является ион метана CH .+
5. [11] Даже при абсолютном нуле не существует жесткой молекулярной структуры; Атомы H всегда находятся в движении. Точнее, пространственное распределение протонов в CH+
5во много раз шире своей родительской молекулы CH 4 , метана. [12] [13]
В то время как нежесткость характерна для пятикоординатных видов, шестикоординированные виды обычно принимают более жесткую октаэдрическую молекулярную геометрию , характеризующуюся плотноупакованным массивом из шести лигирующих атомов, окружающих центральный атом. Такие соединения действительно перестраиваются внутримолекулярно посредством скручивания Рэя-Датта и скручивания Бейлара , но барьеры для этих процессов обычно высоки, так что эти процессы не приводят к уширению линий. Для некоторых соединений динамика происходит за счет диссоциации лиганда с образованием пятикоординатного промежуточного соединения, на которое действуют механизмы, обсуждавшиеся выше. Еще один механизм, демонстрируемый Fe(CO) 4 (SiMe 3 ) 2 и родственными гидридными комплексами, представляет собой внутримолекулярный перебор лигандов по граням тетраэдра, определяемого четырьмя лигандами CO. [14]
Классическим примером флюкционной молекулы является диметилформамид (ДМФ). [15]

При температуре около 100 ° C спектр 1 H ЯМР ДМФА на частоте 500 МГц показывает только один сигнал метильных групп. Однако при комнатной температуре наблюдаются отдельные сигналы для неэквивалентных метильных групп. Скорость обмена можно рассчитать при температуре, при которой два сигнала только что сливаются. Эта «температура слияния» зависит от измерительного поля. Соответствующее уравнение:
где Δν o – разница в Гц между частотами обменивающихся узлов. Эти частоты получены из предельного низкотемпературного спектра ЯМР. При таких более низких температурах динамика, конечно, продолжается, но вклад динамики в уширение линий незначителен.
Например, если Δν o = 1 ppm при 500 МГц
Соединение Fe(η 5 -C 5 H 5 )(η 1 -C 5 H 5 )(CO) 2 проявляет явление «свиста кольца».
При 30°C спектр 1 H ЯМР показывает только два пика: один типичный (δ5,6) для η 5 -C 5 H 5 , а другой соответствует η 1 -C 5 H 5 . Синглет, принадлежащий лиганду η 1 -C 5 H 5 , расщепляется при низких температурах вследствие медленного перескока Fe-центра от углерода к углероду в лиганде η 1 -C 5 H 5 . [16] Были предложены два механизма, при этом консенсус отдает предпочтение пути сдвига 1,2. [17]
{{cite book}}: CS1 maint: отсутствует местоположение издателя ( ссылка )