

Комплексы переходного металла с азотом представляют собой координационные соединения , содержащие переходные металлы в качестве ионных центров и молекулы азота (N 2 ) в качестве лигандов . [2]
Комплексы переходных металлов N 2 изучаются с 1965 года, когда Аллен и Сенофф сообщили о первом комплексе. [3] Этот диамагнитный комплекс [Ru(NH 3 ) 5 (N 2 )] 2+ был синтезирован из гидразингидрата и трихлорида рутения и состоит из центра [Ru(NH 3 ) 5 ] 2+, присоединенного к одному концу Н 2 . [4] [5] Существование N 2 в качестве лиганда в этом соединении было идентифицировано по ИК-спектру с сильной полосой около 2170–2100 см -1 . [4] В 1966 году молекулярная структура [Ru(NH 3 ) 5 (N 2 )]Cl 2 была определена Боттомли и Нюбургом методом рентгеновской кристаллографии . [6]
Диназотный комплекс транс- [IrCl(N 2 )(PPh 3 ) 2 ] получают обработкой комплекса Васки ароматическими ацилазидами . Имеет плоскую геометрию. [7]
О первом получении комплекса металл-диазот с использованием динитрога сообщили в 1967 году Ямамото и его коллеги. Они получили [Co(H)(N 2 )(PPh 3 ) 3 ] восстановлением Co(acac) 3 с помощью AlEt 2 OEt в атмосфере N 2 . Содержащий как гидридо, так и лиганды N 2 , комплекс потенциально имел отношение к фиксации азота. [8]
С конца 1960-х годов были созданы различные комплексы переходного металла с азотом, в том числе с железом, [9] молибденом [10] и ванадием [11] в качестве металлических центров. Интерес к таким комплексам возникает потому, что N 2 составляет большую часть атмосферы и многие полезные соединения содержат азот. Биологическая фиксация азота , вероятно, происходит посредством связывания N 2 с металлическими центрами фермента нитрогеназы , за которым следует ряд стадий, включающих перенос электронов и протонирование . [12]
С точки зрения связи с переходными металлами N 2 связан с CO и ацетиленом , поскольку все три соединения имеют тройные связи . Охарактеризованы различные способы соединения. В зависимости от того, являются ли молекулы N 2 общими еще для двух металлоцентров, комплексы можно разделить на моноядерные и мостиковые. В зависимости от геометрического соотношения между молекулой N 2 и металлическим центром комплексы можно разделить на типы «конец» или «бок». В режимах связи с торца комплексов переходного металла с азотом вектор NN можно рассматривать на одной линии с центром иона металла, тогда как в режимах с боковым расположением связь металл-лиганд, как известно, перпендикулярна вектору NN. . [13]
В качестве лиганда N 2 обычно связывается с металлами как лиганд "конец на конце", как показано на примере [Ru(NH 3 ) 5 N 2 ] 2+ . Такие комплексы обычно аналогичны родственным производным CO. Эту связь иллюстрирует пара комплексов IrCl(CO)(PPh 3 ) 2 и IrCl(N 2 )(PPh 3 ) 2 . [14] В этих моноядерных случаях N 2 выступает как σ-донором, так и π-акцептором. Валентные углы MNN близки к 180°. [2] N 2 является более слабым пи-акцептором, чем CO, что отражает природу π*-орбиталей CO по сравнению с N 2 . По этой причине существует мало примеров комплексов, содержащих как CO, так и лиганд N 2 .
Комплексы переходного металла с азотом могут содержать более одного N 2 в качестве «концевых» лигандов, например мер- [Mo(N 2 ) 3 (PPr n 2 Ph) 3 ], который имеет октаэдрическую геометрию. [15] В другом примере диазотистый лиганд в Mo(N 2 ) 2 (Ph 2 PCH 2 CH 2 PPh 2 ) 2 может быть восстановлен с получением аммиака. [16] Поскольку многие нитрогеназы содержат Mo, особый интерес вызывают комплексы Mo-N 2 .
N 2 также служит мостиковым лигандом, связывающимся «концом» с двумя металлическими центрами, как показано на примере {[Ru(NH 3 ) 5 ] 2 (μ-N 2 )} 4+ . Эти комплексы еще называют многоядерными диазотными комплексами. В отличие от своего моноядерного аналога их можно получать как из ранних, так и из поздних переходных металлов. [2]
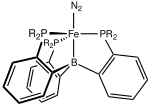
В 2006 году исследование комплексов железа с азотом, проведенное Холландом и его сотрудниками, показало, что связь N–N значительно ослабляется при комплексообразовании с атомами железа с низким координационным числом. В состав комплекса входят бидентатно-хелатирующие лиганды, присоединенные к атомам железа в ядре Fe-N-N-Fe, в котором N 2 выступает в качестве мостикового лиганда между двумя атомами железа. Увеличение координационного числа железа за счет модификации хелатирующих лигандов и добавления еще одного лиганда на атом железа показало увеличение прочности связи N–N в образующемся комплексе. Таким образом, предполагается, что Fe в среде с низкой координацией является ключевым фактором фиксации азота ферментом нитрогеназой , поскольку его кофактор Fe-Mo также содержит Fe с низкими координационными числами. [17]
Средняя длина связи этих комплексов диазота с мостиком-концом составляет около 1,2 Å. В некоторых случаях длина связи может достигать 1,4 Å, что аналогично длине одинарных связей NN. [18] Хасанайн и его коллеги показали, что структуры Льюиса мостиковых комплексов могут быть определены на основе занятости π-молекулярных орбиталей по аналогии с простыми тетратомными органическими молекулами. Например, ядра N 2 -мостиковых комплексов с 8, 10 или 12 π-электронами обычно можно сформулировать соответственно как M≡NN≡M, M=N=N=M и MN≡NM по аналогии с органические молекулы с 8, 10 и 12 π-электронами HC≡CC≡CH, O=C=C=O и FC≡CF. [19]
По сравнению со своим боковым аналогом моноядерные боковые комплексы азота обычно имеют более высокую энергию, и их примеры редки. Динитроген действует как π-донор в комплексах такого типа. Фомичев и Коппенс сообщили о первых кристаллографических доказательствах боковой координации N 2 с одним металлическим центром в фотоиндуцированном метастабильном состоянии. При обработке УФ-светом комплекс переходного металла с азотом [Os(NH 3 ) 5 (N 2 )] 2+ в твердом состоянии может перейти в метастабильное состояние [Os(NH 3 ) 5 (η 2 -N 2 )] 2+ , где колебание диазота сместилось с 2025 до 1831 см -1 .
Считается, что некоторые другие примеры существуют в переходных состояниях изомеризации внутримолекулярных связей. Армор и Таубе сообщили об этих изомеризациях с использованием 15 N-меченного динитрогена в качестве лигандов. [20]
Известны биметаллические комплексы второго типа мостикового соединения, в которых вектор NN перпендикулярен вектору MM, что можно рассматривать как боковой способ. Одним из примеров является [(η 5 -C 5 Me 4 H) 2 Zr] 2 ( μ 2 , η 2 , η 2 -N 2 ). [21] Диметаллический комплекс может реагировать с H 2 для достижения искусственной фиксации азота за счет восстановления N 2 . [22] Родственный комплекс тетрагидрида дитантала также может восстанавливать N 2. [23]
При получении нитридокомплексов металлов из N2 предполагается промежуточное положение диазотного комплекса. Некоторые комплексы Mo(III) также расщепляют N 2 : [24]
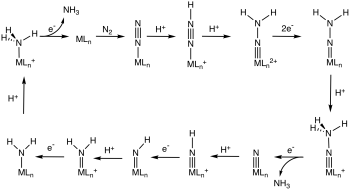
Некоторые богатые электронами комплексы металла и азота чувствительны к атаке электрофилов на азот. Когда электрофилом является протон, реакция представляет интерес с точки зрения абиологической фиксации азота . Некоторые комплексы металл-дитроген даже катализируют гидрирование N 2 до аммиака в цикле, включающем N-протонирование восстановленного комплекса MN 2 . [25] [26]