Диоксид урана или оксид урана(IV) (UO2), также известный как уран или закись урана, является оксидом урана и представляет собой черный радиоактивный кристаллический порошок , который естественным образом встречается в минерале уранините . Он используется в ядерных топливных стержнях в ядерных реакторах . Смесь диоксидов урана и плутония используется в качестве МОКС-топлива . До 1960 года он использовался в качестве желтого и черного цвета в керамических глазурях и стекле.
Диоксид урана получают путем восстановления триоксида урана водородом .
Эта реакция играет важную роль в создании ядерного топлива путем переработки ядерного топлива и обогащения урана .
Твердое тело изоструктурно (имеет ту же структуру, что и) флюорит ( фторид кальция ), где каждый U окружен восемью ближайшими соседями O в кубическом расположении. Кроме того, диоксиды церия , тория и трансурановые элементы от нептуния до калифорния имеют те же структуры. [3] Никакие другие элементарные диоксиды не имеют структуру флюорита. При плавлении измеренная средняя координация UO уменьшается с 8 в кристаллическом твердом теле (кубы UO 8 ) до 6,7 ± 0,5 (при 3270 К) в расплаве. [4] Модели, согласующиеся с этими измерениями, показывают, что расплав состоит в основном из полиэдрических единиц UO 6 и UO 7 , где примерно 2 ⁄ 3 связей между полиэдрами являются общими углами и 1 ⁄ 3 являются общими ребрами. [4]
Диоксид урана окисляется при контакте с кислородом до октаоксида триурана .
Электрохимия диоксида урана была подробно исследована, поскольку гальваническая коррозия диоксида урана контролирует скорость, с которой растворяется отработанное ядерное топливо. См. отработанное ядерное топливо для получения более подробной информации. Вода увеличивает скорость окисления плутония и урана. [5] [6]
Диоксид урана при контакте с углеродом обугливается , образуя карбид урана и оксид углерода .
Этот процесс необходимо проводить в атмосфере инертного газа , поскольку карбид урана легко окисляется обратно в оксид урана .
UO2 используется в основном в качестве ядерного топлива , в частности в виде UO2 или в виде смеси UO2 и PuO2 ( диоксида плутония ), называемой смешанным оксидом ( МОКС-топливо ), в виде топливных стержней в ядерных реакторах .
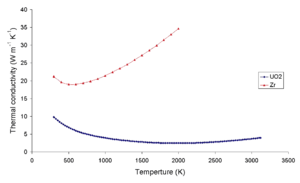
Теплопроводность диоксида урана очень низкая по сравнению с ураном , нитридом урана , карбидом урана и циркониевым материалом оболочки. Эта низкая теплопроводность может привести к локальному перегреву в центрах топливных таблеток. На графике ниже показаны различные температурные градиенты в различных топливных соединениях. Для этих видов топлива тепловая плотность мощности одинакова, а диаметр всех таблеток одинаков. [ необходима цитата ]
Оксид урана (уран) использовался для окрашивания стекла и керамики до Второй мировой войны, и пока не были открыты возможности применения радиоактивности, это было его основным применением. В 1958 году военные США и Европы снова разрешили его коммерческое использование в качестве обедненного урана, и его использование снова началось в более ограниченных масштабах. Керамические глазури на основе урана имеют темно-зеленый или черный цвет при обжиге в восстановлении или при использовании UO2 ; чаще всего его используют при окислении для получения ярко-желтых, оранжевых и красных глазурей. [7] Оранжевый цвет Fiestaware является хорошо известным примером продукта с глазурью цвета урана. Урановое стекло имеет цвет от бледно-зеленого до желтого и часто обладает сильными флуоресцентными свойствами. Урана также использовали в составах эмали и фарфора . С помощью счетчика Гейгера можно определить , содержит ли глазурь или стекло, произведенные до 1958 года, уран.
До того, как стало известно о вреде радиации, уран включали в состав искусственных зубов и зубных протезов, поскольку его слабая флуоресценция делала зубные протезы более похожими на настоящие зубы при различных условиях освещения. [ необходима цитата ]
Обедненный UO 2 (DUO 2 ) может использоваться в качестве материала для радиационной защиты . Например, DUCRETE — это материал «тяжелого бетона », в котором гравий заменен наполнителем из диоксида урана; этот материал исследуется для использования в контейнерах для радиоактивных отходов . Контейнеры также могут быть изготовлены из DUO 2 — стальной металлокерамики , композитного материала, изготовленного из агрегата диоксида урана, служащего радиационной защитой, графита и/или карбида кремния, служащего поглотителем нейтронного излучения и замедлителем, и стали в качестве матрицы, чья высокая теплопроводность позволяет легко отводить остаточное тепло. [ необходима цитата ]
Обедненный диоксид урана может также использоваться в качестве катализатора , например, для разложения летучих органических соединений в газообразной фазе, окисления метана в метанол и удаления серы из нефти . Он обладает высокой эффективностью и долговременной стабильностью при использовании для разрушения ЛОС по сравнению с некоторыми коммерческими катализаторами , такими как драгоценные металлы , катализаторы TiO 2 и Co 3 O 4. В этой области проводится много исследований, причем DU предпочитают для уранового компонента из-за его низкой радиоактивности. [8]
Исследуется использование диоксида урана в качестве материала для перезаряжаемых батарей . Батареи могут иметь высокую плотность мощности и потенциал 4,7 В на ячейку. Другое исследуемое применение — фотоэлектрохимические ячейки для производства водорода с помощью солнечной энергии, где UO 2 используется в качестве фотоанода . Ранее диоксид урана также использовался в качестве теплопроводника для ограничения тока (URDOX-резистор), что было первым применением его полупроводниковых свойств. [ необходима цитата ]
Диоксид урана проявляет сильный пьезомагнетизм в антиферромагнитном состоянии, наблюдаемом при криогенных температурах ниже 30 кельвинов . Соответственно, линейная магнитострикция , обнаруженная в UO2 , меняет знак с приложенным магнитным полем и демонстрирует явления переключения магнитоупругой памяти при рекордно высоких полях переключения 180 000 Э. [9] Микроскопическое происхождение магнитных свойств материала кроется в симметрии гранецентрированной кубической кристаллической решетки атомов урана и ее реакции на приложенные магнитные поля. [10]
Ширина запрещенной зоны диоксида урана сопоставима с таковыми у кремния и арсенида галлия , близка к оптимальной для эффективности кривой зависимости ширины запрещенной зоны для поглощения солнечного излучения, что предполагает его возможное использование для очень эффективных солнечных элементов на основе структуры диода Шоттки ; он также поглощает на пяти различных длинах волн, включая инфракрасный, что еще больше повышает его эффективность. Его собственная проводимость при комнатной температуре примерно такая же, как у монокристаллического кремния. [11]
Диэлектрическая проницаемость диоксида урана составляет около 22, что почти вдвое выше, чем у кремния (11,2) и GaAs (14,1). Это преимущество перед Si и GaAs при построении интегральных схем , поскольку оно может обеспечить более высокую плотность интеграции с более высокими пробивными напряжениями и с меньшей восприимчивостью к туннельному пробою КМОП .
Коэффициент Зеебека диоксида урана при комнатной температуре составляет около 750 мкВ/К, что значительно превышает значение 270 мкВ/К для теллурида таллия и олова (Tl 2 SnTe 5 ) и теллурида таллия и германия (Tl 2 GeTe 5 ), а также для сплавов висмута с теллуром , других материалов, перспективных для применения в термоэлектрической энергетике и элементах Пельтье .
Влияние радиоактивного распада 235 U и 238 U на его полупроводниковые свойства не измерялось по состоянию на 2005 год [обновлять]. Из-за медленной скорости распада этих изотопов, это не должно существенно влиять на свойства солнечных элементов на основе диоксида урана и термоэлектрических устройств, но может стать важным фактором для чипов СБИС . По этой причине необходимо использование обедненного оксида урана. Захват альфа-частиц, испускаемых при радиоактивном распаде в виде атомов гелия в кристаллической решетке, также может вызывать постепенные долгосрочные изменения его свойств. [ необходима цитата ]
Стехиометрия материала существенно влияет на его электрические свойства. Например, электропроводность UO 1,994 на порядки ниже при более высоких температурах, чем проводимость UO 2,001 [ требуется цитата ] .
Диоксид урана, как и U3O8 , представляет собой керамический материал, способный выдерживать высокие температуры (около 2300 °C, по сравнению с максимум 200 ° C для кремния или GaAs), что делает его пригодным для высокотемпературных применений, таких как термофотоэлектрические устройства.
Диоксид урана также устойчив к радиационному воздействию, что делает его пригодным для создания радиационно-стойких устройств специального военного и аэрокосмического назначения.
Диод Шоттки из U3O8 и pnp - транзистор из UO2 были успешно изготовлены в лабораторных условиях. [ 12]
Известно, что диоксид урана поглощается путем фагоцитоза в легких. [13]
{{cite journal}}: Цитировать журнал требует |journal=( помощь )