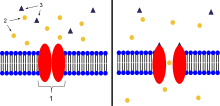
Лиганд-управляемые ионные каналы ( LIC , LGIC ), также часто называемые ионотропными рецепторами , представляют собой группу трансмембранных белков ионных каналов , которые открываются для пропуска ионов, таких как Na + , K + , Ca 2+ и/или Cl -. проходить через мембрану в ответ на связывание химического посланника (т.е. лиганда ) , такого как нейромедиатор . [1] [2] [3]
Когда пресинаптический нейрон возбуждается, он высвобождает нейромедиатор из везикул в синаптическую щель . Затем нейромедиатор связывается с рецепторами, расположенными на постсинаптическом нейроне . Если эти рецепторы представляют собой ионные каналы, управляемые лигандами, в результате конформационного изменения открываются ионные каналы, что приводит к потоку ионов через клеточную мембрану. Это, в свою очередь, приводит либо к деполяризации для реакции возбуждающего рецептора, либо к гиперполяризации для тормозной реакции.
Эти рецепторные белки обычно состоят по меньшей мере из двух разных доменов: трансмембранного домена, который включает ионную пору, и внеклеточного домена, который включает место связывания лиганда (аллостерический сайт связывания). Эта модульность позволила применить подход «разделяй и властвуй» к поиску структуры белков (кристаллизация каждого домена отдельно). Функция таких рецепторов, расположенных в синапсах , заключается в прямом и очень быстром преобразовании химического сигнала пресинаптически высвобождаемого нейромедиатора в постсинаптический электрический сигнал. Многие LIC дополнительно модулируются аллостерическими лигандами , блокаторами каналов , ионами или мембранным потенциалом . LIC подразделяются на три суперсемейства, которые не имеют эволюционного родства: рецепторы цис-петли , ионотропные рецепторы глутамата и АТФ-управляемые каналы .

Рецепторы цис-петли названы в честь характерной петли, образованной дисульфидной связью между двумя остатками цистеина в N-концевом внеклеточном домене. Они являются частью более крупного семейства пентамерных лиганд-управляемых ионных каналов, в которых обычно отсутствует эта дисульфидная связь, отсюда и предварительное название «рецепторы пропетли». [4] [5] Сайт связывания во внеклеточном N-концевом лиганд-связывающем домене придает им специфичность к рецепторам (1) ацетилхолина (AcCh), (2) серотонина, (3) глицина, (4) глутамата и (5) γ-аминомасляная кислота (ГАМК) у позвоночных. Рецепторы подразделяются по типу проводимого ими иона (анионные или катионные) и далее на семейства, определяемые эндогенным лигандом. Обычно они являются пентамерными, каждая субъединица содержит 4 трансмембранные спирали , составляющие трансмембранный домен, и внеклеточный, N-концевой, лигандсвязывающий домен типа сэндвича с бета-листом. [6] Некоторые из них также содержат внутриклеточный домен, как показано на изображении.
Прототипом лиганд-управляемого ионного канала является никотиновый ацетилхолиновый рецептор . Он состоит из пентамера белковых субъединиц (обычно ααβγδ) с двумя сайтами связывания ацетилхолина (по одному на границе каждой альфа-субъединицы). Когда ацетилхолин связывается, он изменяет конфигурацию рецептора (скручивает спирали Т2, что выводит остатки лейцина, блокирующие пору, из пути канала) и вызывает расширение поры примерно на 3 ангстрема до примерно 8 ангстрем, так что ионы могут пройти. Эта пора позволяет ионам Na + течь по электрохимическому градиенту в клетку. При одновременном открытии достаточного количества каналов входящий поток положительных зарядов, переносимый ионами Na + , деполяризует постсинаптическую мембрану в достаточной степени, чтобы инициировать потенциал действия .
Был идентифицирован бактериальный гомолог LIC, который, тем не менее, предположительно действует как хеморецептор. [4] Этот прокариотический вариант nAChR известен как рецептор GLIC , по названию вида, у которого он был идентифицирован; Gloeobacter L igand -gate I на канале C.
Рецепторы Cys-петли имеют хорошо консервативные структурные элементы с большим внеклеточным доменом (ECD), содержащим альфа-спираль и 10 бета-цепей. После ECD четыре трансмембранных сегмента (TMS) соединены внутриклеточными и внеклеточными петлевыми структурами. [7] За исключением петли TMS 3-4, их длина составляет всего 7-14 остатков. Петля TMS 3-4 образует большую часть внутриклеточного домена (ICD) и представляет собой наиболее вариабельную область между всеми этими гомологичными рецепторами. ICD определяется петлей TMS 3-4 вместе с петлей TMS 1-2, предшествующей поре ионного канала. [7] Кристаллизация выявила структуры некоторых членов семейства, но для обеспечения кристаллизации внутриклеточная петля обычно заменялась коротким линкером, присутствующим в прокариотических рецепторах цис-петли, поэтому их структура неизвестна. Тем не менее, эта внутриклеточная петля, по-видимому, участвует в десенсибилизации, модуляции физиологии каналов фармакологическими веществами и посттрансляционных модификациях . Там находятся мотивы, важные для транспорта, и ICD взаимодействует с каркасными белками, обеспечивая образование ингибирующих синапсов . [7]
Ионотропные рецепторы глутамата связывают нейромедиатор глутамат . Они образуют тетрамеры, каждая субъединица которых состоит из внеклеточного аминоконцевого домена (ATD, который участвует в сборке тетрамера), внеклеточного лигандсвязывающего домена (LBD, который связывает глутамат) и трансмембранного домена (TMD, который образует ионный канал). . Трансмембранный домен каждой субъединицы содержит три трансмембранные спирали, а также полумембранную спираль с возвратной петлей. Структура белка начинается с ATD на N-конце, за которой следует первая половина LBD, которая прерывается спиралями 1, 2 и 3 TMD, а затем продолжается последней половиной LBD и затем заканчивается спиралью 4 ВНЧС на С-конце. Это означает, что существует три связи между ВНЧС и внеклеточными доменами. Каждая субъединица тетрамера имеет сайт связывания глутамата, образованный двумя участками LBD, образующими форму раскладушки. Только два из этих сайтов в тетрамере должны быть заняты, чтобы открыть ионный канал. Пора в основном образована полуспиралью 2, напоминающей перевернутый калиевый канал .


Рецептор α-амино-3-гидрокси-5-метил-4-изоксазолпропионовой кислоты (также известный как рецептор AMPA или кисквалатный рецептор ) представляет собой ионотропный трансмембранный рецептор не- NMDA -типа для глутамата , который обеспечивает быструю синаптическую передачу в центральной нервной системе. система (ЦНС). Его название происходит от его способности активироваться искусственным аналогом глутамата AMPA . Рецептор был впервые назван «рецептором кисквалата» Уоткинсом и его коллегами в честь встречающегося в природе агониста кисквалата, и только позже ему было присвоено название «рецептор АМРА» в честь селективного агониста, разработанного Таге Оноре и его коллегами в Датской королевской фармацевтической школе в Копенгагене. . [10] AMPAR обнаружены во многих частях мозга и являются наиболее часто встречающимся рецептором в нервной системе . Тетрамер АМРА-рецептора GluA2 (GluR2) был первым кристаллизованным ионным каналом глутаматного рецептора . Лиганды включают:
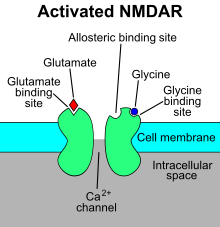
Рецептор N-метил-D-аспартата ( рецептор NMDA ) – тип ионотропного рецептора глутамата – представляет собой лиганд-управляемый ионный канал, который открывается за счет одновременного связывания глутамата и коагониста (т.е. либо D-серина , либо глицин ). [11] Исследования показывают, что рецептор NMDA участвует в регуляции синаптической пластичности и памяти. [12] [13]
Название «рецептор NMDA» происходит от лиганда N-метил-D-аспартата (NMDA), который действует как селективный агонист этих рецепторов. Когда рецептор NMDA активируется связыванием двух коагонистов, катионный канал открывается, позволяя Na + и Ca 2+ поступать в клетку, что, в свою очередь, повышает электрический потенциал клетки . Таким образом, рецептор NMDA является возбуждающим рецептором. При потенциалах покоя связывание Mg 2+ или Zn 2+ в их внеклеточных сайтах связывания на рецепторе блокирует поток ионов через канал рецептора NMDA. «Однако, когда нейроны деполяризуются, например, за счет интенсивной активации колокализованных постсинаптических АМРА-рецепторов , потенциал-зависимая блокада Mg 2+ частично снимается, обеспечивая приток ионов через активированные рецепторы NMDA. Результирующий приток Ca 2+ может вызвать разнообразие внутриклеточных сигнальных каскадов, которые в конечном итоге могут изменить функцию нейронов посредством активации различных киназ и фосфатаз». [14] Лиганды включают:

АТФ-зависимые каналы открываются в ответ на связывание нуклеотида АТФ . Они образуют тримеры с двумя трансмембранными спиралями на субъединицу и C- и N-концами на внутриклеточной стороне.
Лиганд-управляемые ионные каналы, вероятно, являются основным местом действия анестетиков и этанола , хотя однозначные доказательства этого еще не установлены. [16] [17] В частности, на рецепторы ГАМК и NMDA действуют анестетики в концентрациях, аналогичных тем, которые используются в клинической анестезии. [18]
Понимая механизм и исследуя химические/биологические/физические компоненты, которые могут действовать на эти рецепторы, предварительные эксперименты или FDA подтверждают все больше и больше клинических применений . Мемантин одобрен USFDA и Европейским медицинским агентством для лечения болезни Альцгеймера от умеренной до тяжелой степени [19] и в настоящее время получил ограниченную рекомендацию Национального института здравоохранения и передового медицинского обслуживания Великобритании для пациентов, которым другие варианты лечения не помогли. . [20] Агомелатин — это тип препарата, который действует по двойному мелатонинергическому и серотонинергическому пути, который показал свою эффективность при лечении тревожной депрессии во время клинических исследований, [21] [22] исследование также предполагает эффективность при лечении атипичная и меланхолическая депрессия . [23]
{{cite book}}: CS1 maint: несколько имен: список авторов ( ссылка )При мембранных потенциалах, более отрицательных, чем примерно -50 мВ, Mg 2+ во внеклеточной жидкости мозга практически устраняет поток ионов через каналы рецепторов NMDA, даже в присутствии глутамата. ... Рецептор NMDA уникален среди всех рецепторов нейромедиаторов тем, что его активация требует одновременного связывания двух разных агонистов. Помимо связывания глутамата в обычном сайте связывания агониста, для активации рецептора, по-видимому, необходимо связывание глицина. Поскольку ни один из этих агонистов по отдельности не может открыть этот ионный канал, глутамат и глицин называются коагонистами рецептора NMDA. Физиологическое значение сайта связывания глицина неясно, поскольку считается, что нормальная внеклеточная концентрация глицина является насыщающей. Однако недавние данные свидетельствуют о том, что D-серин может быть эндогенным агонистом этого сайта.
На момент редактирования в этой статье используется контент из «1.A.9 The Neurotransmitter Receptor, Cys Loop, Ligand-Gated Ion Channel (LIC) Family» , который лицензируется таким образом, что разрешается повторное использование в соответствии с Creative Commons Attribution-ShareAlike. 3.0 Непортированная лицензия , но не под GFDL . Все соответствующие условия должны быть соблюдены.