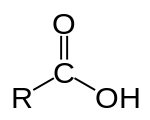


В органической химии карбоновая кислота — это органическая кислота , которая содержит карбоксильную группу ( −C(=O)−OH ) [1], присоединенную к R-группе . Общую формулу карбоновой кислоты часто записывают как R−COOH или R−CO2H , иногда как R−C(O)OH , где R относится к органильной группе (например, алкильной , алкенильной , арильной ), водороду или другим группам. Карбоновые кислоты встречаются широко. Важными примерами являются аминокислоты и жирные кислоты . Депротонирование карбоновой кислоты дает карбоксилат- анион .
Карбоновые кислоты обычно идентифицируются по их тривиальным названиям . Они часто имеют суффикс -ic acid .Также существуют названия, рекомендуемые ИЮПАК ; в этой системе карбоновые кислоты имеют суффикс -овой кислоты . [2] Например, масляная кислота ( CH 3 CH 2 CH 2 CO 2 H ) является бутановой кислотой согласно рекомендациям ИЮПАК. Для номенклатуры сложных молекул, содержащих карбоновую кислоту, карбоксил можно считать позицией один в родительской цепи , даже если есть другие заместители , такие как 3-хлорпропановая кислота . Альтернативно, его можно назвать заместителем «карбокси» или «карбоновой кислоты» в другой родительской структуре, такой как 2-карбоксифуран .
Карбоксилат-анион ( R−COO − или R−CO−2) карбоновой кислоты обычно называют с суффиксом -ate , в соответствии с общей моделью -ic acid и -ate для сопряженной кислоты и ее сопряженного основания соответственно. Например, сопряженное основание уксусной кислоты - ацетат .
Угольная кислота , которая встречается в природе в бикарбонатных буферных системах , обычно не классифицируется как одна из карбоновых кислот, несмотря на то, что она имеет фрагмент , который выглядит как группа COOH.
Карбоновые кислоты являются полярными . Поскольку они являются как акцепторами водородных связей ( карбонил −C(=O)− ), так и донорами водородных связей ( гидроксил −OH ), они также участвуют в образовании водородных связей . Вместе гидроксильная и карбонильная группы образуют функциональную группу карбоксил. Карбоновые кислоты обычно существуют в виде димеров в неполярных средах из-за их тенденции к «самоассоциации». Меньшие карбоновые кислоты (от 1 до 5 атомов углерода) растворимы в воде, тогда как большие карбоновые кислоты имеют ограниченную растворимость из-за возрастающей гидрофобности алкильной цепи. Эти кислоты с более длинной цепью, как правило, растворимы в менее полярных растворителях, таких как эфиры и спирты. [3] Водный гидроксид натрия и карбоновые кислоты, даже гидрофобные, реагируют с образованием водорастворимых солей натрия. Например, энантовая кислота имеет низкую растворимость в воде (0,2 г/л), но ее натриевая соль хорошо растворяется в воде.
Карбоновые кислоты, как правило, имеют более высокие температуры кипения, чем вода, из-за их большей площади поверхности и их тенденции к образованию стабилизированных димеров посредством водородных связей . Для того, чтобы произошло кипение, либо связи димера должны быть разорваны, либо вся димерная структура должна испариться, что значительно увеличивает требования к энтальпии испарения .

Карбоновые кислоты являются кислотами Бренстеда-Лоури, поскольку они являются донорами протона (H + ). Они являются наиболее распространенным типом органических кислот .
Карбоновые кислоты обычно являются слабыми кислотами , что означает, что они лишь частично диссоциируют на катионы [H 3 O] + и R−CO −2 анионы в нейтральном водном растворе. Например, при комнатной температуре в 1- молярном растворе уксусной кислоты диссоциируют только 0,001% кислоты (т.е. 10−5 моль из 1 моль). Электроноакцепторные заместители, такие как группа -CF3 , дают более сильные кислоты (pKa уксусной кислоты составляет 4,76, тогда как трифторуксусная кислота с трифторметильным заместителем имеет apKa 0,23 ) . Электронодонорные заместители дают более слабые кислоты (pKa муравьиной кислоты составляет 3,75, тогда как уксусная кислота с метильным заместителем имеет apKa 4,76 )
Депротонирование карбоновых кислот дает карбоксилатные анионы; они резонансно стабилизированы , поскольку отрицательный заряд делокализован по двум атомам кислорода, что увеличивает стабильность аниона. Каждая из связей углерод-кислород в карбоксилатном анионе имеет частичный характер двойной связи. Частичный положительный заряд карбонильного углерода также ослаблен отрицательными зарядами - 1 / 2 на 2 атомах кислорода.
Карбоновые кислоты часто имеют сильный кислый запах. Эфиры карбоновых кислот, как правило, имеют фруктовые, приятные запахи, и многие из них используются в парфюмерии .
Карбоновые кислоты легко идентифицируются как таковые с помощью инфракрасной спектроскопии . Они демонстрируют острую полосу, связанную с колебанием карбонильной связи C=O ( ν C=O ) между 1680 и 1725 см −1 . Характерная полоса ν O–H появляется как широкий пик в области от 2500 до 3000 см −1 . [3] [6] С помощью спектрометрии ЯМР 1 H гидроксильный водород появляется в области 10–13 ppm, хотя он часто либо уширен, либо не наблюдается из-за обмена со следами воды.
Многие карбоновые кислоты производятся в промышленных масштабах. Они также часто встречаются в природе. Эфиры жирных кислот являются основными компонентами липидов, а полиамиды аминокарбоновых кислот являются основными компонентами белков .
Карбоновые кислоты используются в производстве полимеров, фармацевтических препаратов, растворителей и пищевых добавок. Промышленно важные карбоновые кислоты включают уксусную кислоту (компонент уксуса, предшественник растворителей и покрытий), акриловую и метакриловую кислоты (предшественники полимеров, клеев), адипиновую кислоту (полимеры), лимонную кислоту (ароматизатор и консервант в пищевых продуктах и напитках), этилендиаминтетрауксусную кислоту (хелатирующий агент), жирные кислоты (покрытия), малеиновую кислоту (полимеры), пропионовую кислоту (пищевой консервант), терефталевую кислоту (полимеры). Важные карбоксилатные соли — это мыла.
В целом промышленные способы получения карбоновых кислот отличаются от тех, которые используются в меньших масштабах, поскольку требуют специализированного оборудования.
Методы подготовки для мелкомасштабных реакций в исследовательских целях или для производства тонких химикатов часто требуют использования дорогостоящих расходных реагентов.
Во многих реакциях образуются карбоновые кислоты, но они используются только в особых случаях или представляют в основном академический интерес.

Карбоновые кислоты реагируют с основаниями с образованием карбоксилатных солей, в которых водород гидроксильной ( –ОН ) группы замещен катионом металла . Например, уксусная кислота, содержащаяся в уксусе, реагирует с бикарбонатом натрия (пищевой содой) с образованием ацетата натрия , диоксида углерода и воды:
Широко практикуемые реакции превращают карбоновые кислоты в сложные эфиры , амиды , соли карбоксилатов , хлорангидриды и спирты . Их превращение в сложные эфиры широко используется, например, в производстве полиэфиров . Аналогично, карбоновые кислоты превращаются в амиды , но это превращение обычно не происходит путем прямой реакции карбоновой кислоты и амина. Вместо этого сложные эфиры являются типичными предшественниками амидов. Превращение аминокислот в пептиды является важным биохимическим процессом, требующим АТФ .
Преобразование карбоновой кислоты в амид возможно, но не прямолинейно. Вместо того, чтобы действовать как нуклеофил, амин будет реагировать как основание в присутствии карбоновой кислоты, давая соль карбоксилата аммония . Нагревание соли выше 100 °C приведет к удалению воды и образованию амида. Этот метод синтеза амидов имеет промышленное значение и также имеет лабораторное применение. [9] В присутствии сильного кислотного катализатора карбоновые кислоты могут конденсироваться с образованием ангидридов кислот. Однако конденсация производит воду, которая может гидролизовать ангидрид обратно в исходные карбоновые кислоты. Таким образом, образование ангидрида посредством конденсации является равновесным процессом.
В условиях кислотного катализа карбоновые кислоты будут реагировать со спиртами, образуя эфиры посредством реакции этерификации Фишера , которая также является равновесным процессом. В качестве альтернативы, диазометан может быть использован для преобразования кислоты в эфир. В то время как реакции этерификации с диазометаном часто дают количественные выходы, диазометан полезен только для образования метиловых эфиров. [9]
Подобно сложным эфирам , большинство карбоновых кислот можно восстановить до спиртов путем гидрирования или с использованием переносящих агентов гидрида, таких как алюмогидрид лития . Сильные переносящие агенты алкила, такие как литийорганические соединения, но не реактивы Гриньяра , будут восстанавливать карбоновые кислоты до кетонов вместе с переносом алкильной группы.
Реагент Вильсмейера ( хлорид N , N -диметил(хлорметилен)аммония; [ClHC=N + (CH 3 ) 2 ]Cl − ) является высокохемоселективным агентом для восстановления карбоновой кислоты. Он селективно активирует карбоновую кислоту, давая соль карбоксиметиленаммония, которую можно восстановить мягким восстановителем, таким как трис( трет -бутокси)алюмогидрид лития, с получением альдегида в однореакторной процедуре. Известно, что эта процедура допускает реактивные карбонильные функциональные группы, такие как кетон, а также умеренно реактивные сложноэфирные, олефиновые, нитрильные и галогенидные фрагменты. [10]
Гидроксильная группа карбоновых кислот может быть заменена атомом хлора с использованием тионилхлорида для получения ацилхлоридов . В природе карбоновые кислоты преобразуются в тиоэфиры . Тионилхлорид может быть использован для преобразования карбоновых кислот в соответствующие им ацилхлориды. Сначала карбоновая кислота 1 атакует тионилхлорид, и хлорид-ион уходит. Полученный оксониевый ион 2 активируется в отношении нуклеофильной атаки и имеет хорошую уходящую группу, что отличает его от обычной карбоновой кислоты. На следующем этапе 2 подвергается атаке хлорид-ионом с образованием тетраэдрического промежуточного соединения 3 , хлорсульфита. Тетраэдрическое промежуточное соединение разрушается с потерей диоксида серы и хлорид-иона, давая протонированный ацилхлорид 4. Хлорид-ион может удалить протон из карбонильной группы, давая ацилхлорид 5 с потерей HCl .
Хлорид фосфора(III) (PCl 3 ) и хлорид фосфора(V) (PCl 5 ) также преобразуют карбоновые кислоты в хлорангидриды по схожему механизму. Один эквивалент PCl 3 может реагировать с тремя эквивалентами кислоты, производя один эквивалент H 3 PO 3 , или фосфорной кислоты , в дополнение к желаемому хлорангидриду. PCl 5 реагирует с карбоновыми кислотами в соотношении 1:1 и производит оксихлорид фосфора(V) (POCl 3 ) и хлористый водород (HCl) в качестве побочных продуктов.
Карбоновые кислоты реагируют с реактивами Гриньяра и литийорганическими соединениями с образованием кетонов. Первый эквивалент нуклеофила действует как основание и депротонирует кислоту. Второй эквивалент будет атаковать карбонильную группу, создавая геминальный алкоксидный дианион, который протонируется при обработке, давая гидрат кетона. Поскольку большинство гидратов кетонов нестабильны относительно соответствующих им кетонов, равновесие между ними сильно смещено в пользу кетона. Например, константа равновесия для образования гидрата ацетона из ацетона составляет всего 0,002. Карбоксильная группа является наиболее кислой в органических соединениях. [11]
Карбоксильный радикал , •COOH, существует лишь недолго. [12] Константа кислотной диссоциации •COOH была измерена с помощью спектроскопии электронного парамагнитного резонанса . [13] Карбоксильная группа имеет тенденцию к димеризации с образованием щавелевой кислоты .