Диоксид кремния , также известный как диоксид кремния , представляет собой оксид кремния с химической формулой SiO 2 , обычно встречающийся в природе в виде кварца . [5] [6] Во многих частях мира кремнезем является основным компонентом песка . Кремнезема много, поскольку он состоит из нескольких минералов и синтетических продуктов. Все формы белые или бесцветные, хотя нечистые образцы могут быть окрашены.
Диоксид кремния является основным компонентом стекла .

В большинстве диоксидов кремния атом кремния имеет тетраэдрическую координацию с четырьмя атомами кислорода, окружающими центральный атом Si (см. Трехмерную элементарную ячейку). Таким образом, SiO 2 образует трехмерные сетчатые твердые тела, в которых каждый атом кремния ковалентно связан тетраэдрическим образом с 4 атомами кислорода. [8] [9] Напротив, CO 2 представляет собой линейную молекулу. Резко различная структура диоксидов углерода и кремния является проявлением правила двойной связи . [10]
На основании кристаллических структурных различий диоксид кремния можно разделить на две категории: кристаллический и некристаллический (аморфный). В кристаллической форме это вещество встречается в природе в виде кварца, тридимита , кристобалита , стишовита и коэсита . С другой стороны, аморфный кремнезем можно найти в природе в виде опала , инфузории и диатомита . Кварцевое стекло является формой промежуточного состояния между этой структурой. [11]
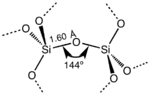
Все эти различные кристаллические формы всегда имеют одинаковую локальную структуру вокруг Si и O. В α-кварце длина связи Si–O составляет 161 пм, тогда как в α-тридимите она находится в диапазоне 154–171 пм. Угол Si–O–Si также варьируется от небольшого значения 140° в α-тридимите до 180° в β-тридимите. В α-кварце угол Si–O–Si равен 144°. [12]
Альфа-кварц — наиболее стабильная форма твердого SiO 2 при комнатной температуре. Высокотемпературные минералы кристобалит и тридимит имеют меньшую плотность и показатель преломления, чем кварц. Превращение альфа-кварца в бета-кварц происходит резко при 573 °С. Поскольку превращение сопровождается значительным изменением объема, оно легко может вызвать разрушение керамики или горных пород, проходящих через этот температурный предел. [13] Однако минералы высокого давления, зейфертит , стишовит и коэсит, имеют более высокие плотности и показатели преломления, чем кварц. [14] Стишовит имеет рутилоподобную структуру, в которой кремний имеет 6-координатную структуру. Плотность стишовита составляет 4,287 г/см 3 , что сопоставимо с плотностью α-кварца, самой плотной из форм низкого давления, имеющей плотность 2,648 г/см 3 . [15] Разницу в плотности можно объяснить увеличением координации, поскольку шесть самых коротких длин связей Si–O в стишовите (четыре связи Si–O по 176 пм и две другие по 181 пм) больше, чем у Si–O. длина связи (161 пм) в α-кварце. [16] Изменение координации увеличивает ионность связи Si–O. [17]
Кремнезем фожазита , еще одна полиморфная модификация, получают путем деалюминирования ультрастабильного цеолита Y с низким содержанием натрия с помощью комбинированной кислотной и термической обработки. Полученный продукт содержит более 99% кремнезема, имеет высокую кристалличность и удельную поверхность (более 800 м 2 /г). Фожазит-кремнезем обладает очень высокой термической и кислотной стабильностью. Например, он сохраняет высокую степень дальнего молекулярного порядка или кристалличности даже после кипячения в концентрированной соляной кислоте . [18]
Расплавленный кремнезем демонстрирует несколько своеобразных физических характеристик, аналогичных тем, которые наблюдаются в жидкой воде : отрицательное температурное расширение, максимум плотности при температуре ~ 5000 ° C и минимум теплоемкости. [19] Его плотность снижается с 2,08 г/см 3 при 1950 °С до 2,03 г/см 3 при 2200 °С. [20]
Молекулярный SiO 2 имеет линейную структуру, как и CO 2 . Он был произведен путем объединения монооксида кремния (SiO) с кислородом в матрице аргона . Димерный диоксид кремния (SiO 2 ) 2 был получен путем взаимодействия O 2 с выделенным в матрице димерным монооксидом кремния (Si 2 O 2 ). В димерном диоксиде кремния между атомами кремния имеются два атома кислорода, образующие мостик с углом Si-O-Si 94° и длиной связи 164,6 пм, а длина концевой связи Si-O составляет 150,2 пм. Длина связи Si–O составляет 148,3 пм, что сопоставимо с длиной 161 пм в α-кварце. Энергия связи оценивается в 621,7 кДж/моль. [21]
SiO 2 чаще всего встречается в природе в виде кварца , составляющего более 10% массы земной коры. [22] Кварц – единственная полиморфная модификация кремнезема, стабильная на поверхности Земли. Метастабильные проявления высокобарических форм коэсита и стишовита обнаружены вокруг ударных структур и связаны с эклогитами , образовавшимися в ходе метаморфизма сверхвысокого давления . Из богатых кремнеземом вулканических пород известны высокотемпературные формы тридимита и кристобалита . Во многих частях мира кремнезем является основным компонентом песка . [23]
Несмотря на то, что кремнезем плохо растворяется, он содержится во многих растениях, таких как рис . Растительные материалы с высоким содержанием кремнезема в фитолитах , по-видимому, имеют важное значение для пасущихся животных, от жующих насекомых до копытных . Кремнезем ускоряет изнашивание зубов, а высокий уровень кремнезема в растениях, которые часто поедают травоядные, возможно, стал защитным механизмом от хищников. [24] [25]
Кремнезем также является основным компонентом золы рисовой шелухи , которая используется, например, для фильтрации и в качестве дополнительного вяжущего материала (СКМ) при производстве цемента и бетона . [26]
На протяжении более 1000 миллионов лет окремнение клеток и внутри клеток было обычным явлением в биологическом мире. В современном мире встречается у бактерий, протистов, растений и животных (беспозвоночных и позвоночных).
Яркие примеры включают:
Кристаллические минералы, образующиеся в физиологической среде, часто демонстрируют исключительные физические свойства (например, прочность, твердость, вязкость разрушения) и имеют тенденцию образовывать иерархические структуры, которые демонстрируют микроструктурный порядок в широком диапазоне масштабов. Кристаллизация минералов происходит в среде, недонасыщенной кремнием, в условиях нейтрального рН и низкой температуры (0–40 °С).
Около 95% коммерческого использования диоксида кремния (песка) приходится на строительную отрасль, например, для производства бетона ( портландцементный бетон ). [22]
Определенные месторождения кварцевого песка с желаемым размером и формой частиц и желаемым содержанием глины и других минералов были важны для литья металлических изделий в песчаные формы . [27] Высокая температура плавления кремнезема позволяет использовать его в таких областях, как литье чугуна; в современном литье из песка иногда используются другие минералы по другим причинам.
Кристаллический кремнезем используется при гидроразрыве пластов, содержащих плотную нефть и сланцевый газ . [28]
Кремнезем является основным ингредиентом в производстве большей части стекла . Поскольку другие минералы плавятся с кремнеземом, принцип понижения температуры замерзания снижает температуру плавления смеси и увеличивает текучесть. Температура стеклования чистого SiO 2 составляет около 1475 К. [29] При быстром охлаждении расплавленного диоксида кремния SiO 2 он не кристаллизуется, а затвердевает в виде стекла. По этой причине в большинстве керамических глазурей в качестве основного ингредиента используется кремнезем.
Структурная геометрия кремния и кислорода в стекле аналогична таковой в кварце и большинстве других кристаллических форм кремния и кислорода, где кремний окружен правильными тетраэдрами кислородных центров. Разница между стеклянной и кристаллической формами возникает из-за связности тетраэдрических единиц: хотя в стекловидной сетке нет дальнодействующей периодичности, упорядоченность сохраняется на масштабах длины, значительно превышающих длину связи SiO. Одним из примеров такого упорядочения является предпочтение образовывать кольца из 6-тетраэдров. [30]
Большинство оптических волокон для телекоммуникаций также изготавливаются из кремнезема. Это основное сырье для многих керамических изделий, таких как фаянс , керамика и фарфор .
Диоксид кремния используется для производства элементарного кремния . Процесс включает карботермическое восстановление в электродуговой печи : [31]
Колючий кремнезем , также известный как пирогенный кремнезем, получают путем сжигания SiCl 4 в богатом кислородом водородном пламени с образованием «дыма» SiO 2 . [15]
Его также можно получить путем испарения кварцевого песка в электрической дуге при температуре 3000 °C. Оба процесса приводят к образованию микроскопических капель аморфного кремнезема, сплавленных в разветвленные, цепочечные, трехмерные вторичные частицы, которые затем агломерируются в третичные частицы, белый порошок с чрезвычайно низкой объемной плотностью (0,03-0,15 г/см 3 ) и, следовательно, с большой площадью поверхности. [32] Частицы действуют как тиксотропный загуститель или агент, препятствующий слеживанию, и могут быть обработаны, чтобы сделать их гидрофильными или гидрофобными для применения с водой или органическими жидкостями.

Дым кремнезема представляет собой ультратонкий порошок, собираемый как побочный продукт производства кремния и сплавов ферросилиция . Состоит из аморфных (некристаллических) сферических частиц со средним диаметром частиц 150 нм, без разветвлений пирогенного продукта. Основное применение — в качестве пуццоланового материала для изготовления бетона с высокими эксплуатационными характеристиками. Наночастицы дымящего кремнезема можно успешно использовать в качестве средства, замедляющего старение, в асфальтовых вяжущих. [33]
Кремнезем, коллоидный, осажденный или пирогенный, является распространенной добавкой в производстве продуктов питания. Он используется главным образом в качестве антислеживающего агента или агента , препятствующего слеживанию, в порошкообразных пищевых продуктах, таких как специи и немолочные сливки для кофе, или в порошках для изготовления фармацевтических таблеток. [32] Он может адсорбировать воду в гигроскопических применениях. Коллоидный диоксид кремния используется в качестве осветлителя для вина, пива и соков, его номер E551 . [22]
В косметике кремнезем полезен благодаря своим светорассеивающим свойствам [34] и естественной впитывающей способности. [35]
Кизельгур , добываемый продукт, веками использовался в продуктах питания и косметике. Он состоит из кремнеземных панцирей микроскопических диатомей ; в менее обработанной форме он продавался как «зубной порошок». [ нужна цитация ] Произведенный или добытый гидратированный диоксид кремния используется в качестве твердого абразива в зубной пасте .
Диоксид кремния широко используется в полупроводниковой технике.
Поскольку диоксид кремния является естественным оксидом кремния, он используется более широко по сравнению с другими полупроводниками, такими как арсенид галлия или фосфид индия .
Диоксид кремния можно выращивать на поверхности кремниевого полупроводника . [36] Слои оксида кремния могут защитить поверхности кремния во время диффузионных процессов и могут использоваться для диффузионной маскировки. [37] [38]
Пассивация поверхности — это процесс, при котором поверхность полупроводника становится инертной и не меняет свойств полупроводника в результате взаимодействия с воздухом или другими материалами, контактирующими с поверхностью или краем кристалла. [39] [40] Формирование термически выращенного слоя диоксида кремния значительно снижает концентрацию электронных состояний на поверхности кремния . [40] Пленки SiO 2 сохраняют электрические характеристики p–n-переходов и предотвращают ухудшение этих электрических характеристик под воздействием газовой окружающей среды. [38] Слои оксида кремния можно использовать для электрической стабилизации кремниевых поверхностей. [37] Процесс пассивации поверхности является важным методом изготовления полупроводниковых устройств , который включает покрытие кремниевой пластины изолирующим слоем оксида кремния, чтобы электричество могло надежно проникать в проводящий кремний ниже. Выращивание слоя диоксида кремния поверх кремниевой пластины позволяет преодолеть поверхностные состояния , которые в противном случае не позволяют электричеству достичь полупроводникового слоя. [39] [41]
Процесс пассивации поверхности кремния путем термического окисления (диоксидом кремния) имеет решающее значение для полупроводниковой промышленности . Он обычно используется для производства полевых транзисторов металл-оксид-полупроводник (MOSFET) и кремниевых интегральных микросхем (планарный процесс ). [39] [41]
В качестве пеногасителя используется гидрофобный диоксид кремния .
В качестве огнеупорного материала он полезен в форме волокна в качестве высокотемпературной термозащитной ткани. [ нужна цитата ]
Кремнезем используется при экстракции ДНК и РНК из-за его способности связываться с нуклеиновыми кислотами в присутствии хаотропов . [42]
Аэрогель кремнезема использовался в космическом корабле Stardust для сбора внеземных частиц. [43]
Чистый кремнезем (диоксид кремния) при охлаждении в виде плавленого кварца в стекло без истинной температуры плавления можно использовать в качестве стекловолокна для стекловолокна.
Диоксид кремния исследовался для применения в сельском хозяйстве в качестве потенциального инсектицида . [44] [45]
Диоксид кремния в основном получают путем добычи полезных ископаемых, включая добычу песка и очистку кварца . Кварц пригоден для многих целей, в то время как для получения более чистого или более подходящего (например, более реакционноспособного или мелкозернистого) продукта требуется химическая обработка. [ нужна цитата ]
Осажденный кремнезем или аморфный кремнезем получают подкислением растворов силиката натрия . Желатиновый осадок или силикагель сначала промывают, а затем обезвоживают с получением бесцветного микропористого кремнезема. [15] Идеализированное уравнение, включающее трисиликат и серную кислоту :
Таким способом производилось около одного миллиарда килограммов кремнезема в год (1999 г.), в основном для использования в полимерных композитах – шинах и подошвах обуви. [22]
Тонкие пленки кремнезема самопроизвольно растут на кремниевых пластинах в результате термического окисления , образуя очень мелкий слой так называемого естественного оксида толщиной около 1 нм или 10 Å . [46] Для выращивания хорошо контролируемых слоев диоксида кремния на кремнии используются более высокие температуры и альтернативные среды, например, при температурах от 600 до 1200 °C, с использованием так называемого сухого окисления O 2 .
или мокрое окисление H 2 O. [47] [48]
Слой собственного оксида полезен в микроэлектронике , где он действует как электрический изолятор с высокой химической стабильностью. Он может защищать кремний, накапливать заряд, блокировать ток и даже действовать как контролируемый путь для ограничения тока. [49]
Многие пути получения диоксида кремния начинаются с кремнийорганических соединений, например, HMDSO, [50] TEOS. Синтез кремнезема проиллюстрирован ниже с использованием тетраэтилортосиликата (ТЭОС). [51] Простое нагревание ТЭОС при температуре 680–730 °C приводит к образованию оксида:
Аналогично TEOS сгорает при температуре около 400 °C:
ТЭОС подвергается гидролизу посредством так называемого золь-гель процесса . Катализаторы влияют на ход реакции и природу продукта, но идеализированное уравнение таково: [52]
Будучи очень стабильным, диоксид кремния получается многими способами. Концептуально простой, но не имеющий практической ценности, сжигание силана дает диоксид кремния. Эта реакция аналогична горению метана:
Однако ранее применялось химическое осаждение диоксида кремния из паровой фазы на поверхность кристаллов из силана с использованием азота в качестве газа-носителя при температуре 200–500 °С. [53]
Диоксид кремния — относительно инертный материал (отсюда его широкое распространение в качестве минерала). Кремнезем часто используется в качестве инертных контейнеров для химических реакций. При высоких температурах он превращается в кремний путем восстановления углеродом.
Фтор реагирует с диоксидом кремния с образованием SiF 4 и O 2 , тогда как другие галогенные газы (Cl 2 , Br 2 , I 2 ) нереакционноспособны. [15]
Большинство форм диоксида кремния подвергаются воздействию («травлению») плавиковой кислоты (HF) с образованием гексафторкремниевой кислоты : [12]
Стишовит в сколько-нибудь существенной степени не реагирует на HF. [54] HF используется для удаления или формирования рисунка диоксида кремния в полупроводниковой промышленности.
Диоксид кремния действует как кислота Люкса-Флуда , способная при определенных условиях вступать в реакцию с основаниями. Поскольку негидратированный кремнезем не содержит водорода, он не может напрямую действовать как кислота Бренстеда-Лоури . В то время как диоксид кремния плохо растворим в воде при низком или нейтральном pH (обычно от 2 × 10 -4 М для кварца до 10 -3 М для скрытокристаллического халцедона ), сильные основания реагируют со стеклом и легко растворяют его. Поэтому сильные основания необходимо хранить в пластиковых флаконах во избежание заклинивания крышки флакона, сохранения целостности ресивера и во избежание нежелательного загрязнения силикат-анионами. [55]
Диоксид кремния растворяется в горячей концентрированной щелочи или плавленном гидроксиде, как описано в этом идеализированном уравнении: [15]
Диоксид кремния нейтрализует оксиды основных металлов (например , оксид натрия , оксид калия , оксид свинца (II) , оксид цинка или смеси оксидов, образуя силикаты и стекла по мере последовательного разрыва связей Si-O-Si в кремнеземе). [12] Например, реакция оксида натрия и SiO 2 может привести к образованию ортосиликата натрия , силиката натрия и стекол, в зависимости от пропорций реагентов: [15]
Примеры таких стекол имеют коммерческое значение, например, натриево-известковое стекло , боросиликатное стекло , свинцовое стекло . В этих стеклах кремнезем называют сеткообразователем или решетообразователем. [12] Реакция также используется в доменных печах для удаления примесей песка из руды путем нейтрализации оксидом кальция с образованием силикатно-кальциевого шлака .

Диоксид кремния реагирует при нагретой флегме в атмосфере динитрога с этиленгликолем и основанием щелочного металла с образованием высокореактивных пятикоординированных силикатов, которые обеспечивают доступ к широкому спектру новых соединений кремния. [56] Силикаты по существу нерастворимы во всех полярных растворителях, кроме метанола .
Диоксид кремния реагирует с элементарным кремнием при высоких температурах с образованием SiO: [12]
Растворимость диоксида кремния в воде сильно зависит от его кристаллической формы и у кремнезема [ необходимо уточнение ] в три-четыре раза выше , чем у кварца; В зависимости от температуры она достигает максимума около 340 ° C (644 ° F). [57] Это свойство используется для выращивания монокристаллов кварца в гидротермальном процессе, при котором природный кварц растворяется в перегретой воде в сосуде под давлением, который более прохладен вверху. Кристаллы массой 0,5–1 кг можно вырастить за 1–2 месяца. [12] Эти кристаллы являются источником очень чистого кварца для использования в электронных приложениях. [15] Выше критической температуры воды 647,096 К (373,946 °C; 705,103 °F) и давления 22,064 мегапаскаля (3200,1 фунтов на квадратный дюйм) или выше вода представляет собой сверхкритическую жидкость , и ее растворимость снова выше, чем при более низких температурах. [58]

Кремнезем, принимаемый перорально, практически нетоксичен: его LD 50 составляет 5000 мг/кг (5 г/кг). [22] Исследование 2008 года, в котором участвовали испытуемые в течение 15 лет, показало, что более высокие уровни кремнезема в воде, по-видимому, снижают риск деменции . Увеличение содержания кремнезема в питьевой воде на 10 мг/день было связано со снижением риска деменции на 11%. [59]
Вдыхание мелкодисперсной пыли кристаллического кремнезема может привести к силикозу , бронхиту или раку легких , поскольку пыль задерживается в легких и постоянно раздражает ткани, снижая объем легких. [60] Когда мелкие частицы кремнезема вдыхаются в достаточно больших количествах (например, в результате профессионального воздействия), это увеличивает риск системных аутоиммунных заболеваний , таких как волчанка [61] и ревматоидный артрит, по сравнению с ожидаемыми показателями среди населения в целом. [45]
Кремнезем представляет собой профессиональную опасность для людей, занимающихся пескоструйной обработкой или работающих с продуктами, содержащими порошкообразный кристаллический кремнезем. Аморфный кремнезем, такой как коллоидный кремнезем, в некоторых случаях может вызывать необратимое повреждение легких, но не связан с развитием силикоза. Дети, астматики любого возраста, аллергики и пожилые люди (у всех из которых снижен объем легких ) могут пострадать за меньшее время. [62]
Кристаллический кремнезем представляет собой профессиональную опасность для тех, кто работает с каменными столешницами , поскольку в процессе резки и установки столешниц образуется большое количество переносимого по воздуху кремнезема. [63] Кристаллический кремнезем, используемый при гидроразрыве пласта, представляет опасность для здоровья рабочих. [28]
В организме частицы кристаллического кремнезема не растворяются в течение клинически значимого периода времени. Кристаллы кремнезема внутри легких могут активировать воспалительную сому NLRP3 внутри макрофагов и дендритных клеток и тем самым приводить к выработке интерлейкина , сильно провоспалительного цитокина в иммунной системе. [64] [65] [66]
В правилах, ограничивающих воздействие кремнезема «в связи с опасностью силикоза», указывается, что они касаются только кремнезема, который является как кристаллическим, так и пылящим. [67] [68] [69] [70] [71] [72]
В 2013 году Управление по охране труда США снизило предельно допустимый уровень воздействия до 50 мкг /м 3 воздуха. До 2013 года допускалось 100 мкг/м 3 , а у строителей – даже 250 мкг/м 3 . [28] В 2013 году OSHA также потребовало «зеленого заканчивания» скважин с гидроразрывом, чтобы уменьшить воздействие кристаллического кремнезема, а также ограничить предел воздействия. [28]
SiO 2 в большей степени, чем любой другой материал, существует во многих кристаллических формах. Эти формы называются полиморфами .
Вдыхание мелкодисперсного кристаллического кремнезема может привести к тяжелому воспалению легочной ткани , силикозу , бронхиту , раку легких и системным аутоиммунным заболеваниям , таким как волчанка и ревматоидный артрит . Вдыхание аморфного диоксида кремния в высоких дозах приводит к непостоянному кратковременному воспалению, при котором все последствия заживают. [88]
В этом расширенном списке перечислены синонимы диоксида кремния; все эти значения взяты из одного источника; значения в источнике были представлены с заглавной буквы. [89]
Эти мягкофокусные пигменты, в основном состоящие из полимеров, слюд и тальков, покрытых шероховатыми или сферическими частицами небольшого диаметра, такими как диоксид кремния или диоксид титана, используются для оптического уменьшения морщин. Эти эффекты достигаются за счет оптимизации очертаний морщин и уменьшения разницы яркости из-за диффузного отражения.
Кремнезем представляет собой многопористый ингредиент, который впитывает масло и кожный жир.