Кобальт — химический элемент ; он имеет символ Co и атомный номер 27. Как и никель , кобальт встречается в земной коре только в химически связанной форме, за исключением небольших месторождений, обнаруженных в сплавах природного метеорного железа . Свободный элемент , получаемый восстановительной плавкой , представляет собой твердый, блестящий, серебристый металл .
Синие пигменты на основе кобальта ( синий кобальт ) использовались с древности для изготовления ювелирных изделий и красок, а также для придания стеклу характерного синего оттенка. Долгое время считалось, что этот цвет обусловлен металлом висмутом . Шахтеры издавна использовали название « кобольдская руда» ( по -немецки «руда гоблинов ») для некоторых минералов , производящих синий пигмент . Они были названы так потому, что были бедны известными металлами и при плавке выделяли ядовитые пары, содержащие мышьяк . [7] В 1735 году было обнаружено, что такие руды можно восстановить до нового металла (первого открытого с древних времен), который в конечном итоге был назван в честь кобольда .
Сегодня некоторая часть кобальта производится специально из одной из ряда руд с металлическим блеском, таких как кобальтит (CoAsS). Этот элемент чаще всего производится как побочный продукт добычи меди и никеля. Медный пояс в Демократической Республике Конго (ДРК) и Замбии обеспечивает большую часть мирового производства кобальта. Мировое производство в 2016 году составило 116 000 тонн (114 000 длинных тонн; 128 000 коротких тонн) (по данным Natural Resources Canada ), причем на одну только ДРК пришлось более 50%. [8]
Кобальт в основном используется в литий-ионных аккумуляторах , а также в производстве магнитных , износостойких и высокопрочных сплавов . Соединения силиката кобальта и алюмината кобальта(II) (CoAl 2 O 4 , синий кобальт) придают характерный глубокий синий цвет стеклу , керамике , чернилам , краскам и лакам . В природе кобальт встречается только в виде одного стабильного изотопа — кобальта-59. Кобальт-60 — коммерчески важный радиоизотоп, используемый в качестве радиоактивного индикатора и для производства гамма-лучей высокой энергии . Кобальт также используется в нефтяной промышленности в качестве катализатора при переработке сырой нефти. Это делается для того, чтобы очистить его от серы, которая при сжигании сильно загрязняет окружающую среду и вызывает кислотные дожди. [9]
Кобальт является активным центром группы коферментов , называемых кобаламинами . Витамин B12 , самый известный представитель этого типа, является незаменимым витамином для всех животных. Кобальт в неорганической форме также является микроэлементом для бактерий , водорослей и грибов .

Кобальт — ферромагнитный металл с удельным весом 8,9. Температура Кюри составляет 1115 °C (2039 °F) [10] , а магнитный момент составляет 1,6–1,7 магнетона Бора на атом . [11] Относительная проницаемость кобальта составляет две трети от относительной проницаемости железа . [12] Металлический кобальт встречается в виде двух кристаллографических структур : ГПУ и ГЦК . Идеальная температура перехода между структурами ГПУ и ГЦК составляет 450 ° C (842 ° F), но на практике разница в энергии между ними настолько мала, что случайное срастание этих двух структур является обычным явлением. [13] [14] [15]
Кобальт – слабовосстанавливающий металл, защищенный от окисления пассивирующей оксидной пленкой . Он подвергается воздействию галогенов и серы . При нагревании в кислороде образуется Co 3 O 4 , который теряет кислород при 900 °C (1650 °F) с образованием монооксида CoO. [16] Металл реагирует с фтором (F 2 ) при 520 К с образованием CoF 3 ; с хлором (Cl 2 ), бромом (Br 2 ) и йодом (I 2 ), образуя эквивалентные бинарные галогениды . Он не реагирует с газообразным водородом ( H 2 ) или газообразным азотом ( N 2 ) даже при нагревании, но реагирует с бором , углеродом , фосфором , мышьяком и серой. [17] При обычных температурах медленно реагирует с минеральными кислотами и очень медленно с влажным, но не сухим воздухом. [ нужна ссылка ] [18]
Обычные степени окисления кобальта включают +2 и +3, хотя также известны соединения со степенями окисления от -3 до +5 . Обычная степень окисления простых соединений +2 (кобальт (II)). Эти соли образуют аквакомплекс металла розового цвета [Co(H
2О)
6]2+
в воде. Добавление хлорида дает ярко-синий цвет [CoCl
4]2-
. [4] При испытании пламенем шариков буры кобальт имеет темно-синий цвет как в окислительном, так и в восстановительном пламени. [19]
Известно несколько оксидов кобальта. Зеленый оксид кобальта(II) (CoO) имеет структуру каменной соли . Он легко окисляется водой и кислородом до коричневого гидроксида кобальта(III) (Co(OH) 3 ). При температуре 600–700 °С СоО окисляется до синего оксида кобальта(II,III) (Со 3 О 4 ), имеющего структуру шпинели . [4] Также известен черный оксид кобальта(III) (Co 2 O 3 ). [20] Оксиды кобальта являются антиферромагнитными при низкой температуре : CoO ( температура Нееля 291 К) и Co 3 O 4 (температура Нееля: 40 К), что аналогично магнетиту (Fe 3 O 4 ), со смесью +2 и +3 степени окисления. [21]
Основные халькогениды кобальта включают черные сульфиды кобальта (II) , CoS 2 , который имеет пиритоподобную структуру, и сульфид кобальта (III) (Co 2 S 3 ). [ нужна цитата ]
-chloride-hexahydrate-sample.jpg/440px-Cobalt(II)-chloride-hexahydrate-sample.jpg)
Известны четыре дигалогенида кобальта(II): фторид кобальта(II) (CoF 2 , розовый), хлорид кобальта(II) (CoCl 2 , синий), бромид кобальта(II) (CoBr 2 , зелёный), кобальт(II) йодид (CoI 2 , сине-черный). Эти галогениды существуют в безводной и гидратированной формах. В то время как безводный дихлорид имеет синий цвет, гидрат — красный. [22]
Восстановительный потенциал реакции Co3+
+ е − → Со2+
составляет +1,92 В, а для хлора в хлорид - +1,36 В. Следовательно, хлорид кобальта(III) самопроизвольно восстанавливается до хлорида кобальта(II) и хлора. Поскольку потенциал восстановления фтора до фторида очень высок, +2,87 В, фторид кобальта (III) является одним из немногих простых стабильных соединений кобальта (III). Фторид кобальта(III), который используется в некоторых реакциях фторирования, бурно реагирует с водой. [16]
Как и все металлы, молекулярные соединения и многоатомные ионы кобальта классифицируются как координационные комплексы , то есть молекулы или ионы, содержащие кобальт, связанный с одним или несколькими лигандами . Это могут быть комбинации потенциально бесконечного множества молекул и ионов, таких как:
Эти присоединенные группы влияют на стабильность состояний окисления атомов кобальта в соответствии с общими принципами электроотрицательности и твердости -мягкости . Например, комплексы Co 3+ обычно содержат амминные лиганды. Поскольку фосфор мягче азота, фосфиновые лиганды, как правило, содержат более мягкие Co 2+ и Co + , примером является хлорид трис(трифенилфосфин)кобальта(I) ( P(C
6ЧАС
5)
3)
3КоКл ). Более электроотрицательные (и более твердые) оксид и фторид могут стабилизировать производные Co 4+ и Co 5+ , например гексафторкобальтат(IV) цезия (Cs 2 CoF 6 ) и перкобальтат калия (K 3 CoO 4 ). [16]
Альфред Вернер , лауреат Нобелевской премии в области координационной химии , работал с соединениями эмпирической формулы [Co(NH
3)
6]3+
. Одним из определенных изомеров был хлорид гексаммина кобальта(III) . Этот координационный комплекс, типичный комплекс типа Вернера, состоит из центрального атома кобальта, координированного шестью аминоортогональными лигандами и тремя хлоридными противоанионами. Использование хелатирующих этилендиаминовых лигандов вместо аммиака дает трис(этилендиамин)кобальт(III) ( [Co(en)
3]3+
), который был одним из первых координационных комплексов , разделенных на оптические изомеры . Комплекс существует в право- и левосторонней формах «трехлопастного винта». Этот комплекс был впервые выделен Вернером в виде игольчатых кристаллов желтого золота. [26] [27]
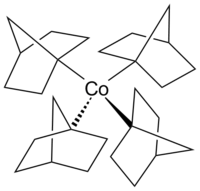
Кобальтоцен является структурным аналогом ферроцена , в котором вместо железа находится кобальт. Кобальтоцен гораздо более чувствителен к окислению, чем ферроцен. [28] Карбонил кобальта ( Co 2 (CO) 8 ) является катализатором реакций карбонилирования и гидросилилирования . [29] Витамин B 12 (см. ниже ) представляет собой металлоорганическое соединение, встречающееся в природе, и единственный витамин , содержащий атом металла. [30] Примером комплекса алкилкобальта в необычной степени окисления кобальта +4 является гомолептический комплекс тетракис(1-норборнил)кобальт(IV) (Co(1-norb) 4 ), комплекс переходный металл-алкил, который отличается устойчивостью к удалению β-водорода [31] в соответствии с правилом Бредта . Комплексы кобальта(III) и кобальта(V) [Li(THF)
4]+
[Co(1-норб)
4]−
и [Co(1-norb)
4]+
[БФ
4]−
также известны. [32]
59 Co — единственный стабильный изотоп кобальта и единственный изотоп , который существует в природе на Земле. Охарактеризовано двадцать два радиоизотопа : наиболее стабильный, 60 Co , имеет период полураспада 5,2714 года; Период полураспада 57 Co составляет 271,8 дня; Период полураспада 56 Co составляет 77,27 дней; и 58 Co имеет период полураспада 70,86 дней. Все остальные радиоактивные изотопы кобальта имеют период полураспада менее 18 часов и в большинстве случаев менее 1 секунды. У этого элемента также есть 4 метасостояния , период полураспада каждого из которых короче 15 минут. [33]
Атомный вес изотопов кобальта варьируется от 50 u ( 50 Co) до 73 u ( 73 Co). Основным способом распада изотопов с атомной массой меньше, чем у единственного стабильного изотопа 59 Co, является захват электрона , а основным способом распада изотопов с атомной массой более 59 атомных единиц массы является бета-распад . Первичными продуктами распада ниже 59 Co являются изотопы элемента 26 ( железа ); выше этого продуктами распада являются изотопы элемента 28 (никель). [33]

Соединения кобальта веками использовались для придания насыщенного синего цвета стеклу , глазури и керамике . Кобальт был обнаружен в египетской скульптуре, персидских украшениях третьего тысячелетия до нашей эры, в руинах Помпеи , разрушенной в 79 году нашей эры, а также в Китае, датируемом династиями Тан (618–907 годы нашей эры) и династией Мин (1368–1644 годы) . ОБЪЯВЛЕНИЕ). [34]
Кобальт использовался для окраски стекла с бронзового века . При раскопках затонувшего корабля Улубурун был найден слиток синего стекла, отлитый в 14 веке до нашей эры. [35] [36] Голубое стекло из Египта было окрашено медью, железом или кобальтом. Самое старое стекло кобальтового цвета относится к восемнадцатой династии Египта (1550–1292 гг. До н.э.). Источник кобальта, который использовали египтяне, неизвестен. [37] [38]
Слово «кобальт» происходит от немецкого «кобальт» , от слова « кобольд », означающего «гоблин», суеверного термина, используемого горняками для обозначения кобальтовой руды . Первые попытки переплавить эти руды на медь или серебро не увенчались успехом, вместо этого был получен просто порошок (оксид кобальта (II)). Поскольку первичные кобальтовые руды всегда содержат мышьяк, плавка руды окисляла мышьяк в высокотоксичный и летучий оксид мышьяка , что добавляло этой руде дурной славы. [39] Парацельс , Георгий Агрикола и Василий Валентин называли такие силикаты «кобальтом». [40]
Шведскому химику Георгу Брандту (1694–1768) приписывают открытие кобальта c. 1735 г. , что показывает, что это ранее неизвестный элемент, отличный от висмута и других традиционных металлов. Брандт назвал его новым «полуметаллом». [41] [42] Он показал, что соединения металлического кобальта были источником синего цвета стекла, который ранее приписывался висмуту, обнаруженному с кобальтом. Кобальт стал первым металлом, открытым с доисторического периода. Все остальные известные металлы (железо, медь, серебро, золото, цинк, ртуть, олово, свинец и висмут) не имели зарегистрированных первооткрывателей. [43]
В XIX веке значительная часть мирового производства синего кобальта (пигмента, изготовленного из соединений кобальта и оксида алюминия) и смальты ( порошкового кобальтового стекла для использования в качестве пигмента в керамике и живописи) осуществлялась на норвежском Blaafarveværket . [44] [45] Первые шахты по производству смальты в 16 веке были расположены в Норвегии, Швеции, Саксонии и Венгрии. С открытием кобальтовой руды в Новой Каледонии в 1864 году добыча кобальта в Европе сократилась. С открытием рудных месторождений в Онтарио , Канада, в 1904 году и открытием еще более крупных месторождений в провинции Катанга в Конго в 1914 году, горнодобывающие операции снова изменились. [39] Когда в 1978 году начался конфликт в Шабе , медные рудники провинции Катанга практически прекратили добычу. [46] [47] Влияние этого конфликта на мировую кобальтовую экономику оказалось меньшим, чем ожидалось: кобальт — редкий металл, пигмент высокотоксичен, а промышленность уже разработала эффективные способы переработки кобальтовых материалов. В некоторых случаях промышленность смогла перейти на безкобальтовые альтернативы. [46] [47]
В 1938 году Джон Ливингуд и Гленн Т. Сиборг открыли радиоизотоп кобальт-60 . [48] Этот изотоп широко использовался в Колумбийском университете в 1950-х годах для установления нарушения четности при радиоактивном бета-распаде . [49] [50]
После Второй мировой войны США хотели гарантировать поставки кобальтовой руды для военных целей (как это делали немцы) и проводили разведку кобальта на территории США. Кобальт высокой чистоты пользовался большим спросом из-за его использования в реактивных двигателях и газовых турбинах. [51] Достаточный запас руды был найден в Айдахо недалеко от каньона Блэкберд . Компания Calera Mining начала добычу на этом месте. [52]
В 21 веке спрос на кобальт еще больше увеличился, поскольку он является важным компонентом материалов, используемых в перезаряжаемых батареях, суперсплавах и катализаторах. [51] Утверждалось, что кобальт будет одним из главных объектов геополитической конкуренции в мире, работающем на возобновляемых источниках энергии и зависящем от батарей, но эта точка зрения также подвергалась критике за недооценку силы экономических стимулов для расширения производства. [53]
Стабильная форма кобальта производится в сверхновых посредством r-процесса . [54] Он составляет 0,0029% земной коры . Свободный кобальт ( самородный металл ) не встречается на поверхности Земли из-за его склонности вступать в реакцию с кислородом атмосферы. Небольшие количества соединений кобальта обнаружены в большинстве горных пород, почв, растений и животных. [55] В океане кобальт обычно реагирует с хлором. За исключением недавно доставленного метеоритного железа, чистый кобальт в самородной металлической форме на Земле неизвестен.
В природе кобальт часто сочетается с никелем . Оба являются характерными компонентами метеоритного железа , хотя кобальта в железных метеоритах гораздо меньше, чем никеля. Как и никель, кобальт в сплавах метеоритного железа мог быть достаточно хорошо защищен от кислорода и влаги, чтобы оставаться свободным (но легированным) металлом. [56]
Кобальт в сложной форме встречается в минералах меди и никеля. Это основной металлический компонент, который соединяется с серой и мышьяком в сульфидных минералах кобальтита (CoAsS), сафлорита (CoAs 2 ), глаукодота ( (Co,Fe)AsS ) и скуттерудита (CoAs 3 ). [16] Минерал каттиерит подобен пириту и встречается вместе с ваэситом в медных месторождениях провинции Катанга . [57] Когда он достигает атмосферы, происходит выветривание ; сульфидные минералы окисляются и образуют розовый эритрит («кобальтовый блеск»: Co 3 (AsO 4 ) 2 ·8H 2 O ) и сферокобальтит (CoCO 3 ). [58] [59]
Кобальт также входит в состав табачного дыма . [60] Растение табака легко поглощает и накапливает в своих листьях тяжелые металлы, такие как кобальт, из окружающей почвы. Впоследствии они вдыхаются во время курения табака . [61]

Основными рудами кобальта являются кобальтит , эритрит , глаукодот и скуттерудит (см. выше), но большая часть кобальта получается за счет восстановления кобальтовых побочных продуктов добычи и выплавки никеля и меди . [63] [64]
Поскольку кобальт обычно производится как побочный продукт, предложение кобальта в значительной степени зависит от экономической целесообразности добычи меди и никеля на конкретном рынке. Прогнозируется, что в 2017 году спрос на кобальт вырастет на 6% [65].
Первичные месторождения кобальта встречаются редко, например, в гидротермальных месторождениях , связанных с ультраосновными породами , типичным примером которых является район Бу-Аззер в Марокко . В таких местах добываются исключительно кобальтовые руды, хотя и с более низкой концентрацией, и поэтому для извлечения кобальта требуется более глубокая переработка. [66] [67]
Существует несколько методов отделения кобальта от меди и никеля, в зависимости от концентрации кобальта и точного состава используемой руды. Одним из методов является пенная флотация , при которой поверхностно-активные вещества связываются с компонентами руды, что приводит к обогащению кобальтовых руд. Последующий обжиг превращает руду в сульфат кобальта , а медь и железо окисляются до оксида. При выщелачивании водой сульфат экстрагируется вместе с арсенатами . Остатки дополнительно выщелачивают серной кислотой , получая раствор медного купороса. Кобальт также можно выщелачивать из шлака медеплавильного производства. [68]
Продукты указанных процессов превращаются в оксид кобальта (Co 3 O 4 ). Этот оксид восстанавливается до металла путем алюминотермической реакции или восстановления углеродом в доменной печи . [16]

Геологическая служба США оценивает мировые запасы кобальта в 7 100 000 метрических тонн. [69] Демократическая Республика Конго (ДРК) в настоящее время производит 63% мирового кобальта. Эта доля рынка может достичь 73% к 2025 году, если запланированное расширение горнодобывающих компаний, таких как Glencore Plc, произойдет, как ожидается. По оценкам Bloomberg New Energy Finance , к 2030 году мировой спрос на кобальт может вырасти в 47 раз по сравнению с 2017 годом . [70]
Изменения, внесенные Конго в законы о горнодобывающей промышленности в 2002 году, привлекли новые инвестиции в конголезские проекты по добыче меди и кобальта. В 2016 году рудник Мутанда компании Glencore отгрузил 24 500 тонн кобальта, что составляет 40% добычи в Конго и почти четверть мирового производства. В конце 2019 года из-за переизбытка предложения Glencore закрыла Mutanda на два года. [71] [72] Проект Glencore Katanga Mining также возобновляется и, по данным Glencore, к 2019 году должен произвести 300 000 тонн меди и 20 000 тонн кобальта. [65]
В 2005 году крупнейшим производителем кобальта были месторождения меди в провинции Катанга Демократической Республики Конго . По данным Британской геологической службы в 2009 году , в этой области, бывшей провинции Шаба, располагалось почти 40% мировых запасов. [73]
Кустарная добыча обеспечивала от 17% до 40% продукции ДРК. [74] Около 100 000 шахтеров кобальта в Конго (ДРК) используют ручные инструменты, чтобы выкопать сотни футов, практически не планируя и не принимая меньше мер безопасности, говорят рабочие, представители правительства и НПО, а также наблюдения репортеров The Washington Post о посещениях изолированных шахт. Отсутствие мер предосторожности часто приводит к травмам или смерти. [75] По словам представителей здравоохранения, горнодобывающая промышленность загрязняет окрестности и подвергает местную дикую природу и коренные общины воздействию токсичных металлов, которые, как считается, вызывают врожденные дефекты и затруднения дыхания. [76]
Детский труд используется при добыче кобальта на африканских кустарных рудниках . [74] [77] Правозащитники подчеркнули это, и журналистские расследования подтвердили это. [78] [79] Это открытие побудило производителя сотовых телефонов Apple Inc. 3 марта 2017 года прекратить покупать руду у поставщиков, таких как Zhejiang Huayou Cobalt , которые добывают руду на кустарных рудниках в ДРК, и начать использовать только проверенных поставщиков. соответствовать стандартам на рабочем месте. [80] [81]
Во всем мире ЕС и крупные производители автомобилей (OEM) настаивают на том, чтобы глобальное производство кобальта осуществлялось устойчиво, ответственно и с возможностью отслеживания цепочки поставок. Горнодобывающие компании принимают и реализуют инициативы ESG в соответствии с рекомендациями ОЭСР и создают доказательства деятельности с нулевым или низким уровнем выбросов углекислого газа в цепочке поставок производства литий-ионных аккумуляторов . Эти инициативы уже реализуются с крупными горнодобывающими компаниями, кустарными и мелкими горнодобывающими компаниями (ASM). Производители автомобилей и цепочки поставок производителей аккумуляторов: Tesla, VW, BMW, BASF и Glencore участвуют в нескольких инициативах, таких как Инициатива «Ответственный кобальт» и исследование «Кобальт для развития». В 2018 году BMW Group в партнерстве с BASF, Samsung SDI и Samsung Electronics запустила в ДРК пилотный проект на одной пилотной шахте, чтобы улучшить условия и решить проблемы для старателей и близлежащих сообществ.
Политическая и этническая динамика региона в прошлом приводила к вспышкам насилия и многолетним вооруженным конфликтам, а также к перемещению населения. Эта нестабильность повлияла на цену кобальта, а также создала у участников Первой и Второй войн в Конго порочные стимулы к продолжению боевых действий, поскольку доступ к алмазным рудникам и другим ценным ресурсам помогал финансировать их военные цели, которые часто сводились к геноциду, и обогатило и самих бойцов. Хотя в 2010-х годах ДР Конго не подвергалась в последнее время вторжению соседних вооруженных сил, некоторые из самых богатых месторождений полезных ископаемых соседствуют с районами, где до сих пор часто происходят столкновения тутси и хуту, беспорядки продолжаются, хотя и в меньших масштабах, а беженцы по-прежнему бегут от вспышек насилия. [82]
Кобальт, добытый на небольших кустарных горнодобывающих предприятиях Конго, в 2007 году поставлялся единственной китайской компании Congo DongFang International Mining. Дочерняя компания Zhejiang Huayou Cobalt, одного из крупнейших в мире производителей кобальта, Конго DongFang поставляла кобальт некоторым крупнейшим мировым производителям аккумуляторов, которые производили аккумуляторы для повсеместно распространенных продуктов, таких как Apple iPhone . Из-за обвинений в трудовых нарушениях и экологических опасений компания LG Chem впоследствии провела аудит Congo DongFang в соответствии с руководящими принципами ОЭСР. LG Chem, которая также производит материалы для аккумуляторов для автомобильных компаний, ввела кодекс поведения для всех поставщиков, которых она проверяет. [83]
Проект горы Мукондо , которым управляет Центральноафриканская горнодобывающая и геологоразведочная компания (CAMEC) в провинции Катанга, может быть самым богатым запасом кобальта в мире. В 2008 году она произвела примерно одну треть от общего мирового производства кобальта. [84] В июле 2009 года CAMEC объявила о долгосрочном соглашении о поставке всей годовой продукции кобальтового концентрата с горы Мукондо в компанию Zhejiang Galico Cobalt & Nickel Materials из Китай. [85]
В феврале 2018 года глобальная компания по управлению активами AllianceBernstein определила ДРК как экономически « Саудовскую Аравию эпохи электромобилей» из-за ее ресурсов кобальта, который необходим для литий-ионных батарей , используемых в электромобилях . [86]
9 марта 2018 года президент Джозеф Кабила обновил Кодекс горнодобывающей промышленности 2002 года, увеличив размер роялти и объявив кобальт и колтан «стратегическими металлами». [87] [88]
Кодекс горнодобывающей промышленности 2002 г. был фактически обновлен 4 декабря 2018 г. [89]
В декабре 2019 года правозащитная неправительственная организация International Rights Advocates подала знаковый иск против Apple, Tesla , Dell , Microsoft и компании Google Alphabet за «сознательное получение выгоды, содействие и подстрекательство к жестокому и зверскому использованию маленьких детей» при добыче кобальта. . [90] Компании, о которых идет речь, отрицают свою причастность к детскому труду . [91]
В 2017 году некоторые геологоразведочные компании планировали обследовать старые серебряные и кобальтовые рудники в районе Кобальта, Онтарио , где, как предполагается, находятся значительные месторождения. [92]
Канадская компания Sherritt International перерабатывает кобальтовые руды на никелевых месторождениях на рудниках Моа на Кубе , а на острове есть еще несколько рудников в Майари , Камагуэй и Пинар-дель-Рио . Продолжающиеся инвестиции Sherritt International в кубинское производство никеля и кобальта при приобретении прав на добычу полезных ископаемых на 17–20 лет сделали коммунистическую страну третьей по запасам кобальта в 2019 году, опередив саму Канаду. [93]
Начиная с меньших объемов в 2021 году, Индонезия начала производить кобальт как побочный продукт производства никеля . К 2022 году страна стала вторым по величине производителем кобальта в мире, а компания Benchmark Mineral Intelligence прогнозирует, что добыча в Индонезии к 2030 году составит 20 процентов мирового производства. [94]
В 2016 году было использовано 116 000 тонн (128 000 коротких тонн) кобальта. [8] Кобальт использовался в производстве высокопроизводительных сплавов. [63] [64] Он также используется в некоторых аккумуляторных батареях.
Суперсплавы на основе кобальта исторически потребляли большую часть производимого кобальта. [63] [64] Температурная стабильность этих сплавов делает их пригодными для изготовления лопаток газовых турбин и авиационных реактивных двигателей , хотя монокристаллические сплавы на основе никеля превосходят их по характеристикам. [95] Сплавы на основе кобальта также устойчивы к коррозии и износу, что делает их, как и титан , полезными для изготовления ортопедических имплантатов , которые не изнашиваются с течением времени. Разработка износостойких кобальтовых сплавов началась в первом десятилетии 20 века со стеллитовых сплавов, содержащих хром с различным количеством вольфрама и углерода. Сплавы с карбидами хрома и вольфрама очень тверды и износостойки. [96] Специальные сплавы кобальт-хром- молибден, такие как виталлий , используются для изготовления деталей протеза (замены бедра и колена). [97] Сплавы кобальта также используются для зубного протезирования в качестве полезного заменителя никеля, который может быть аллергенным. [98] Некоторые быстрорежущие стали также содержат кобальт для повышения термостойкости и износостойкости. В постоянных магнитах используются специальные сплавы алюминия, никеля, кобальта и железа, известные как алнико , а также самария и кобальта ( самарий-кобальтовый магнит ) . [99] Он также легирован 95% платиной для ювелирных изделий, в результате чего получается сплав, подходящий для тонкого литья, который также является слегка магнитным. [100]
Оксид лития-кобальта (LiCoO 2 ) широко используется в катодах литий-ионных аккумуляторов . Материал состоит из слоев оксида кобальта с интеркалированным литием . Во время разрядки ( т. е. при отсутствии активной зарядки) литий высвобождается в виде ионов лития. [101] Никель-кадмиевые [102] (NiCd) и никель-металлогидридные [103] (NiMH) аккумуляторы также содержат кобальт для улучшения окисления никеля в аккумуляторе. [102] Исследование Transparency Market Research оценило мировой рынок литий-ионных аккумуляторов в 30 миллиардов долларов США в 2015 году и прогнозировало увеличение до более чем 75 миллиардов долларов США к 2024 году. [104]
Хотя в 2018 году большая часть кобальта в батареях использовалась в мобильных устройствах, [105] более поздним применением кобальта являются аккумуляторные батареи для электромобилей. Спрос на кобальт в этой отрасли увеличился в пять раз, что делает актуальным поиск нового сырья в более стабильных регионах мира. [106] Ожидается, что спрос сохранится или увеличится по мере увеличения распространенности электромобилей. [107] Разведочные работы в 2016–2017 годах включали территорию вокруг Кобальта, Онтарио, где многие серебряные рудники прекратили работу несколько десятилетий назад. [106] Потребление кобальта для электромобилей выросло на 81% по сравнению с первой половиной 2018 года до 7200 тонн в первой половине 2019 года при емкости аккумулятора 46,3 ГВтч. [108] [109]
Поскольку неоднократно сообщалось о детском и рабском труде при добыче кобальта, в первую очередь на кустарных рудниках ДР Конго, технологические компании, стремящиеся к этической цепочке поставок, столкнулись с нехваткой этого сырья, и [110] цена на металлический кобальт достигла девятилетнего уровня. максимум в октябре 2017 года, более 30 долларов США за фунт, по сравнению с 10 долларами США в конце 2015 года. [ 111 ] После избыточного предложения цена упала до более нормальных 15 долларов США в 2019 году. добыча кобальта в ДР Конго ряд поставщиков кобальта и их клиенты сформировали Справедливый кобальтовый альянс (FCA), целью которого является прекращение использования детского труда и улучшение условий труда при добыче и переработке кобальта в ДР Конго. Членами FCA являются Zhejiang Huayou Cobalt , Sono Motors , The Responsible Cobalt Initiative, Fairphone , Glencore и Tesla, Inc. [114] [115]
Европейский Союз проводит исследования возможности устранения требований к кобальту при производстве литий-ионных аккумуляторов. [116] [117] По состоянию на август 2020 года производители аккумуляторов постепенно снизили содержание кобальта в катоде с 1/3 ( NMC 111) до 1/5 (NMC 442) до 1/10 (NMC 811), а также ввели кобальт. свободный литий-железо-фосфатный катод в аккумуляторные блоки электромобилей, таких как Tesla Model 3 . [118] [119] В сентябре 2020 года Tesla изложила свои планы по производству собственных аккумуляторных элементов, не содержащих кобальт. [120]
Литий-железо-фосфатные батареи официально превзошли тройные кобальтовые батареи в 2021 году с 52% установленной емкости. По оценкам аналитиков, в 2024 году его доля рынка превысит 60%. [121]
Некоторые соединения кобальта являются катализаторами окисления . Ацетат кобальта используется для преобразования ксилола в терефталевую кислоту , предшественник объемного полимера полиэтилентерефталата . Типичными катализаторами являются карбоксилаты кобальта (известные как кобальтовые мыла). Они также используются в красках, лаках и чернилах в качестве «высыхающих агентов» посредством окисления олифы . [122] [101] Однако их использование постепенно прекращается из-за проблем токсичности. [123] Те же карбоксилаты используются для улучшения сцепления между сталью и резиной в радиальных шинах со стальным кордом. Кроме того, они используются в качестве ускорителей в системах полиэфирных смол . [124] [125] [126]
Катализаторы на основе кобальта используются в реакциях с участием оксида углерода . Кобальт также является катализатором процесса Фишера-Тропша гидрирования окиси углерода в жидкое топливо . [127] При гидроформилировании алкенов в качестве катализатора часто используется октакарбонил кобальта . [128]
При гидрообессеривании нефти используется катализатор, полученный из кобальта и молибдена . Этот процесс помогает очистить нефть от примесей серы, мешающих переработке жидкого топлива. [101]


До 19 века кобальт преимущественно использовался в качестве пигмента. Со времен Средневековья его использовали для изготовления смальты — стекла синего цвета. Смальту производят путем плавления смеси обожженного минерала смальтита , кварца и карбоната калия , в результате чего получается темно-синее силикатное стекло, которое после производства тонко измельчается. [129] Смальта широко использовалась для окраски стекла и в качестве пигмента для картин. [130] В 1780 году Свен Ринман открыл зеленый кобальт , а в 1802 году Луи Жак Тенар открыл синий кобальт . [131] Кобальтовые пигменты, такие как кобальтовый синий (алюминат кобальта), лазурный синий (станнат кобальта (II), различные оттенки кобальтово-зеленого (смесь оксида кобальта (II) и оксида цинка ) и кобальтовый фиолетовый ( фосфат кобальта ). используются в качестве художественных пигментов из-за их превосходной хроматической стабильности. [132] [133]
Кобальт-60 (Co-60 или Co -60 ) полезен в качестве источника гамма-излучения, поскольку его можно производить в предсказуемых количествах с высокой активностью путем бомбардировки кобальта нейтронами . Он производит гамма-лучи с энергиями 1,17 и 1,33 МэВ . [33] [134]
Кобальт используется в дистанционной лучевой терапии , стерилизации предметов медицинского назначения и медицинских отходов, радиационной обработке пищевых продуктов для стерилизации (холодная пастеризация ), [135] промышленной радиографии (например, рентгенограммах целостности сварных швов), измерениях плотности (например, измерения плотности бетона) и резервуарах. переключатели высоты заполнения. Металл имеет досадное свойство образовывать мелкую пыль, что вызывает проблемы с радиационной защитой . Кобальт из аппаратов лучевой терапии представлял собой серьезную опасность, если его не утилизировать должным образом, и одна из самых страшных аварий с радиационным загрязнением в Северной Америке произошла в 1984 году, когда выброшенный аппарат лучевой терапии, содержащий кобальт-60, был по ошибке разобран на свалке в Хуаресе, Мексика. [136] [137]
Кобальт-60 имеет период радиоактивного полураспада 5,27 года. Потеря эффективности требует периодической замены источника при лучевой терапии и является одной из причин, по которой в современной лучевой терапии кобальтовые аппараты в значительной степени были заменены линейными ускорителями . [138] Кобальт-57 (Co-57 или 57 Co) представляет собой радиоизотоп кобальта, который чаще всего используется в медицинских тестах, в качестве радиометки для поглощения витамина B 12 и для теста Шиллинга . Кобальт-57 используется в качестве источника в мессбауэровской спектроскопии и является одним из нескольких возможных источников в рентгеновских флуоресцентных устройствах. [139] [140]
В конструкции ядерного оружия можно намеренно включать 59 Co, часть которого будет активирована при ядерном взрыве с образованием 60 Co. 60 Co, рассеянный в виде ядерных осадков , иногда называют кобальтовой бомбой . [141]
[142]
Кобальт необходим для обмена веществ всех животных. Это ключевой компонент кобаламина , также известного как витамин B12 , основного биологического резервуара кобальта как ультра-микроэлемента . [145] [146] Бактерии в желудках жвачных животных преобразуют соли кобальта в витамин B 12 , соединение, которое может вырабатываться только бактериями или архей . Таким образом, минимальное присутствие кобальта в почве заметно улучшает здоровье пасущихся животных, и рекомендуется его потребление в дозе 0,20 мг/кг в день, поскольку у них нет другого источника витамина B 12 . [147]
Белки на основе кобаламина используют коррин для удержания кобальта. Коэнзим B 12 имеет реакционноспособную связь C-Co, которая участвует в реакциях. [148] У людей B 12 имеет два типа алкильных лигандов : метил и аденозил. MeB 12 способствует переносу метильной (-CH 3 ) группы. Аденозильный вариант B 12 катализирует перегруппировки, при которых атом водорода непосредственно переносится между двумя соседними атомами с сопутствующей заменой второго заместителя X, который может представлять собой атом углерода с заместителями, атом кислорода спирта или амина. Метилмалонил-коэнзим А-мутаза (MUT) превращает MML-CoA в Su-CoA , что является важным этапом извлечения энергии из белков и жиров. [149]
Хотя они гораздо менее распространены, чем другие металлопротеины (например, цинка и железа), помимо B 12 известны и другие кобальтопротеины . Эти белки включают метионинаминопептидазу 2 , фермент, встречающийся у людей и других млекопитающих, который не использует корриновое кольцо B 12 , но напрямую связывает кобальт. Другим некорриновым кобальтовым ферментом является нитрилгидратаза , фермент бактерий, который метаболизирует нитрилы . [150]
У человека потребление кобальтсодержащего витамина B 12 удовлетворяет все потребности в кобальте. Для крупного рогатого скота и овец, которые удовлетворяют потребности в витамине B12 за счет синтеза резидентными бактериями в рубце, существует функция неорганического кобальта. В начале 20 века, во время развития земледелия на вулканическом плато Северного острова в Новой Зеландии, крупный рогатый скот страдал от так называемой «кустарниковой болезни». Было обнаружено, что в вулканических почвах отсутствуют соли кобальта, необходимые для пищевой цепи крупного рогатого скота. [151] [152] Было обнаружено , что «береговая болезнь» овец в пустыне Девяносто миль на юго-востоке Южной Австралии в 1930-х годах возникла из-за дефицита в питании микроэлементов кобальта и меди. Дефицит кобальта был преодолен за счет разработки «кобальтовых пуль» — плотных гранул оксида кобальта, смешанных с глиной, которые вводились перорально и попадали в рубец животного . [ нужны разъяснения ] [153] [152] [154]
По оценкам , значение LD 50 для растворимых солей кобальта составляет от 150 до 500 мг/кг. [156] В США Управление по охране труда (OSHA) определило допустимый предел воздействия (PEL) на рабочем месте как средневзвешенное по времени значение (TWA) 0,1 мг/м 3 . Национальный институт охраны труда (NIOSH) установил рекомендуемый предел воздействия (REL) на уровне 0,05 мг/м 3 , средневзвешенное по времени. Значение IDLH (непосредственно опасно для жизни и здоровья) составляет 20 мг/м 3 . [157]
Однако хроническое употребление кобальта в дозах, намного меньших смертельной, вызывает серьезные проблемы со здоровьем. В 1966 году добавление соединений кобальта для стабилизации пивной пены в Канаде привело к своеобразной форме токсин-индуцированной кардиомиопатии , которая стала известна как кардиомиопатия любителя пива . [158] [159]
Кроме того, согласно монографиям Международного агентства по исследованию рака (IARC) , металлический кобальт подозревается в вызывании рака (т.е. возможно канцерогенном , группа 2B IARC ) . [160]
При вдыхании вызывает проблемы с дыханием. [161] При прикосновении он также вызывает проблемы с кожей; После никеля и хрома кобальт является основной причиной контактного дерматита . [162]
шахта будет поставлена на уход и техническое обслуживание сроком не менее двух лет.