В супрамолекулярной химии [ 1] химия хозяин-гость описывает комплексы , состоящие из двух или более молекул или ионов , которые удерживаются вместе в уникальных структурных отношениях силами, отличными от сил полностью ковалентных связей . Химия хозяин-гость охватывает идею молекулярного распознавания и взаимодействия посредством нековалентной связи . Нековалентная связь имеет решающее значение для поддержания трехмерной структуры больших молекул, таких как белки, и участвует во многих биологических процессах, в которых большие молекулы специфически, но временно связываются друг с другом.
Хотя нековалентные взаимодействия можно грубо разделить на взаимодействия с большим электростатическим или дисперсионным вкладом, существует несколько общеупотребительных типов нековалентных взаимодействий: ионная связь , водородная связь , силы Ван-дер-Ваальса и гидрофобные взаимодействия . [2]
Взаимодействие хозяина и гостя привлекло к себе огромное внимание с момента его открытия. Это важная область, поскольку многие биологические процессы требуют взаимодействия хозяина и гостя, и оно может быть полезным в некоторых конструкциях материалов. Существует несколько типичных молекул-хозяев, таких как циклодекстрин, краун-эфир и др .


Хотя Ван-дер-Ваальс постулировал межмолекулярное взаимодействие в 1873 году, в 1894 году Фишер построил философскую основу для супрамолекулярной химии . Он указал, что взаимодействия ферментов и белков ведут себя по принципу «замок и ключ». Это взаимодействие является основой химии хозяина и гостя. С более глубоким пониманием нековалентных взаимодействий, например, с четким разъяснением структуры ДНК , химики начали подчеркивать важность нековалентных взаимодействий. [5] В 1967 году Чарльз Дж. Педерсен открыл краун-эфиры, которые представляют собой кольцеобразные структуры, способные хелатировать определенные ионы металлов. Затем, в 1969 году, Жан-Мари Лен открыл класс молекул, похожих на краун-эфиры, называемых криптандами. После этого Дональд Дж. Крам синтезировал множество вариаций краун-эфиров, поверх отдельных молекул, способных избирательно взаимодействовать с определенными химическими веществами. Трое ученых были удостоены Нобелевской премии по химии в 1987 году за «разработку и использование молекул со структурно-специфическими взаимодействиями высокой селективности». [6] В 2016 году Бернард Л. Феринга, сэр Дж. Фрейзер Стоддарт и Жан-Пьер Соваж были удостоены Нобелевской премии по химии «за разработку и синтез молекулярных машин ». [7]
Супрамолекулярная химия относится к химическим системам, которые содержат дискретное число химических компонентов. Силы систем варьируются от межмолекулярных сил до ковалентных связей. Исследователи, упомянутые выше, создали и расширили область взаимодействия хозяина и гостя, одну из важнейших концепций областей супрамолекулярной химии. Во взаимодействии хозяина и гостя есть два важных компонента. Один из них - это «молекулы хозяина», которые обычно имеют «порообразную» структуру, которая способна захватывать некоторые другие молекулы. Другой - это «молекулы гостя», которые, как правило, меньше молекул хозяина и способны связывать молекулы хозяина. Движущие силы взаимодействия могут различаться, например, гидрофобный эффект, хелатный эффект, сила Ван-дер-Ваальса и т. д. [8] Различные связи будут обеспечивать различные свойства для материалов, т. е. чувствительность к раздражителям, самовосстановление, жесткость матрицы. В результате взаимодействие хозяина и гостя может применяться для самовосстанавливающихся материалов, материалов, реагирующих на раздражители, фосфоресценции при комнатной температуре (RTP), улучшения механических свойств и т. д. Размеры молекул хозяина и гостя играют существенную роль во взаимодействиях, и некоторые типичные примеры взаимодействий хозяина будут рассмотрены ниже. [8] [9] [10] [11]
Химия хозяина-гостя — это раздел супрамолекулярной химии , в котором молекула хозяина связывает так называемую гостевую молекулу или ион. Два компонента комплекса взаимодействуют нековалентными силами, чаще всего водородными связями . Связывание между хозяином и гостем может быть высокоселективным, в этом случае взаимодействие называется молекулярным распознаванием . Часто между несвязанными и связанными состояниями существует динамическое равновесие :
Компонент «хозяина» часто представляет собой большую молекулу, и она охватывает меньшую молекулу «гостя». В биологических системах аналогичные термины хозяин и гость обычно называются ферментом и субстратом соответственно. [12]

Краун-эфиры хорошо известны своей способностью связывать металлические каионы. Например, 12-краун-4, 15-краун-5, 18-краун-6, 21-краун-7 и 24-краун-8 взаимодействуют с ионами калия, натрия, аммония и кальция соответственно. [8] Помимо ионного гостя, краун-эфиры также связываются с некоторыми нейтральными молекулами, например , 1, 2, 3-триазолом. Краун-эфиры также могут быть связаны с тонкими линейными молекулами и/или полимерами, что приводит к образованию супрамолекулярных структур, называемых ротаксанами. Учитывая, что краун-эфиры не связаны с цепями, они могут двигаться вверх и вниз по связанной молекуле. [11]
Циклодекстрин (CD) — это трубчатые молекулы, состоящие из нескольких единиц глюкозы, соединенных эфирными связями. Три типа CD, α-CD (6 единиц), β-CD (7 единиц) и γ-CD (8 единиц) различаются по размеру полостей: 5, 6 и 8 Å соответственно. α-CD может нанизываться на одну цепь ПЭГ, тогда как γ-CD может нанизываться на 2 цепи ПЭГ. β-CD может связываться с молекулой на основе тиофена. [8]

Структура криптофанов содержит 6 фенильных колец, в основном соединенных 4 способами. Благодаря фенильным группам и алифатическим цепям клетки внутри криптофанов являются высокогидрофобными, что предполагает возможность захвата неполярных молекул. Исходя из этого, криптофаны могут быть использованы для захвата ксенона в водном растворе, что может быть полезно в биологических исследованиях. [8]
Ниже представлена одна из классических структур резорцинаренов и пирогаллоларенов . Из-за фенольной группы между молекулами образуются некоторые водородные связи . Иногда соотношение связывания хозяина и гостя может достигать 2 : 1. [8] Кукурбит[n]урилы имеют схожий размер γ-CD, которые также ведут себя аналогично ( например , 1 кукурбит[n]урил может нанизываться на 2 цепи ПЭГ). [8]
Термодинамику взаимодействия хозяин-гость можно оценить с помощью ЯМР-спектроскопии, УФ/видимой спектроскопии и изотермической титрационной калориметрии. [13] Количественный анализ значений констант связывания дает полезную термодинамическую информацию. [12]
Константа ассоциации может быть определена выражением
где {HG} — термодинамическая активность комплекса в равновесии. {H} представляет активность хозяина, а {G} — активность гостя. Величины , и — соответствующие концентрации, а — частное коэффициентов активности .
На практике константа равновесия обычно определяется через концентрации.
При использовании этого определения подразумевается, что отношение коэффициентов активности имеет численное значение, равное единице. Тогда оказывается, что константа равновесия имеет размерность 1/концентрация, но это не может быть правдой, поскольку стандартное изменение свободной энергии Гиббса пропорционально логарифму .
Этот очевидный парадокс разрешается, когда размерность определяется как обратная размерности частного концентраций. Подразумевается, что рассматривается как имеющая постоянное значение при всех соответствующих экспериментальных условиях. Тем не менее, общепринятой практикой является приписывание размерности, например миллимоль на литр или микромоль на литр, значению K, которое было определено экспериментально.
Большое значение указывает на то, что молекулы хозяина и гостя сильно взаимодействуют, образуя комплекс хозяин–гость.
Когда молекулы хозяина и гостя объединяются в единый комплекс, равновесие представляется как
а константа равновесия K определяется как
где [X] обозначает концентрацию химического вещества X (предполагается, что все коэффициенты активности имеют числовые значения 1). Уравнения баланса массы в любой точке данных
где и представляют собой общие концентрации хозяина и гостя, могут быть сведены к одному квадратному уравнению, скажем, [G] и, таким образом, могут быть решены аналитически для любого заданного значения K. Затем можно вывести концентрации [H] и [HG].
Следующим шагом в расчете является вычисление значения, , величины, соответствующей наблюдаемой величине . Затем, сумма квадратов, U, по всем точкам данных, np, может быть определена как
и это может быть минимизировано относительно значения константы стабильности, K, и параметра, такого как химический сдвиг вида HG (данные ЯМР) или его молярная поглощательная способность (данные УФ/видимого). Минимизация может быть выполнена в приложении для работы с электронными таблицами, таком как EXCEL , с использованием встроенной утилиты SOLVER.
Данная процедура применима к аддуктам 1:1.
В спектрах ядерного магнитного резонанса (ЯМР) наблюдаемое значение химического сдвига , δ , возникающее из данного атома, содержащегося в молекуле реагента и одном или нескольких комплексах этого реагента, будет средним взвешенным по концентрации значением всех сдвигов этих химических видов. Химический обмен предполагается быстрым в шкале времени ЯМР. термины мольных долей ,
— химический сдвиг i- го химического вида, содержащего ядро, и — концентрация/мольная доля ( c — концентрация/моль дм −3 ) этого вида. Это выражение имеет ту же математическую форму, что и закон Бера . Значения химического сдвига могут быть получены для более чем одного ядра аналогичным образом, которым поглощение может быть измерено на более чем одной длине волны. Типичные изотопы, которые могут использоваться в этом контексте, — это 1 H, 13 C и 31 P. Обычно при измерении значений химического сдвига 1 H используют дейтерированный растворитель .

Предполагается, что поглощение каждого вида пропорционально концентрации этого вида в соответствии с законом Бера-Ламберта .
где λ — длина волны, — оптическая длина пути кюветы, содержащей раствор N соединений ( хромофоров ), — молярная поглощательная способность (также известная как коэффициент экстинкции) i- го химического вида на длине волны λ, c i — его концентрация. Когда концентрации были рассчитаны, как указано выше, и поглощение было измерено для образцов с различными концентрациями хозяина и гостя, закон Бера-Ламберта дает набор уравнений на заданной длине волны, которые могут быть решены линейным методом наименьших квадратов для неизвестных значений коэффициента экстинкции на этой длине волны.
Обработка этого типа данных похожа на обработку данных поглощения. Фактически, уравнение, определяющее связь между интенсивностью флуоресценции и концентрацией видов, очень похоже.
где - интенсивность флуоресценции i-го вида при единичной концентрации.
Тепло, выделяющееся при добавлении аликвоты раствора хозяина к раствору, содержащему гостя, представляет собой сумму вкладов каждой реакции.
где - измеренное значение изменения тепла (скорректированное с учетом всех внешних тепловых вкладов) в точке данных j , - количество тепла, поглощенного или выделенного при образовании 1 моля i- го продукта реакции, и - фактическое изменение числа молей этого продукта в этой точке данных. рассчитывается путем решения уравнений баланса масс с заданными значениями констант равновесия. Если известны значения констант равновесия, стандартное изменение энтальпии можно рассчитать с помощью линейного процесса наименьших квадратов, в противном случае необходимо использовать нелинейный метод подгонки данных.
Изотермическая титрационная калориметрия обычно используется для определения значений как константы равновесия, так и соответствующей стандартной энтальпии реакции. Производители приборов ITC поставляют некоторое программное обеспечение, с помощью которого эти величины могут быть получены из значений экспериментальных данных.
Для каждого равновесия, включающего хозяина, H, и гостя G
константа равновесия, определяется как
Значения свободных концентраций и получаются путем решения уравнений баланса масс с известными или оценочными значениями констант устойчивости.
Затем концентрации каждого сложного вида также могут быть рассчитаны как . Связь между концентрацией вида и измеренным количеством специфична для метода измерения, как указано в каждом разделе выше. Используя эту связь, набор параметров, значения констант устойчивости и значения свойств, таких как молярная поглощательная способность или заданные химические сдвиги, могут быть уточнены с помощью нелинейного процесса уточнения наименьших квадратов . Для более подробного изложения теории см. Определение констант равновесия . Некоторые специализированные компьютерные программы перечислены в разделе Реализации .
Процесс связывания обратим, что указывает на то, что константа ассоциации (ka ) не намного больше константы диссоциации (kd ) . Объединяя скорость реакции, ka , kd , концентрацию и время, можно рассчитать соотношение свободной гостевой молекулы и времени. [14] Рассчитав интегрирование УФ-спектра или ЯМР , [15] [14] можно получить концентрацию как функцию кривой времени.
В кооперативности первоначальное связывание лиганда влияет на сродство хозяина к последующим лигандам. В положительной кооперативности первое связывание усиливает сродство хозяина к другому лиганду. Примерами положительной и отрицательной кооперативности являются рецептор гемоглобина и аспартата соответственно. [16]

Термодинамические свойства кооперативности были изучены для того, чтобы определить математические параметры, которые различают положительную или отрицательную кооперативность. Традиционное уравнение свободной энергии Гиббса гласит: . Однако для количественной оценки кооперативности в системе хозяин-гость необходимо учитывать энергию связи. Схема справа показывает связывание A, связывание B, положительное кооперативное связывание A–B и, наконец, отрицательное кооперативное связывание A–B. Поэтому альтернативная форма уравнения свободной энергии Гиббса будет иметь вид
где:
Считается, что если больше суммы и , то он положительно кооперативен. Если меньше, то он отрицательно кооперативен. [17] Химия хозяина-гостя не ограничивается взаимодействиями рецептор-линганд. Она также демонстрируется в системах ионного спаривания. Такие взаимодействия изучаются в водной среде с использованием синтетических металлоорганических хозяев и органических гостевых молекул. Например, поликатионный рецептор, содержащий медь (хозяин), координируется с такими молекулами, как тетракарбоксилаты, трикарбаллат, аспартат и ацетат (гости). Это исследование иллюстрирует, что энтропия, а не энтальпия, определяет энергию связи системы, приводящую к отрицательной кооперативности. Большое изменение энтропии возникает из-за смещения молекул растворителя, окружающих лиганд и рецептор. Когда несколько ацетатов связываются с рецептором, он высвобождает больше молекул воды в окружающую среду, чем тетракарбоксилат. Это привело к снижению свободной энергии, подразумевая, что система сотрудничает отрицательно. [18] В похожем исследовании с использованием гуанидиния, Cu(II) и гостей из поликарбоксилата было показано, что положительная кооперативность в значительной степени определяется энтальпией. [19] Помимо термодинамических исследований, химия хозяин-гость также имеет биологическое применение.

Самовосстанавливающийся гидрогель , созданный из модифицированного циклодекстрина и адамантана. [20] [22] Другая стратегия заключается в использовании взаимодействия между полимерной основой и молекулой-хозяином (молекула-хозяин, нанизываемая на полимер). Если процесс нанизывания достаточно быстрый, самовосстановление также может быть достигнуто. [21]
Структуры хозяин-гость могут обеспечить жесткую матрицу, которая защищает излучатели от гашения, продлевая срок службы фосфоресценции. [23] В этом случае можно использовать α-CD и CB, [24] [25] , в которых фосфор служит гостем для взаимодействия с хозяином. Например, производные 4-фенилпиридия взаимодействуют с CB и сополимеризуются с акриламидом . Полученный полимер дает ~2 с срока службы фосфоресценции. Кроме того, Чжу и др. использовали краун-эфир и ион калия для модификации полимера и усиления испускания фосфоресценции. [26]
Многие гостевые молекулы реагируют на свет. [27]
Система шифрования, построенная с помощью Pillar[5]арена, спиропирана и пентаннитрила (в свободном состоянии и привитых к полимеру), была создана Ваном и др . После УФ-облучения спиропиран трансформировался в мероцианин. Когда видимый свет освещал материал, мероцианин, близкий к Pillar[5]арен-свободному пентаннитрильному комплексу, быстрее трансформировался в спиропиран; напротив, тот, что близок к Pillar[5]арен-привитому пентаннитрильному комплексу, имел гораздо более медленную скорость трансформации. Это преобразование спиропирана в мероцианин можно использовать для шифрования сообщений. [28] Другая стратегия основана на металлоячейках и полициклических ароматических углеводородах. [29] Из-за различий в излучении флуоресценции между комплексом и клетками информация может быть зашифрована.
Хотя некоторые взаимодействия хозяин-гость не являются сильными, увеличение количества взаимодействия хозяин-гость может улучшить механические свойства материалов. Например, нанизывание молекул хозяина на полимер является одной из часто используемых стратегий для повышения механических свойств полимера. Требуется время для того, чтобы молекулы хозяина вылезли из полимера, что может быть способом рассеивания энергии. [22] [30] [31] Другой метод заключается в использовании медленного обмена взаимодействия хозяин-гость. Хотя медленный обмен улучшает механические свойства, одновременно будут принесены в жертву свойства самовосстановления. [32]
Традиционно химическое зондирование осуществлялось с помощью системы, которая содержит ковалентно связанный индикатор с рецептором через линкер. После связывания аналита индикатор меняет цвет или флуоресцирует. Этот метод называется подходом индикатор-спейсер-рецептор (ISR). [33] В отличие от ISR, анализ смещенного индикатора (IDA) использует нековалентное взаимодействие между рецептором (хозяином), индикатором и аналитом (гостем). Подобно ISR, IDA также использует колориметрические (C-IDA) и флуоресцентные (F-IDA) индикаторы. В анализе IDA рецептор инкубируется с индикатором. Когда аналит добавляется в смесь, индикатор высвобождается в окружающую среду. После высвобождения индикатор либо меняет цвет (C-IDA), либо флуоресцирует (F-IDA). [34]
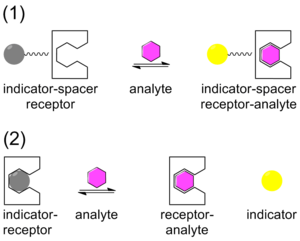
IDA предлагает несколько преимуществ по сравнению с традиционным подходом химического зондирования ISR. Во-первых, он не требует, чтобы индикатор был ковалентно связан с рецептором. Во-вторых, поскольку нет ковалентной связи, различные индикаторы могут использоваться с одним и тем же рецептором. Наконец, среда, в которой может использоваться анализ, разнообразна. [35]

Химические методы зондирования, такие как C-IDA, имеют биологические последствия. Например, протамин — это коагулянт, который обычно вводят после кардиопульмональной операции, который противодействует антикоагулянтной активности герапина. Для количественного определения протамина в образцах плазмы используется колориметрический анализ вытеснения. Краситель Azure A имеет синий цвет, когда он не связан, но когда он связан с герапином, он показывает фиолетовый цвет. Связь между Azure A и гепарином слабая и обратимая. Это позволяет протамину вытеснять Azure A. После высвобождения красителя он показывает фиолетовый цвет. Степень вытеснения красителя пропорциональна количеству протамина в плазме. [36]
F-IDA использовался Квальчиковским и его коллегами для мониторинга активности геликазы в E.coli . В этом исследовании они использовали тиазоловый оранжевый в качестве индикатора. Хеликаза раскручивает dsDNA, чтобы сделать ssDNA. Интенсивность флуоресценции тиазолового оранжевого имеет большее сродство к dsDNA, чем к ssDNA, и его интенсивность флуоресценции увеличивается, когда он связан с dsDNA, чем когда он не связан. [37] [38]
Кристаллическое твердое тело традиционно рассматривалось как статическое образование, в котором движения его атомных компонентов ограничены его колебательным равновесием. Как видно из превращения графита в алмаз, превращение твердого тела в твердое тело может происходить под физическим или химическим давлением. Было высказано предположение, что превращение из одной кристаллической структуры в другую происходит кооперативным образом. [39] [40] Большинство этих исследований были сосредоточены на изучении органического или металлоорганического каркаса. [41] [42] В дополнение к исследованиям макромолекулярного кристаллического превращения существуют также исследования монокристаллических молекул, которые могут изменять свою конформацию в присутствии органических растворителей. Было показано, что металлоорганический комплекс трансформируется в различные ориентации в зависимости от того, подвергается ли он воздействию паров растворителя или нет. [43]
Системы «хозяин-гость» были предложены для удаления опасных материалов. Определенные каликс[4]арены связывают ионы цезия-137, что в принципе может быть использовано для очистки радиоактивных отходов. Некоторые рецепторы связывают канцерогены. [44] [45]
{{cite book}}: CS1 maint: location missing publisher (link) CS1 maint: others (link)