
Координационный полимер представляет собой неорганическую или металлоорганическую полимерную структуру, содержащую катионные центры металлов, связанные лигандами . Более формально координационный полимер представляет собой координационное соединение с повторяющимися координационными единицами, простирающимися в 1, 2 или 3 измерениях. [1] [2]
Его также можно описать как полимер, повторяющиеся звенья которого представляют собой координационные комплексы . Координационные полимеры содержат подклассы координационных сетей, которые представляют собой координационные соединения, простирающиеся через повторяющиеся координационные единицы в одном измерении, но с поперечными связями между двумя или более отдельными цепями, петлями или спиро-связями, или координационное соединение, простирающееся через повторяющиеся координационные единицы. в 2 или 3 измерениях. Их подклассом являются металлоорганические каркасы , или MOF, которые представляют собой координационные сети с органическими лигандами, содержащими потенциальные пустоты. [1]
Координационные полимеры актуальны для многих областей и имеют множество потенциальных применений. [3]
Координационные полимеры можно классифицировать по-разному в зависимости от их структуры и состава. Одна важная классификация называется размерностью . Структуру можно определить как одно-, двух- или трехмерную, в зависимости от количества направлений в пространстве, в которых простирается массив. Одномерная структура простирается по прямой линии (вдоль оси x); двумерная структура простирается в плоскости (два направления, оси x и y); а трехмерная структура простирается во всех трех направлениях (оси x, y и z). [4] Это показано на рисунке 1.
Работы Альфреда Вернера и его современников заложили основу для изучения координационных полимеров. Многие проверенные временем материалы теперь признаны координационными полимерами. К ним относятся цианидные комплексы берлинской лазури и клатраты Гофмана . [5]
Координационные полимеры часто получают путем самосборки , включающей кристаллизацию соли металла с лигандом. Актуальны механизмы кристаллической инженерии и молекулярной самосборки . [3]

Структура и размерность координационного полимера определяются линкерами и координационной геометрией металлоцентра. Координационные числа чаще всего находятся в диапазоне от 2 до 10. [6] Примеры различных координационных чисел показаны в плоской геометрии на рисунке 2. На рисунке 1 одномерная структура является 2-координированной, плоская - 4-координированной, а трехмерная - 6-координированной. -скоординированный.

Металлические центры, часто называемые узлами или хабами, связываются с определенным количеством линкеров под четко определенными углами. Количество линкеров, связанных с узлом, известно как координационное число , которое вместе с углами, под которыми они удерживаются, определяет размерность структуры. Координационное число и координационная геометрия металлоцентра определяются неравномерным распределением электронной плотности вокруг него, и, как правило, координационное число увеличивается с размером катиона. Некоторые модели, в первую очередь модель гибридизации и теория молекулярных орбиталей , используют уравнение Шредингера для предсказания и объяснения геометрии координации, однако это сложно отчасти из-за сложного влияния окружающей среды на распределение электронной плотности . [8]
В качестве узлов обычно используются переходные металлы . Частично заполненные d -орбитали в атоме или ионе могут гибридизоваться по-разному в зависимости от окружающей среды. Эта электронная структура заставляет некоторые из них проявлять множественную координационную геометрию , особенно ионы меди и золота, которые в качестве нейтральных атомов имеют полные d-орбитали в своих внешних оболочках.
Лантаниды представляют собой большие атомы с координационными числами от 7 до 14. Их координационную среду сложно предсказать, что затрудняет их использование в качестве узлов. Они предлагают возможность включения люминесцентных компонентов.
Щелочные и щелочноземельные металлы существуют в виде стабильных катионов. Щелочные металлы легко образуют катионы со стабильными валентными оболочками, что придает им иное координационное поведение, чем у лантаноидов и переходных металлов. На них сильно влияет противоион соли , используемой в синтезе, чего трудно избежать. Все координационные полимеры, показанные на рисунке 3, представляют собой металлы второй группы. При этом размерность этих структур увеличивается по мере увеличения радиуса металла вниз по группе (от кальция к стронцию и к барию ).
Координационные полимеры требуют лигандов, способных образовывать множественные координационные связи, т.е. действовать как мостики между металлоцентрами. Известны многие мостиковые лиганды . Они варьируются от полифункциональных гетероциклов, таких как пиразин, до простых галогенидов. Лигандом может служить практически любой тип атома с неподеленной парой электронов .
Были исследованы очень сложные лиганды. [9] и фосфор , [10] [11] .

Лиганды могут быть гибкими и жесткими. Жесткий лиганд — это лиганд, который не имеет свободы вращаться вокруг связей или переориентироваться внутри структуры. Гибкие лиганды могут изгибаться, вращаться вокруг связей и переориентироваться. Эти различные конформации создают больше разнообразия в структуре. Известны примеры координационных полимеров, включающих в одной структуре две конфигурации одного и того же лиганда [12] , а также две отдельные структуры, единственное различие между которыми заключается в ориентации лигандов.
Длина лиганда может быть важным фактором, определяющим возможность образования полимерной структуры по сравнению с неполимерными (моно- или олигомерными) структурами. [13]
Помимо выбора металла и лиганда, существует множество других факторов, влияющих на структуру координационного полимера. Например, большинство металлоцентров представляют собой положительно заряженные ионы, существующие в виде солей. Противоион в соли может влиять на общую структуру . Например, когда соли серебра, такие как AgNO 3 , AgBF 4 , AgClO 4 , AgPF 6 , AgAsF 6 и AgSbF 6 , кристаллизуются с одним и тем же лигандом, структуры различаются с точки зрения координационного окружения металла, а также размерность всего координационного полимера. [14]
Кроме того, изменения в среде кристаллизации также могут изменить структуру. Изменения pH , [15] воздействие света или изменения температуры [16] могут изменить полученную структуру. Влияние на структуру, связанное с изменением условий кристаллизации, определяется в каждом конкретном случае.

В структуре координационных полимеров часто присутствуют пустые пространства в виде пор или каналов. Это пустое пространство термодинамически невыгодно. Чтобы стабилизировать структуру и предотвратить коллапс, поры или каналы часто занимают молекулы-гости. Молекулы-гости не образуют связей с окружающей решеткой, но иногда взаимодействуют посредством межмолекулярных сил, таких как водородные связи или пи-стэкинг. Чаще всего молекулой-гостем будет растворитель, в котором кристаллизовался координационный полимер, но на самом деле это может быть что угодно (присутствуют другие соли, атмосферные газы, такие как кислород , азот , диоксид углерода и т. д.). Иногда присутствие молекулы-гостя может быть влиять на структуру, поддерживая поры или каналы, которых в противном случае не было бы.
Координационные полимеры встречаются в некоторых коммерческих красках. Металлокомплексные красители с использованием меди или хрома обычно используются для получения тусклых цветов. Красители с тридентатными лигандами полезны, поскольку они более стабильны, чем их би- или монодентатные аналоги. [17] [18]
Некоторые первые коммерческие координационные полимеры представляют собой соединения Гофмана, имеющие формулу Ni(CN) 4 Ni(NH 3 ) 2 . Эти материалы кристаллизуются с небольшими ароматическими гостями (бензолом, некоторыми ксилолами), и эта селективность использовалась в коммерческих целях для разделения этих углеводородов. [19]
Пористые координационные полимеры, хотя это еще и непрактично, имеют потенциал в качестве молекулярных сит наряду с пористым углеродом и цеолитами . [5] Размер и форма пор могут контролироваться размером линкера, длиной и функциональными группами связывающих лигандов . Чтобы изменить размер пор и добиться эффективной адсорбции, нелетучие гости встраиваются в пространство пористого координационного полимера, чтобы уменьшить размер пор. Активные гости поверхности также могут способствовать адсорбции . Например, крупнопористый MOF-177 диаметром 11,8 Å может быть легирован молекулами C 60 (диаметром 6,83 Å) или полимерами с высокосопряженной системой с целью увеличения площади поверхности для адсорбции H 2 .
Гибкие пористые координационные полимеры потенциально привлекательны для молекулярного хранения, поскольку размеры их пор могут изменяться в результате физических изменений. Пример этого можно увидеть в полимере, который содержит молекулы газа в нормальном состоянии, но при сжатии полимер разрушается и высвобождает накопленные молекулы. В зависимости от структуры полимера, возможно, что структура будет достаточно гибкой, чтобы схлопывание пор было обратимым, и полимер можно было повторно использовать для повторного поглощения молекул газа. [20] На странице « Металло -органическая структура» есть подробный раздел, посвященный хранению газа H 2 .
Люминесцентные координационные полимеры обычно содержат органические хромофорные лиганды, которые поглощают свет, а затем передают энергию возбуждения иону металла. Координационные полимеры потенциально являются наиболее универсальными люминесцентными видами, поскольку их эмиссионные свойства сочетаются с гостевым обменом. Люминесцентные супрамолекулярные архитектуры в последнее время вызывают большой интерес из-за их потенциального применения в оптоэлектронных устройствах или в качестве флуоресцентных датчиков и зондов. Координационные полимеры часто более стабильны (устойчивы к термо- и растворителям), чем чисто органические полимеры. Для лигандов, которые флуоресцируют без присутствия металлического линкера (не из-за LMCT), интенсивное фотолюминесцентное излучение этих материалов имеет тенденцию быть на порядок выше, чем у одного свободного лиганда. Эти материалы могут быть использованы для разработки потенциальных кандидатов на светодиодные ( LED ) устройства. Резкое увеличение флуоресценции вызвано увеличением жесткости и асимметрии лиганда при координации с металлическим центром. [21]
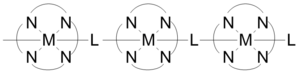
Координационные полимеры могут иметь в своей структуре короткие неорганические и сопряженные органические мостики, которые обеспечивают пути электропроводности . Примером таких координационных полимеров являются проводящие металлоорганические каркасы . Некоторые одномерные координационные полимеры, построенные, как показано на рисунке, обладают проводимостью в диапазоне от 1x10 -6 до 2x10 -1 См/см. Проводимость обусловлена взаимодействием d-орбитали металла и уровня pi* мостикового лиганда. В некоторых случаях координационные полимеры могут иметь полупроводниковое поведение. Трехмерные структуры, состоящие из листов серебросодержащих полимеров, демонстрируют полупроводимость, когда металлические центры выровнены, а проводимость уменьшается при переходе атомов серебра от параллельного к перпендикулярному направлению. [21]
Координационные полимеры обладают многими видами магнетизма . Антиферромагнетизм , ферримагнетизм и ферромагнетизм — это кооперативные явления магнитных спинов внутри твердого тела, возникающие в результате связи между спинами парамагнитных центров. Чтобы обеспечить эффективное магнитное поле, ионы металлов должны быть соединены небольшими лигандами, обеспечивающими короткие контакты металл-металл (такими как оксо-, циано- и азидо-мостики). [21]
Координационные полимеры также могут изменять цвет при изменении молекул растворителя , включенных в структуру. Примером этого могут быть два координационных полимера Co кластера [Re 6 S 8 (CN) 6 ] 4- , который содержит водные лиганды, которые координируются с атомами кобальта. Этот первоначально оранжевый раствор становится либо фиолетовым, либо зеленым при замене воды тетрагидрофураном и синим при добавлении диэтилового эфира. Таким образом, полимер может действовать как датчик растворителя, который физически меняет цвет в присутствии определенных растворителей. Изменение цвета связано с тем, что поступивший растворитель вытесняет водные лиганды у атомов кобальта, что приводит к изменению их геометрии с октаэдрической на тетраэдрическую. [21]