
Цикл кремнезема — это биогеохимический цикл , в котором биогенный кремнезем транспортируется между системами Земли. Кремний считается биоэссенциальным элементом и является одним из самых распространенных элементов на Земле. [2] [3] Цикл кремнезема во многом перекрывается с углеродным циклом (см. карбонатно-силикатный цикл ) и играет важную роль в секвестрации углерода посредством выветривания континентов , биогенного экспорта и захоронения в виде илов в геологических временных масштабах. [4]
Кремний — седьмой по распространенности элемент во Вселенной и второй по распространенности элемент в земной коре (самый распространенный — кислород). Выветривание земной коры дождевой водой, богатой углекислым газом, является ключевым процессом в контроле содержания углекислого газа в атмосфере . [5] [6] Это приводит к образованию кремниевой кислоты в водной среде. Кремниевая кислота Si(OH) 4 представляет собой гидратированную форму кремнезема, встречающуюся только в виде нестабильного раствора в воде, однако она играет центральную роль в кремнеземном цикле. [1]
Силикификаторы – это организмы, которые используют кремниевую кислоту для осаждения биогенного кремнезема SiO 2 . Биогенный кремнезем, также называемый опалом , осаждается силикификаторами в виде внутренних структур [7] и/или внешних структур. [8] Силикификаторы являются одними из наиболее важных водных организмов. К ним относятся такие микроорганизмы, как диатомовые водоросли , ризарии , силикофлагелляты и несколько видов хоанофлагеллят , а также макроорганизмы, такие как кремнистые губки . Фототрофные кремнеземы, такие как диатомовые водоросли, во всем мире потребляют огромное количество кремния вместе с азотом (N), фосфором (P) и неорганическим углеродом (C), связывая биогеохимию этих элементов и способствуя связыванию атмосферного углекислого газа в океане. . [9] Гетеротрофные организмы, такие как ризарии , хоанофлагелляты и губки , производят биогенный кремнезем независимо от фотоавтотрофного процесса переработки C и N. [10] [8] [11] [1]
Диатомовые водоросли доминируют в фиксации и экспорте твердых частиц в современном морском цикле кремнезема. Это включает в себя экспорт органического углерода из эвфотической зоны в глубокие глубины океана посредством биологического углеродного насоса . В результате диатомовые водоросли и другие организмы, выделяющие кремнезем, играют решающую роль в глобальном углеродном цикле , связывая углерод в океане. Связь между биогенным кремнеземом и органическим углеродом, а также значительно более высокий потенциал сохранности биогенных кремнистых соединений по сравнению с органическим углеродом делают записи накопления опалов интересными для палеоокеанографии и палеоклиматологии .
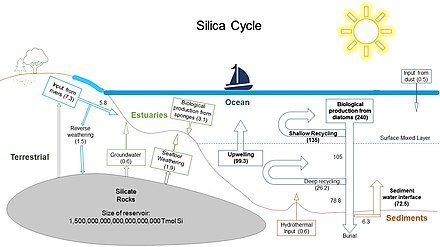
Понимание цикла кремнезема важно для понимания функционирования морских пищевых сетей , биогеохимических циклов и биологического насоса. Кремниевая кислота попадает в океан шестью путями, как показано на схеме выше, и все они в конечном итоге возникают в результате выветривания земной коры. [12] [1]
Кремнезем является важным питательным веществом, используемым растениями, деревьями и травами в земной биосфере . Силикат переносится реками и может откладываться в почвах в виде различных модификаций кремнезема . Растения легко усваивают силикат в виде H 4 SiO 4 для образования фитолитов . Фитолиты — это крошечные жесткие структуры, обнаруженные внутри растительных клеток, которые способствуют структурной целостности растения. [2] Фитолиты также служат для защиты растений от потребления травоядными животными , которые не могут эффективно потреблять и переваривать растения, богатые кремнеземом. [2] По оценкам , высвобождение кремнезема в результате деградации или растворения фитолитов происходит в два раза быстрее, чем глобальное выветривание силикатных минералов . [3] Учитывая биогеохимический цикл внутри экосистем, импорт и экспорт кремнезема в наземные экосистемы и из них невелики.
Силикатные минералы изобилуют горными породами по всей планете, составляя примерно 90% земной коры. [4] Основным источником силикатов в земной биосфере является выветривание . Процесс и скорость выветривания варьируются в зависимости от количества осадков, стока, растительности, литологии и топографии.
При наличии достаточного времени дождевая вода может растворить даже очень стойкий минерал на основе силиката, такой как кварц . [13] Вода разрывает связи между атомами в кристалле: [14]
Общая реакция растворения кварца приводит к образованию кремниевой кислоты.
Другим примером минерала на основе силиката является энстатит (MgSiO 3 ). Дождевая вода превращает это в кремниевую кислоту следующим образом: [15]
В последние годы влияние обратного выветривания на биогенный кремнезем представляет интерес для количественной оценки цикла кремнезема. Во время выветривания растворенный кремнезем попадает в океаны через ледниковый сток и речные стоки. [16] Этот растворенный кремнезем поглощается множеством морских организмов, таких как диатомовые водоросли , и используется для создания защитных панцирей. [16] Когда эти организмы умирают, они погружаются в толщу воды. [16] Без активной продукции биогенного SiO 2 минерал начинает диагенез . [16] Преобразование этого растворенного кремнезема в аутигенные силикатные глины в процессе обратного выветривания представляет собой удаление 20-25% входного кремния. [17]
Обратное выветривание часто наблюдается в дельтах рек , поскольку в этих системах наблюдаются высокие скорости накопления наносов и наблюдается быстрый диагенез. [18] Образование силикатных глин удаляет активный кремнезем из поровых вод осадочных пород, увеличивая концентрацию кремнезема, обнаруженного в породах, которые образуются в этих местах. [18]
Силикатное выветривание также, по-видимому, является доминирующим процессом в более глубоких метаногенных отложениях, тогда как обратное выветривание более распространено в поверхностных отложениях, но все же происходит с меньшей скоростью. [19]
Основным стоком земного круговорота кремнезема является его вывоз в океан реками. Кремнезем, который хранится в растительных веществах или растворяется, может быть вывезен реками в океан. Скорость этого транспорта составляет примерно 6 Тмоль Si/ год . [20] [3] Это основной поглотитель земного цикла кремнезема, а также крупнейший источник морского цикла кремнезема. [20] Незначительным поглотителем земного кремнезема является силикат, который откладывается в земных отложениях и в конечном итоге экспортируется в земную кору .
По состоянию на 2021 год наилучшая оценка общего поступления кремниевой кислоты в реки составляет 6,2 (±1,8) Тмоль Si/ год . [12] Это основано на данных, отражающих 60% мирового речного стока и средневзвешенную по расходу речную концентрацию кремниевой кислоты 158 мкм-Si. [22] [12] Однако кремниевая кислота — не единственный способ переноса кремния из наземных в речные системы, поскольку твердый кремний также может быть мобилизован в кристаллической или аморфной формах. [22] Согласно Сакконе и другим в 2007 году, [23] термин «аморфный кремнезем» включает биогенный кремнезем (из фитолитов , пресноводных диатомей , спикул губок ), измененный биогенный кремнезем и педогенные силикаты, все три из которых могут иметь одинаково высокие растворимость и реакционная способность. Доставка аморфного кремнезема в речную систему была рассмотрена Фрингсом и другими в 2016 году [24] , которые предложили значение 1,9(±1,0) Tmol Si/ год . Таким образом, общий речной приток составляет 8,1(±2,0) Tmol Si/ год . [1]
Никакого прогресса в отношении осаждения эоловой пыли в океан [25] и последующего выброса кремниевой кислоты в результате растворения пыли в морской воде не было достигнуто с 2013 года, когда Трегер и Де Ла Роша суммировали поток частиц растворимого кремнезема и влажное осаждение кремниевой кислоты в виде осадков. . [12] Таким образом, наилучшая оценка эолового потока кремниевой кислоты FA остается равной 0,5(±0,5) Tmol Si/ год . [1]
Исследование 2019 года показало, что в зоне прибоя на пляжах воздействие волн нарушало абиотические песчинки и со временем растворяло их. [26] Чтобы проверить это, исследователи поместили образцы песка в закрытые контейнеры с разными видами воды и вращали контейнеры, чтобы имитировать воздействие волн. Они обнаружили, что чем выше соотношение камня и воды внутри контейнера и чем быстрее вращается контейнер, тем больше кремнезема растворяется в растворе. После анализа и масштабирования своих результатов они подсчитали, что от 3,2 ± 1,0 до 5,0 ± 2,0 Тмоль Si/год литогенного DSi может попасть в океан с песчаных пляжей, что значительно превышает предыдущую оценку в 0,3 Тмоль Si/ год . [27] Если это подтвердится, это будет представлять собой значительный вклад растворенного LSi, который ранее игнорировался. [26] [1]

Кремнистые организмы в океане, такие как диатомовые водоросли и радиолярии , являются основным источником растворенной кремниевой кислоты в опаловом кремнеземе. [32] Ежегодно только 3% молекул кремния, растворенных в океане, экспортируются и навсегда откладываются в морских отложениях на морском дне, что свидетельствует о том, что рециркуляция кремния является доминирующим процессом в океанах. [3] Эта быстрая рециркуляция зависит от растворения кремнезема в органических веществах в толще воды с последующим биологическим поглощением в фотозоне . Предполагаемое время существования кремнеземного биологического резервуара составляет около 400 лет. [3] Опаловый кремнезем в Мировом океане преимущественно недонасыщен. Это недонасыщение способствует быстрому растворению в результате постоянной рециркуляции и длительного времени пребывания. Расчетный срок оборота Si составляет 1,5х10 4 года. [20] Общие чистые поступления и выбросы кремнезема в океан составляют 9,4 ± 4,7 Тмоль Si год -1 и 9,9 ± 7,3 Тмоль Si год -1 соответственно. [20]
Производство биогенного кремнезема в фотической зоне оценивается в 240 ± 40 Тмоль Si/ год . [20] Растворение на поверхности удаляет примерно 135 Тмоль Si в год -1 , а оставшийся Si экспортируется в глубины океана вместе с тонущими частицами. [3] В глубоком океане еще 26,2 Тмоль Si в год растворяется , а затем откладывается в отложениях в виде опалового дождя. [3] Более 90% кремнезема здесь растворяется, перерабатывается и в конечном итоге поднимается вверх для повторного использования в эвфотической зоне. [3]
Основными источниками морского кремнезема являются реки, потоки грунтовых вод, выветривание морского дна, гидротермальные жерла и атмосферные отложения ( эоловый поток ). [15] Реки на сегодняшний день являются крупнейшим источником кремнезема в морскую среду, на их долю приходится до 90% всего кремнезема, попадающего в океан. [15] [20] [35] Источником кремнезема для морского биологического цикла кремнезема является кремнезем, который был переработан путем подъема из глубин океана и морского дна.
Диаграмма низкотемпературных процессов показывает, как они могут контролировать растворение (аморфных или кристаллизованных) кремнистых минералов в морской воде в прибрежной зоне и глубоком океане, питая подводные грунтовые воды (F GW ) и растворенный кремний в морской воде и отложения (F W ). [1] Эти процессы соответствуют как низкому, так и среднему потоку энергии, диссипируемому в объеме данной кремниевой частицы в прибрежной зоне, на окраинах континентов и в безднах , и потоку высокой энергии, диссипируемому в зоне прибоя . [1]
Быстрое растворение на поверхности удаляет примерно 135 Тмоль опала Si в год , превращая его обратно в растворимую кремниевую кислоту, которую можно снова использовать для биоминерализации. [20] Оставшийся опаловый кремнезем экспортируется в глубокие океаны в виде тонущих частиц. [20] В глубоком океане еще 26,2 Тмоль Si в год растворяется , а затем откладывается в осадках в виде опалового кремнезема. [20] На границе раздела осадочных вод более 90% кремнезема перерабатывается и поднимается вверх для повторного использования в фотической зоне. [20] Производство биогенного кремнезема в фотической зоне оценивается в 240 ± 40 Тмоль/с / год . [36] Время пребывания в биологическом масштабе оценивается примерно в 400 лет, при этом каждая молекула кремнезема перерабатывается 25 раз перед захоронением отложений. [20]
Глубоководные отложения на морском дне являются крупнейшим долговременным стоком морского цикла кремнезема (6,3 ± 3,6 тмоль Si в год -1 ) и примерно уравновешиваются источниками кремнезема в океане. [15] Кремнезем, отложившийся в глубоком океане, в основном находится в форме кремнистого ила . Когда опаловый кремнезем накапливается быстрее, чем растворяется, он захоранивается и может обеспечить диагенетическую среду для формирования морских кремней . [37] Процессы, приводящие к образованию кремней, наблюдаются в Южном океане, где накопление кремнистого ила происходит быстрее всего. [37] Однако формирование кремня может занять десятки миллионов лет. [38] Фрагменты скелета кремнистых организмов подвержены рекристаллизации и цементации. [37] Черт является основной судьбой погребенного кремниевого ила и навсегда удаляет кремнезем из океанического цикла кремнезема.
Кремнистый ил со временем погружается под кору и метаморфизуется в верхней мантии . [39] Под мантией силикатные минералы образуются в илах и в конечном итоге поднимаются на поверхность. На поверхности кремнезем может снова войти в круговорот в результате выветривания. [39] Этот процесс может занять десятки миллионов лет. [39] Единственным другим крупным стоком кремнезема в океан являются захоронения вдоль окраин континентов (3,6 ± 3,7 Тмоль Si год -1 ), главным образом в виде кремнистых губок . [15] Из-за высокой степени неопределенности в оценках источников и поглотителей трудно сделать вывод, находится ли цикл морского кремнезема в равновесии. Время пребывания кремнезема в океанах оценивается примерно в 10 000 лет. [15] Кремнезем также можно удалить из круговорота, превратив в кремень и навсегда похоронив.
Развитие сельского хозяйства за последние 400 лет привело к увеличению обнажения горных пород и почв, что привело к увеличению скорости выветривания силикатов. В свою очередь, выщелачивание запасов аморфного кремнезема из почв также увеличилось, что приводит к увеличению концентрации растворенного кремнезема в реках. [15] И наоборот, усиление плотин привело к сокращению поступления кремнезема в океан из-за его поглощения пресноводными диатомовыми водорослями за плотинами. Преобладание некремниевого фитопланктона из-за антропогенной нагрузки азотом и фосфором и усиленного растворения кремнезема в более теплых водах потенциально может ограничить экспорт кремниевых океанских отложений в будущем. [15]
В 2019 году группа ученых предположила, что подкисление приводит к сокращению производства диатомового кремнезема в Южном океане . [40] [41]
Цикл кремнезема играет важную роль в долгосрочном регулировании глобального климата. Глобальный цикл кремнезема также оказывает большое влияние на глобальный углеродный цикл через карбонатно-силикатный цикл . [43] Процесс выветривания силикатных минералов переносит атмосферный CO 2 в гидрологический цикл посредством химической реакции, показанной выше. [4] В геологических временных масштабах скорость выветривания меняется из-за тектонической активности. Во время высокой скорости поднятия усиливается выветривание силикатов, что приводит к высоким темпам поглощения CO 2 , компенсируя увеличение вулканических выбросов CO 2 , связанных с геологической активностью. Этот баланс выветривания и вулканов является частью того, что контролирует парниковый эффект и pH океана в геологических временных масштабах.
Накопление биогенного кремнезема на морском дне содержит много информации о том, где в океане происходило экспортное производство в масштабах времени от сотен до миллионов лет. По этой причине записи об отложениях опалов предоставляют ценную информацию о крупномасштабных океанографических реорганизациях в геологическом прошлом, а также о палеопродуктивности. Среднее время пребывания силиката в океане составляет примерно 10 000–15 000 лет. Такое относительно короткое время пребывания делает концентрации и потоки океанических силикатов чувствительными к ледниковым / межледниковым возмущениям и, таким образом, является отличным показателем для оценки изменений климата. [44] [45]
Соотношения изотопов кислорода (O 18 :O 16 ) и кремния (Si 30 :Si 28 ) анализируются на основе биогенного кремнезема, сохранившегося в озерных и морских отложениях, с целью получения данных о прошлых изменениях климата и круговороте питательных веществ (De La Rocha, 2006; Leng и Баркер, 2006). Это особенно ценный подход, учитывая роль диатомовых водорослей в глобальном круговороте углерода. Кроме того, изотопный анализ BSi полезен для отслеживания прошлых изменений климата в таких регионах, как Южный океан , где сохранилось мало биогенных карбонатов .
Изотопный состав кремния в спикулах ископаемых губок (δ30Si) все чаще используется для оценки уровня кремниевой кислоты в морских условиях на протяжении всей геологической истории, что позволяет реконструировать прошлые циклы кремнезема. [46]
{{cite web}}: CS1 maint: multiple names: authors list (link)