Локус количественного признака ( QTL ) — локус (участок ДНК ) , который коррелирует с вариацией количественного признака в фенотипе популяции организмов . [1] QTL картируются путем определения того, какие молекулярные маркеры (такие как SNP или AFLP ) коррелируют с наблюдаемым признаком. Часто это ранний шаг в выявлении реальных генов , вызывающих вариацию признака.
Локус количественного признака ( QTL ) представляет собой область ДНК , которая связана с определенным фенотипическим признаком , степень которого варьируется и которую можно объяснить полигенными эффектами, т. е. продуктом двух или более генов и их окружения. [2] Эти QTL часто встречаются на разных хромосомах . Количество QTL, объясняющих вариации фенотипического признака, указывает на генетическую архитектуру признака. Это может указывать на то, что высота растения контролируется множеством генов с небольшим эффектом или несколькими генами с большим эффектом.
Как правило, QTL лежат в основе непрерывных признаков (тех признаков, которые непрерывно изменяются, например, рост), в отличие от дискретных признаков (признаков, которые имеют два или несколько значений признака, например, рыжие волосы у людей, рецессивный признак или гладкие или морщинистые горошины, используемые Менделем) . в своих экспериментах).
Более того, один фенотипический признак обычно определяется многими генами. Следовательно, многие QTL связаны с одним признаком. Другое использование QTL — идентификация генов-кандидатов, лежащих в основе признака. Последовательность ДНК любых генов в этой области затем можно сравнить с базой данных ДНК генов, функция которых уже известна, и эта задача имеет фундаментальное значение для улучшения сельскохозяйственных культур с помощью маркеров. [3] [4]
Менделевское наследие было вновь открыто в начале 20 века. По мере распространения идей Менделя генетики начали связывать менделевские правила наследования отдельных факторов с дарвиновской эволюцией . Ранним генетикам не сразу было ясно, что плавное изменение таких признаков, как размер тела (т. е. неполное доминирование ), вызвано наследованием отдельных генетических факторов. Хотя сам Дарвин заметил, что инбредные признаки необычных голубей наследуются в соответствии с законами Менделя (хотя Дарвин на самом деле не знал об идеях Менделя, когда делал это наблюдение), не было очевидным, что эти особенности, выбранные заводчиками необычных голубей, могут аналогичным образом объяснить количественные характеристики. изменчивость в природе. [5]
Ранняя попытка Уильяма Эрнеста Касла объединить законы менделевской наследственности с теорией видообразования Дарвина вызвала идею о том, что виды становятся отличными друг от друга по мере того, как тот или иной вид приобретает новый менделевский фактор. [6] Вывод Касла был основан на наблюдении, что новые черты, которые можно изучать в лаборатории и которые показывают менделевские закономерности наследования, отражают большое отклонение от дикого типа, и Касл считал, что приобретение таких признаков является основой «прерывистой изменчивости». ", что характеризует видообразование. [6] Дарвин обсуждал наследование сходных мутантных признаков, но не ссылался на них как на необходимое условие видообразования. [5] Вместо этого Дарвин использовал появление таких особенностей в размножающихся популяциях как доказательство того, что мутации могут происходить случайным образом внутри размножающихся популяций, что является центральной предпосылкой его модели отбора в природе. [5] Позже в своей карьере Касл усовершенствовал свою модель видообразования, чтобы учесть небольшие вариации, способствующие видообразованию с течением времени. Ему также удалось продемонстрировать это, путем селективного разведения лабораторных популяций крыс для получения фенотипа с капюшоном в течение нескольких поколений. [7]
Возможно, попытка Касла была первой попыткой, предпринятой в научной литературе, направить эволюцию путем искусственного отбора признака с непрерывными основными вариациями, однако ранее эта практика широко использовалась в развитии сельского хозяйства для получения домашнего скота или растений с благоприятными характеристиками из популяций, которые демонстрируют количественные вариации таких признаков, как размер тела или урожайность зерна.
Работа Касла была одной из первых попыток объединить недавно вновь открытые законы менделевской наследственности с теорией эволюции Дарвина. Тем не менее, пройдет почти тридцать лет, прежде чем теоретическая основа эволюции сложных признаков будет широко формализована. [8] В раннем изложении теории эволюции непрерывной изменчивости Сьюэлл Райт , аспирант, обучавшийся у Касла, резюмировал современные представления о генетической основе количественной естественной изменчивости: «По мере продолжения генетических исследований обнаруживались все меньшие различия. менделизировать, и любой персонаж, достаточно исследованный, оказался подвержен влиянию многих факторов». [8] Райт и другие формализовали теорию популяционной генетики, которая была разработана за предыдущие 30 лет, объясняя, как такие черты могут наследоваться и создавать стабильно размножающиеся популяции с уникальными характеристиками. Сегодня количественная генетика признаков использует наблюдения Райта о статистических взаимосвязях между генотипом и фенотипом в семьях и популяциях, чтобы понять, как определенные генетические особенности могут влиять на вариации в природных и производных популяциях.
Полигенное наследование означает наследование фенотипической характеристики (признака), которая связана с двумя или более генами и может быть измерена количественно. Многофакторное наследование относится к полигенному наследованию, которое также включает взаимодействие с окружающей средой. В отличие от моногенных признаков , полигенные признаки не следуют закономерностям менделевского наследования (дискретные категории). Вместо этого их фенотипы обычно варьируются по непрерывному градиенту, изображенному колоколообразной кривой . [9]
Примером полигенного признака является изменение цвета кожи человека . Несколько генов влияют на определение естественного цвета кожи человека, поэтому изменение только одного из этих генов может изменить цвет кожи незначительно, а в некоторых случаях, например, в случае SLC24A5 , умеренно. Многие заболевания с генетическими компонентами являются полигенными, включая аутизм , рак , диабет и многие другие. Большинство фенотипических характеристик являются результатом взаимодействия множества генов.
Примеры болезненных процессов, которые обычно считаются результатом действия многих способствующих факторов:
Врожденный порок развития
Заболевания, возникающие у взрослых
Утверждается, что многофакторные наследственные заболевания составляют большинство генетических нарушений, поражающих человека, которые влекут за собой госпитализацию или особый уход. [14] [15]
Признаки, контролируемые как средой, так и генетическими факторами, называются мультифакториальными. Обычно многофакторные признаки вне болезни приводят к тому, что мы считаем непрерывными характеристиками организмов, особенно человеческих, таких как рост, [14] цвет кожи и масса тела. [16] Все эти фенотипы осложнены большим количеством компромиссов между генами и воздействием окружающей среды. [14] Непрерывное распределение таких признаков, как рост и цвет кожи, описанное выше, отражает действие генов, которые не проявляют типичных закономерностей доминирования и рецессивности. Вместо этого считается, что вклад каждого вовлеченного локуса аддитивен. Авторы различали этот вид наследования как полигенное , или количественное наследование . [17]
Таким образом, из-за природы полигенных признаков наследование не будет следовать той же схеме, что и простое моногибридное или дигибридное скрещивание . [15] Полигенное наследование можно объяснить как менделевское наследование во многих локусах, [14] приводящее к нормальному распределению признака . Если n — количество вовлеченных локусов, то коэффициенты биномиального разложения ( a + b ) 2n дадут частоту распределения всех n комбинаций аллелей . При достаточно высоких значениях n это биномиальное распределение начнет напоминать нормальное распределение. С этой точки зрения болезненное состояние станет очевидным на одном из хвостов распределения после некоторого порогового значения. Будут ожидаться болезненные состояния возрастающей степени тяжести по мере того, как человек будет проходить дальше порогового значения и от среднего значения . [17]
Мутация, приводящая к болезненному состоянию, часто является рецессивной, поэтому оба аллеля должны быть мутантными, чтобы заболевание проявлялось фенотипически. Заболевание или синдром также могут быть результатом экспрессии мутантных аллелей более чем в одном локусе. Когда задействовано более одного гена, независимо от наличия триггеров окружающей среды, мы говорим, что заболевание является результатом многофакторного наследования.
Чем больше генов участвует в скрещивании, тем больше распределение генотипов будет напоминать нормальное или гауссово распределение. [14] Это показывает, что многофакторное наследование является полигенным, и генетические частоты можно предсказать с помощью полигибридного менделевского скрещивания. Другое дело — фенотипические частоты, особенно если они осложнены факторами окружающей среды.
Парадигма полигенного наследования, используемая для определения мультифакториального заболевания, вызвала много разногласий. Тернпенни (2004) обсуждает, что простое полигенное наследование не может объяснить некоторые заболевания, такие как начало сахарного диабета I типа, и что в таких случаях не все гены вносят одинаковый вклад. [17]
Предположение о полигенном наследовании состоит в том, что все вовлеченные локусы вносят равный вклад в симптомы заболевания. Это должно привести к нормальному (гауссову) распределению генотипов. В противном случае идея полигенетического наследования не может быть поддержана для этой болезни.
Вышеупомянутое является хорошо известными примерами заболеваний, имеющих как генетические, так и экологические компоненты. Другие примеры включают атопические заболевания, такие как экзема или дерматит ; [14] расщелина позвоночника (открытый позвоночник) и анэнцефалия (открытый череп). [10]
Хотя биопсихиатры широко полагают, что шизофрения является многофакторно-генетической , никакие характерные генетические маркеры не были определены с какой-либо уверенностью.
Если будет доказано, что братья и сестры пациента больны этим заболеванием, то существует большая вероятность того, что заболевание является генетическим [ нужна ссылка ] и что пациент также будет генетическим носителем. Этого недостаточно, поскольку необходимо также доказать, что тип наследования неменделевский. Для этого потребуется изучить десятки, даже сотни различных семейных родословных, прежде чем будет сделан вывод о многофакторном наследовании. Часто это занимает несколько лет.
Если действительно имеет место многофакторное наследование, то вероятность заражения пациента снижается только в том случае, если заболевание есть у двоюродных братьев и сестер и более дальних родственников. [10] Следует отметить, что хотя мультифакториально наследуемые заболевания имеют тенденцию передаваться в семьях, наследование не будет следовать той же схеме, что и простое моногибридное или дигибридное скрещивание . [15]
Если подозревается генетическая причина и мало что известно о заболевании, то еще предстоит выяснить, сколько именно генов участвует в фенотипическом проявлении заболевания. Как только это будет установлено, необходимо ответить на вопрос: если у двух людей есть необходимые гены, почему между ними существуют различия в экспрессии? Как правило, то, что отличает этих двух людей, скорее всего, является факторами окружающей среды. Из-за сложного характера генетических исследований, необходимых для определения таких закономерностей наследования, обычно это не первое направление исследований, которое выбирают для определения этиологии. [ нужна цитата ]
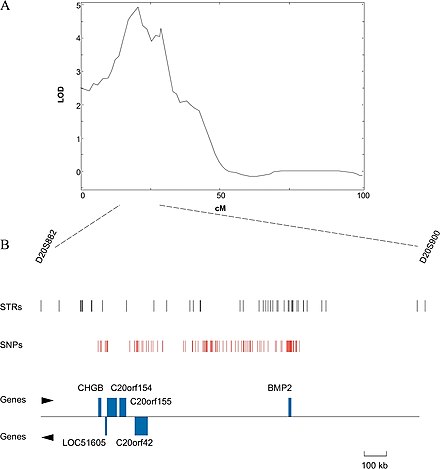

Для организмов, геномы которых известны, теперь можно попытаться исключить гены в идентифицированной области, функция которых известна с некоторой уверенностью и не связана с рассматриваемым признаком. Если геном недоступен, можно секвенировать идентифицированную область и определить предполагаемые функции генов по их сходству с генами с известной функцией, обычно в других геномах. Это можно сделать с помощью BLAST , онлайн-инструмента, который позволяет пользователям вводить первичную последовательность и искать похожие последовательности в базе данных BLAST генов различных организмов. Часто за фенотипическим признаком отвечает не сам ген, а скорее участок ДНК, тесно связанный с геном [18] [19]
Другой интерес статистических генетиков, использующих QTL-картирование, заключается в определении сложности генетической архитектуры, лежащей в основе фенотипического признака. Например, им может быть интересно узнать, формируется ли фенотип многими независимыми локусами или несколькими локусами, и взаимодействуют ли эти локусы. Это может предоставить информацию о том, как может развиваться фенотип. [20]
В недавней разработке классический анализ QTL был объединен с профилированием экспрессии генов, т.е. с помощью микрочипов ДНК . Такие QTL экспрессии (eQTL) описывают цис- и транс -контролирующие элементы для экспрессии часто ассоциированных с заболеванием генов. [21] Было обнаружено, что наблюдаемые эпистатические эффекты полезны для идентификации ответственного гена путем перекрестной проверки генов в взаимодействующих локусах с метаболическим путем - и баз данных научной литературы .
Самый простой метод картирования QTL — это дисперсионный анализ ( ANOVA , иногда называемый «маркерной регрессией») в маркерных локусах. В этом методе при обратном скрещивании можно рассчитать t-статистику для сравнения средних значений двух групп генотипов маркеров . Для других типов скрещиваний (таких как интеркросс), где существует более двух возможных генотипов, используется более общая форма ANOVA, которая обеспечивает так называемую F-статистику . Подход ANOVA для картирования QTL имеет три важных недостатка. Во-первых, мы не получаем отдельных оценок местоположения QTL и эффекта QTL. Местоположение QTL указывается только путем рассмотрения того, какие маркеры дают наибольшие различия между средними значениями групп генотипов, и видимый эффект QTL на маркере будет меньше, чем истинный эффект QTL в результате рекомбинации между маркером и QTL. Во-вторых, мы должны отбросить особей, чьи генотипы отсутствуют в маркере. В-третьих, когда маркеры расположены далеко друг от друга, QTL может находиться довольно далеко от всех маркеров, и поэтому эффективность обнаружения QTL снизится.
Ландер и Ботштейн разработали интервальное картирование, которое устраняет три недостатка дисперсионного анализа маркерных локусов. [22] Интервальное картирование в настоящее время является наиболее популярным подходом для картирования QTL в экспериментальных скрещиваниях. Этот метод использует генетическую карту типизированных маркеров и, как и дисперсионный анализ, предполагает наличие одного QTL. При картировании интервалов каждый локус рассматривается по одному, и логарифм отношения шансов ( оценка LOD ) рассчитывается для модели, согласно которой данный локус является истинным QTL. Отношение шансов связано с коэффициентом корреляции Пирсона между фенотипом и маркерным генотипом для каждой особи в экспериментальном скрещивании. [23]
Термин «интервальное картирование» используется для оценки положения QTL в пределах двух маркеров (часто обозначаемых как «маркерная скобка»). Интервальное отображение изначально основано на максимальном правдоподобии, но с помощью простой регрессии также возможны очень хорошие аппроксимации.
Принцип картирования QTL заключается в следующем: 1) Вероятность может быть рассчитана для заданного набора параметров (в частности, эффекта QTL и положения QTL) с учетом наблюдаемых данных о фенотипах и маркерных генотипах. 2) Оценки параметров – это те, вероятность которых наибольшая. 3) Порог значимости может быть установлен путем перестановочного тестирования. [24]
Обычные методы обнаружения локусов количественных признаков (QTL) основаны на сравнении моделей одиночного QTL с моделью, предполагающей отсутствие QTL. Например, в методе «интервального картирования» [25] вероятность наличия одного предполагаемого QTL оценивается в каждом месте генома. Однако QTL, расположенные в других частях генома, могут оказывать мешающее действие. Как следствие, способность обнаружения может быть поставлена под угрозу, а оценки местоположения и эффектов QTL могут быть необъективными (Lander and Botstein 1989; Knapp 1991). Могут появиться даже несуществующие так называемые «призрачные» QTL (Haley and Knott 1992; Martinez and Curnow 1992). Следовательно, несколько QTL можно картировать более эффективно и точно, используя несколько моделей QTL. [26] Одним из популярных подходов к картированию QTL, когда множественные QTL вносят вклад в признак, является итеративное сканирование генома и добавление известных QTL в регрессионную модель по мере идентификации QTL. Этот метод, называемый картированием составных интервалов, определяет как местоположение, так и размер эффекта QTL более точно, чем подходы с одним QTL, особенно в небольших популяциях картирования, где эффект корреляции между генотипами в картируемой популяции может быть проблематичным.
В этом методе выполняется картирование интервалов, используя подмножество маркерных локусов в качестве ковариат. Эти маркеры служат заместителями для других QTL для повышения разрешения картирования интервалов за счет учета связанных QTL и уменьшения остаточной вариации. Ключевая проблема CIM касается выбора подходящих маркерных локусов, которые будут служить ковариатами; как только они выбраны, CIM превращает задачу выбора модели в одномерное сканирование. Однако вопрос выбора маркерных ковариат еще не решен. Неудивительно, что подходящие маркеры — это те, которые наиболее близки к истинным QTL, и поэтому, если бы можно было их найти, проблема картирования QTL в любом случае была бы решена.
Инклюзивное картирование составных интервалов (ICIM) также было предложено в качестве потенциального метода картирования QTL. [27]
Картирование QTL на основе семьи или картирование на основе семейной родословной ( картирование связей и ассоциаций ) включает в себя несколько семей, а не одну семью. Картирование QTL на основе семейства было единственным способом картирования генов, в которых экспериментальные скрещивания провести сложно. Однако из-за некоторых преимуществ сейчас генетики растений пытаются использовать некоторые методы, впервые использованные в генетике человека. [28] Обсуждалось использование семейно-родословного подхода (Bink et al. 2008). Семейные связи и ассоциации были успешно реализованы (Rosyara et al. 2009) [29]
{{cite web}}: CS1 maint: архивная копия в заголовке ( ссылка )Евфитика 2008, 161:85–96.