

Мускариновые рецепторы ацетилхолина , или mAChR , представляют собой рецепторы ацетилхолина , которые образуют комплексы рецепторов, связанных с G-белком, в клеточных мембранах определенных нейронов [1] и других клеток . Они играют несколько ролей, в том числе действуют как основные концевые рецепторы, стимулируемые ацетилхолином , высвобождаемым из постганглионарных волокон парасимпатической нервной системы .
Мускариновые рецепторы названы так потому, что они более чувствительны к мускарину , чем к никотину . [2] Их аналогами являются никотиновые рецепторы ацетилхолина (nAChR), рецепторные ионные каналы, которые также важны в вегетативной нервной системе . Многие лекарства и другие вещества (например, пилокарпин и скополамин ) манипулируют этими двумя отдельными рецепторами, действуя как селективные агонисты или антагонисты . [3]
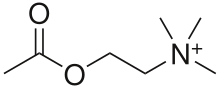
Ацетилхолин (АХ) — нейромедиатор, обнаруженный в головном мозге , нервно-мышечных соединениях и вегетативных ганглиях . Мускариновые рецепторы используются в следующих ролях:
АХ всегда используется в качестве нейромедиатора в вегетативном ганглии . Никотиновые рецепторы постганглионарного нейрона ответственны за начальную быструю деполяризацию (быстрый ВПСП ) этого нейрона. Вследствие этого никотиновые рецепторы часто называют рецепторами постганглионарных нейронов ганглия . Однако последующая гиперполяризация ( IPSP ) и медленная деполяризация (Slow EPSP), которые представляют собой восстановление постганглионарных нейронов после стимуляции, на самом деле опосредуются мускариновыми рецепторами типов M 2 и M 1 соответственно (обсуждается ниже). [ нужна цитата ]
Периферические вегетативные волокна (симпатические и парасимпатические волокна) анатомически классифицируются как преганглионарные или постганглионарные волокна , а затем далее обобщаются как адренергические волокна, выделяющие норадреналин, или холинергические волокна, одновременно высвобождающие ацетилхолин и экспрессирующие ацетилхолиновые рецепторы. Как преганглионарные симпатические волокна, так и преганглионарные парасимпатические волокна являются холинергическими. Большинство постганглионарных симпатических волокон являются адренергическими: их нейромедиатором является норадреналин, за исключением постганглионарных симпатических волокон, идущих к потовым железам, пилоэректильным мышцам волосков тела и артериолам скелетных мышц, которые не используют адреналин/норадреналин.
Мозговое вещество надпочечников считается симпатическим ганглием и, как и другие симпатические ганглии, снабжается холинергическими преганглионическими симпатическими волокнами: ацетилхолин является нейромедиатором, используемым в этом синапсе. Хромаффинные клетки мозгового вещества надпочечников действуют как «модифицированные нейроны», выделяя адреналин и норадреналин в кровоток в виде гормонов, а не нейромедиаторов. Остальные постганглионарные волокна периферической вегетативной системы относятся к парасимпатическому отделу; все они являются холинергическими волокнами и используют ацетилхолин в качестве нейромедиатора.
Другая роль этих рецепторов заключается в соединении иннервируемых тканей и постганглионарных нейронов парасимпатического отдела вегетативной нервной системы. Здесь ацетилхолин снова используется в качестве нейромедиатора, а мускариновые рецепторы образуют основные рецепторы иннервируемой ткани.
Очень немногие части симпатической системы используют холинергические рецепторы. В потовых железах рецепторы мускаринового типа . Симпатическая нервная система также имеет несколько преганглионарных нервов, оканчивающихся у хромаффинных клеток мозгового слоя надпочечников , которые секретируют адреналин и норадреналин в кровоток. Некоторые [ кто? ] считают, что хромаффинные клетки представляют собой модифицированные постганглионарные волокна ЦНС. В мозговом веществе надпочечников в качестве нейромедиатора используется ацетилхолин, а рецептор никотинового типа .
Соматическая нервная система использует никотиновый рецептор ацетилхолина в нервно-мышечном соединении.
Мускариновые рецепторы ацетилхолина также присутствуют и распределены по всей местной нервной системе, в постсинаптических и пресинаптических позициях. Есть также некоторые свидетельства того, что постсинаптические рецепторы на симпатических нейронах позволяют парасимпатической нервной системе ингибировать симпатические эффекты.
Известно, что мускариновые рецепторы ацетилхолина появляются также на пресинаптической мембране соматических нейронов нервно-мышечного соединения, где они участвуют в регуляции высвобождения ацетилхолина.
Мускариновые рецепторы ацетилхолина относятся к классу метаботропных рецепторов , которые используют G-белки в качестве сигнального механизма. В таких рецепторах сигнальная молекула ( лиганд ) связывается с мономерным рецептором , имеющим семь трансмембранных областей ; в данном случае лигандом является АХ. Этот рецептор связан с внутриклеточными белками, известными как G-белки, которые запускают информационный каскад внутри клетки. [4]
Напротив, никотиновые рецепторы образуют пентамерные комплексы и используют для передачи сигналов механизм лиганд-управляемых ионных каналов . В этом случае связывание лигандов с рецептором вызывает открытие ионного канала , позволяя одному или нескольким конкретным типам ионов (например, K + , Na + , Ca 2+ ) диффундировать в клетку или из нее.
С помощью селективных радиоактивно меченных агонистов и антагонистов были определены пять подтипов мускариновых рецепторов, названных М 1 –М 5 (с использованием заглавной буквы М и нижнего индекса). [5] Рецепторы M 1 , M 3 , M 5 связаны с белками Gq , а рецепторы M 2 и M 4 связаны с белками G i/o . [4] Существуют и другие системы классификации. Например, препарат пирензепин является мускариновым антагонистом (снижает действие АХ), который гораздо более эффективен в отношении рецепторов М 1 , чем в отношении других подтипов. Принятие различных подтипов происходило в числовом порядке, поэтому более ранние источники могут признавать только подтипы M 1 и M 2 , [ нужна ссылка ] , в то время как более поздние исследования признают подтипы M 3 , M 4 , [1] и совсем недавно M 5 подтипы. [ нужна цитата ]
Тем временем генетики и молекулярные биологи охарактеризовали пять генов, которые, по-видимому, кодируют мускариновые рецепторы, названные m1-m5 (строчная буква m, без индекса). Они кодируют фармакологические типы М 1 -М 5 . Рецепторы m1 и m2 определяли на основе частичного секвенирования белков рецепторов M1 и M2 . Остальные были найдены путем поиска гомологии с использованием биоинформатических методов.
G-белки содержат альфа-субъединицу, которая имеет решающее значение для функционирования рецепторов. Эти субъединицы могут принимать различные формы. Существует четыре широких класса форм G-белка: G s , G i , G q и G 12/13 . [6] Мускариновые рецепторы различаются по G-белку, с которым они связаны, с некоторой корреляцией в зависимости от типа рецептора. G-белки также классифицируются в зависимости от их чувствительности к холерному токсину (СТХ) и коклюшному токсину (ПТХ, коклюшный токсин). G s и некоторые подтипы Gi ( G αt и G αg ) чувствительны к CTX. Только Gi восприимчив к PTX, за исключением одного подтипа Gi ( Gαz ) , который обладает иммунитетом. Кроме того, только при связывании с агонистом те G-белки, которые обычно чувствительны к PTX, также становятся чувствительными к CTX. [7]
Различные субъединицы G-белка по-разному действуют на вторичные мессенджеры, повышая активность фосфолипаз, подавляя цАМФ и так далее.
Из-за сильной корреляции с типом мускариновых рецепторов CTX и PTX являются полезными экспериментальными инструментами для изучения этих рецепторов.
Этот рецептор опосредует медленное ВПСП в ганглии постганглионарного нерва , распространен в экзокринных железах и в ЦНС. [23] [24]
Он преимущественно обнаруживается связанным с G-белками класса Gq [ 25] , которые используют активацию фосфолипазы C и, следовательно, инозитолтрифосфата и внутриклеточного кальция в качестве сигнального пути. Связанный таким образом рецептор не будет восприимчив к CTX или PTX. Однако было показано, что G i (вызывающий снижение цАМФ ) и G s (вызывающий увеличение цАМФ) участвуют во взаимодействиях в определенных тканях и поэтому могут быть чувствительны к PTX и CTX соответственно.
Мускариновые рецепторы М 2 расположены в сердце и легких. В сердце они замедляют частоту сердечных сокращений ниже нормального синусового ритма , замедляя скорость деполяризации . У человека в условиях покоя активность блуждающего нерва доминирует над симпатической активностью. Следовательно, ингибирование рецепторов М 2 (например, атропином) приведет к увеличению частоты сердечных сокращений. Они также умеренно снижают сократительные силы предсердной сердечной мышцы и снижают скорость проводимости атриовентрикулярного узла (АВ-узла). Он также служит для незначительного уменьшения сократительной силы желудочковой мышцы .
Мускариновые рецепторы М 2 действуют через рецептор типа Gi , что вызывает снижение уровня цАМФ в клетке, ингибирование потенциалзависимых Са 2+ -каналов и увеличение оттока К + , что в целом приводит к эффектам ингибирующего типа.
Мускариновые рецепторы М 3 расположены во многих местах тела. Они расположены в гладких мышцах сосудов, а также в легких. Поскольку рецептор M 3 связан с G q и опосредует увеличение внутриклеточного кальция, он обычно вызывает сокращение гладких мышц, например, наблюдаемое во время бронхоконстрикции и мочеиспускания . [26] Однако, что касается сосудистой сети, активация М 3 на эндотелиальных клетках сосудов вызывает повышенный синтез оксида азота , который диффундирует к соседним гладкомышечным клеткам сосудов и вызывает их расслабление , тем самым объясняя парадоксальный эффект парасимпатомиметиков на сосудистый тонус и бронхиолярный тонус. тон. Действительно, прямая стимуляция гладких мышц сосудов М 3 опосредует вазоконстрикцию при заболеваниях, при которых нарушается эндотелий сосудов. [27] Рецепторы М 3 также расположены во многих железах, которые помогают стимулировать секрецию, например, в слюнных железах, а также в других железах организма.
Подобно мускариновому рецептору М1 , рецепторы М3 представляют собой G-белки класса Gq , которые активируют фосфолипазу С и, следовательно, инозитолтрифосфат и внутриклеточный кальций в качестве сигнального пути. [4]
Рецепторы М 4 обнаружены в ЦНС.
Рецепторы М 4 действуют через рецепторы Gi , снижая уровень цАМФ в клетке и, таким образом, оказывая в целом ингибирующее действие. Возможен бронхоспазм при стимуляции мускариновыми агонистами.
Местоположение рецепторов М 5 недостаточно известно.
Подобно мускариновым рецепторам М1 и М3 , рецепторы М5 связаны с G-белками класса Gq , которые активируют фосфолипазу С и, следовательно, инозитолтрифосфат и внутриклеточный кальций в качестве сигнального пути. [ нужна цитата ]
Лиганды , нацеленные на mAChR, которые в настоящее время одобрены для клинического использования, включают неселективные антагонисты для лечения болезни Паркинсона , [28] атропин (для расширения зрачка ), скополамин (используется для предотвращения укачивания ) и ипратропий (используется для лечения ХОБЛ ) . [3] [29]
{{cite book}}: CS1 maint: несколько имен: список авторов ( ссылка ){{cite journal}}: Требуется цитировать журнал |journal=( помощь )