Ацетилхолин ( АХ ) — органическое соединение , которое действует в мозге и теле многих видов животных (включая человека) в качестве нейромедиатора . [1] Его название происходит от его химической структуры: это сложный эфир уксусной кислоты и холина . [2] Части тела, которые используют ацетилхолин или подвергаются его воздействию, называются холинергическими .
Ацетилхолин — это нейротрансмиттер, используемый в нервно-мышечных соединениях , другими словами, это химическое вещество, которое выделяют мотонейроны нервной системы для активации мышц. Это свойство означает, что препараты, влияющие на холинергические системы, могут иметь очень опасные эффекты — от паралича до судорог. Ацетилхолин также является нейромедиатором в вегетативной нервной системе , как внутренним передатчиком симпатической нервной системы , так и конечным продуктом, выделяемым парасимпатической нервной системой . [1] Ацетилхолин является основным нейромедиатором парасимпатической нервной системы. [2] [3]
В мозге ацетилхолин действует как нейромедиатор и нейромодулятор . Мозг содержит ряд холинергических областей, каждая из которых выполняет различные функции; например, играет важную роль в возбуждении , внимании , памяти и мотивации . [4]
Ацетилхолин также был обнаружен в клетках неневрального происхождения, а также в микробах. Недавно ферменты, связанные с его синтезом, деградацией и клеточным поглощением, были прослежены до раннего происхождения одноклеточных эукариот. [5] Возбудитель простейших Acanthamoeba spp. продемонстрировали доказательства присутствия АХ, который обеспечивает рост и пролиферативные сигналы через расположенный на мембране гомолог М1-мускаринового рецептора. [6]
Частично из-за его функции активации мышц, а также из-за его функций в вегетативной нервной системе и мозге многие важные лекарства оказывают свое действие, изменяя холинергическую передачу. Многочисленные яды и токсины, вырабатываемые растениями, животными и бактериями, а также химические нервно-паралитические агенты , такие как зарин , причиняют вред, инактивируя или гиперактивируя мышцы, воздействуя на нервно-мышечные соединения. Препараты, действующие на мускариновые ацетилхолиновые рецепторы , такие как атропин , могут быть ядовитыми в больших количествах, но в меньших дозах они обычно используются для лечения определенных заболеваний сердца и глаз. [ нужна цитация ] Скополамин или дифенгидрамин , которые также действуют в основном на мускариновые рецепторы тормозным образом в мозге (особенно на рецептор М 1 ), могут вызывать делирий , галлюцинации и амнезию через антагонизм рецепторов в этих местах. По состоянию на 2016 год только подтип рецептора М1 был вовлечен в антихолинергический делирий. [7] Привыкание к никотину обусловлено его воздействием на никотиновые рецепторы ацетилхолина в головном мозге.
Ацетилхолин представляет собой молекулу холина , ацетилированную по атому кислорода . Из-за заряженной аммониевой группы ацетилхолин не проникает через липидные мембраны. В связи с этим при наружном введении молекула остается во внеклеточном пространстве и в настоящее время считается, что молекула не проходит через гематоэнцефалический барьер.
Ацетилхолин синтезируется в определенных нейронах ферментом холин - ацетилтрансферазой из соединений холина и ацетил-КоА . Холинергические нейроны способны продуцировать АХ. Примером центральной холинергической области является базальное ядро Мейнерта в базальном отделе переднего мозга. [8] [9] Фермент ацетилхолинэстераза превращает ацетилхолин в неактивные метаболиты холин и ацетат . Этот фермент широко распространен в синаптической щели, и его роль в быстром выведении свободного ацетилхолина из синапса важна для правильного функционирования мышц. Некоторые нейротоксины действуют путем ингибирования ацетилхолинэстеразы, что приводит к избытку ацетилхолина в нервно-мышечных соединениях , вызывая паралич мышц, необходимых для дыхания, и останавливая биение сердца.

Ацетилхолин действует как в центральной нервной системе (ЦНС), так и в периферической нервной системе (ПНС). В ЦНС холинергические проекции от базального отдела переднего мозга к коре головного мозга и гиппокампу поддерживают когнитивные функции этих целевых областей. В ПНС ацетилхолин активирует мышцы и является основным нейромедиатором вегетативной нервной системы. [10] [2]
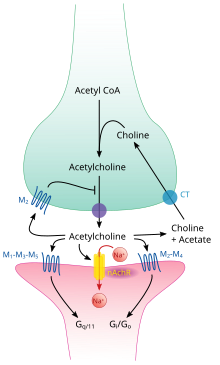
Как и многие другие биологически активные вещества, ацетилхолин оказывает свое действие путем связывания и активации рецепторов, расположенных на поверхности клеток. Существует два основных класса рецепторов ацетилхолина: никотиновые и мускариновые . Они названы в честь химических веществ, которые могут избирательно активировать каждый тип рецепторов, не активируя другой: мускарин — соединение, обнаруженное в грибе Amanita muscaria ; никотин содержится в табаке.
Никотиновые ацетилхолиновые рецепторы представляют собой лиганд-управляемые ионные каналы, проницаемые для ионов натрия , калия и кальция . Другими словами, это ионные каналы, встроенные в клеточные мембраны, способные переключаться из закрытого состояния в открытое при связывании с ними ацетилхолина; в открытом состоянии они пропускают ионы. Никотиновые рецепторы бывают двух основных типов: мышечные и нейрональные. Мышечный тип можно избирательно блокировать кураре , нейрональный тип — гексаметонием . Основное расположение рецепторов мышечного типа находится на мышечных клетках, как более подробно описано ниже. Рецепторы нейронального типа расположены в вегетативных ганглиях (как симпатических, так и парасимпатических) и в центральной нервной системе.
Мускариновые рецепторы ацетилхолина имеют более сложный механизм и влияют на клетки-мишени в течение более длительного периода времени. У млекопитающих идентифицировано пять подтипов мускариновых рецепторов, обозначенных от М1 до М5. Все они функционируют как рецепторы, связанные с G-белком , а это означает, что они оказывают свое воздействие через систему вторичных мессенджеров . Подтипы M1, M3 и M5 связаны с Gq ; они повышают внутриклеточные уровни IP 3 и кальция путем активации фосфолипазы C. Их воздействие на клетки-мишени обычно носит возбуждающий характер. Подтипы M2 и M4 связаны с Gi / Go ; они снижают внутриклеточные уровни цАМФ путем ингибирования аденилатциклазы . Их влияние на клетки-мишени обычно носит ингибирующий характер. Мускариновые рецепторы ацетилхолина обнаружены как в центральной нервной системе, так и в периферической нервной системе сердца, легких, верхних отделах желудочно-кишечного тракта и потовых железах.
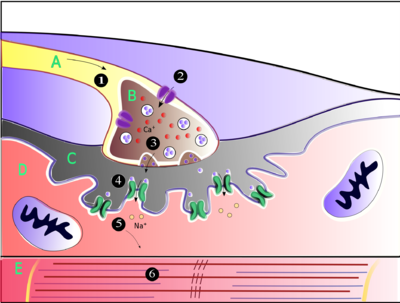
Ацетилхолин — это вещество, которое нервная система использует для активации скелетных мышц , разновидности поперечно-полосатых мышц. Это мышцы, используемые для всех типов произвольных движений, в отличие от гладкой мышечной ткани , которая участвует в ряде непроизвольных действий, таких как перемещение пищи через желудочно-кишечный тракт и сужение кровеносных сосудов. Скелетные мышцы напрямую контролируются мотонейронами , расположенными в спинном мозге или, в некоторых случаях, в стволе мозга . Эти мотонейроны посылают свои аксоны через двигательные нервы , из которых они выходят и соединяются с мышечными волокнами в специальном типе синапсов , называемом нервно-мышечным соединением .
Когда мотонейрон генерирует потенциал действия , он быстро перемещается по нерву, пока не достигнет нервно-мышечного соединения, где инициирует электрохимический процесс, вызывающий высвобождение ацетилхолина в пространство между пресинаптическим окончанием и мышечным волокном. Молекулы ацетилхолина затем связываются с никотиновыми рецепторами ионных каналов на мембране мышечных клеток, вызывая открытие ионных каналов. Затем ионы натрия поступают в мышечную клетку, запуская последовательность шагов, которые в конечном итоге вызывают мышечное сокращение .
Факторы, которые уменьшают высвобождение ацетилхолина (и тем самым влияют на кальциевые каналы P-типа ): [11]
Блокаторы кальциевых каналов (нифедипин, дилтиазем) не влияют на Р-каналы. Эти препараты влияют на кальциевые каналы L-типа .
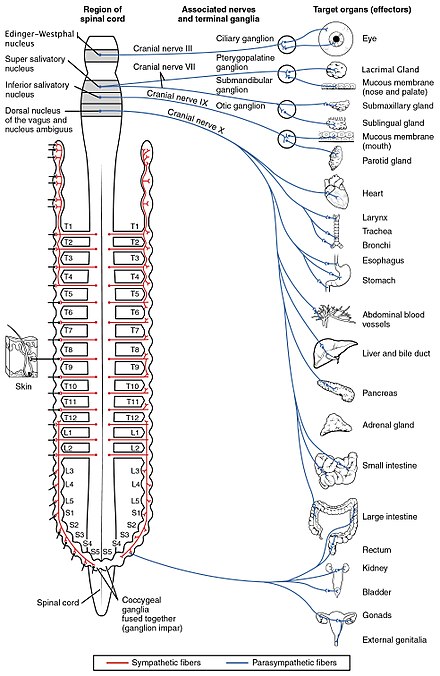
Вегетативная нервная система контролирует широкий спектр непроизвольных и бессознательных функций организма. Ее основными ветвями являются симпатическая нервная система и парасимпатическая нервная система . В широком смысле функция симпатической нервной системы заключается в мобилизации организма к действию; Для описания этого часто используют фразу « бей или беги» . Функция парасимпатической нервной системы заключается в том, чтобы привести организм в состояние, способствующее отдыху, регенерации, пищеварению и воспроизводству; для его описания часто используют фразу «отдыхать и переваривать» или «кормить и размножаться». Обе вышеупомянутые системы используют ацетилхолин, но по-разному.
На схематическом уровне симпатическая и парасимпатическая нервные системы организованы по существу одинаково: преганглионарные нейроны центральной нервной системы посылают проекции нейронам, расположенным в вегетативных ганглиях, которые посылают выходные проекции практически во все ткани тела. В обеих ветвях внутренние связи, проекции центральной нервной системы на вегетативные ганглии, используют ацетилхолин в качестве нейромедиатора для иннервации (или возбуждения) нейронов ганглиев. В парасимпатической нервной системе выходные соединения — отростки ганглиозных нейронов к тканям, не принадлежащим к нервной системе, также выделяют ацетилхолин, но действуют на мускариновые рецепторы. В симпатической нервной системе выходные соединения в основном выделяют норадреналин , хотя в некоторых точках, например, при судомоторной иннервации потовых желез, выделяется ацетилхолин.
Ацетилхолин в сыворотке оказывает прямое влияние на тонус сосудов путем связывания с мускариновыми рецепторами , присутствующими на эндотелии сосудов . Эти клетки реагируют увеличением выработки оксида азота , который сигнализирует окружающим гладким мышцам о необходимости расслабиться, что приводит к расширению сосудов . [12]

В центральной нервной системе АХ оказывает разнообразное влияние на пластичность, возбуждение и вознаграждение . АХ играет важную роль в повышении бдительности, когда мы просыпаемся, [13] в поддержании внимания [14] , а также в обучении и памяти. [15]
Было показано, что повреждение холинергической (продуцирующей ацетилхолин) системы головного мозга связано с дефицитом памяти, связанным с болезнью Альцгеймера . [16] Также было показано, что ACh способствует быстрому сну. [17]
В стволе мозга ацетилхолин образуется из педункулопонтинного ядра и латеродорсального покрышки, известных под общим названием мезопонтинная покрышка или понтомезэнцефалотегментальный комплекс. [18] [19] В базальном отделе переднего мозга он берет начало из базального ядра Мейнерта и медиального перегородочного ядра :
Кроме того, АХ действует как важный внутренний передатчик в полосатом теле , которое является частью базальных ганглиев . Он высвобождается холинергическими интернейронами . У людей, приматов и грызунов эти интернейроны реагируют на выраженные стимулы окружающей среды реакциями, которые по времени совпадают с реакциями дофаминергических нейронов черной субстанции . [20] [21]
Ацетилхолин участвует в обучении и памяти несколькими способами. Антихолинергический препарат скополамин ухудшает усвоение новой информации у людей [22] и животных. [15] У животных нарушение поступления ацетилхолина в неокортекс ухудшает обучение простым задачам распознавания, сравнимое с получением фактической информации [23], а нарушение поступления ацетилхолина в гиппокамп и прилегающие к нему области коры приводит к забывчивости, сравнимо с антероградной амнезией у человека. [24]
Заболевание миастения гравис , характеризующееся мышечной слабостью и утомляемостью, возникает, когда организм ненадлежащим образом вырабатывает антитела против никотиновых рецепторов ацетилхолина и, таким образом, подавляет правильную передачу сигнала ацетилхолина. Со временем концевая пластина двигателя разрушается. Препараты, конкурентно ингибирующие ацетилхолинэстеразу (например, неостигмин, физостигмин или прежде всего пиридостигмин), эффективны при лечении симптомов этого заболевания. Они дают эндогенно высвобождаемому ацетилхолину больше времени для взаимодействия с соответствующим рецептором, прежде чем он будет инактивирован ацетилхолинэстеразой в синаптической щели (пространстве между нервом и мышцей).
Блокирование, затруднение или имитация действия ацетилхолина имеет множество применений в медицине. Лекарственные средства, действующие на систему ацетилхолина, являются либо агонистами рецепторов, стимулирующих систему, либо антагонистами, ингибирующими ее. Агонисты и антагонисты ацетилхолиновых рецепторов могут либо оказывать действие непосредственно на рецепторы, либо оказывать свое действие опосредованно, например, воздействуя на фермент ацетилхолинэстеразу , которая разрушает лиганд рецептора. Агонисты повышают уровень активации рецепторов; антагонисты уменьшают его.
Сам по себе ацетилхолин не имеет терапевтической ценности как препарат для внутривенного введения из-за его многогранного действия (неселективности) и быстрой инактивации холинэстеразой. Однако его используют в виде глазных капель, чтобы вызвать сужение зрачка во время операции по удалению катаракты, что способствует быстрому послеоперационному восстановлению.
Никотин связывается с никотиновыми рецепторами ацетилхолина и активирует их, имитируя действие ацетилхолина на эти рецепторы. АХ открывает канал Na + при связывании, так что Na + поступает в клетку. Это вызывает деполяризацию и приводит к возникновению возбуждающего постсинаптического потенциала. Таким образом, АХ оказывает возбуждающее действие на скелетные мышцы; Электрический отклик быстрый и кратковременный. Кураре — это яд стрел, который действует на никотиновые рецепторы и использовался для разработки клинически полезных методов лечения.
Мускариновые рецепторы образуют рецепторные комплексы, связанные с G-белком, в клеточных мембранах нейронов и других клеток. Атропин является неселективным конкурентным антагонистом ацетилхолина мускариновых рецепторов.
Многие агонисты рецепторов ACh действуют косвенно, ингибируя фермент ацетилхолинэстеразу . Возникающее в результате накопление ацетилхолина вызывает постоянную стимуляцию мышц, желез и центральной нервной системы, что может привести к фатальным судорогам, если доза высока.
Они являются примерами ингибиторов ферментов и усиливают действие ацетилхолина, замедляя его распад; некоторые из них использовались в качестве нервно-паралитических агентов ( зарин и нервно-паралитический газ VX ) или пестицидов ( органофосфаты и карбаматы ). Многие токсины и яды, вырабатываемые растениями и животными, также содержат ингибиторы холинэстеразы. В клинической практике их применяют в низких дозах [ почему? ] для обратного действия миорелаксантов , для лечения миастении и лечения симптомов болезни Альцгеймера ( ривастигмин , который увеличивает холинергическую активность в головном мозге).
Органические соединения ртути , такие как метилртуть , обладают высоким сродством к сульфгидрильным группам , что вызывает дисфункцию фермента холин-ацетилтрансферазы. Это ингибирование может привести к дефициту ацетилхолина и иметь последствия для двигательной функции.
Ботулинический токсин (Ботокс) действует путем подавления высвобождения ацетилхолина, тогда как яд паука черной вдовы ( альфа-латротоксин ) имеет обратный эффект. Ингибирование АХ вызывает паралич . При укусе паука черной вдовы человек теряет запасы АХ, и мышцы начинают сокращаться. Если и когда запасы исчерпаны, наступает паралич .
Ацетилхолин используется организмами во всех сферах жизни для самых разных целей. Считается, что холин , предшественник ацетилхолина, использовался одноклеточными организмами миллиарды лет назад для синтеза фосфолипидов клеточных мембран. [25] После эволюции переносчиков холина обилие внутриклеточного холина открыло путь для включения холина в другие пути синтеза, включая производство ацетилхолина. Ацетилхолин используется бактериями, грибами и множеством других животных. Многие применения ацетилхолина основаны на его действии на ионные каналы через GPCR, такие как мембранные белки.
Два основных типа рецепторов ацетилхолина, мускариновые и никотиновые рецепторы, эволюционно эволюционировали и стали реагировать на ацетилхолин. Это означает, что эти рецепторы произошли не от общего гомолога, а из отдельных семейств рецепторов. Подсчитано, что семейство никотиновых рецепторов насчитывает более 2,5 миллиардов лет. [25] Аналогичным образом, считается, что мускариновые рецепторы отделились от других GPCR по крайней мере 0,5 миллиарда лет назад. Обе эти группы рецепторов развили множество подтипов с уникальным сродством к лигандам и механизмами передачи сигналов. Разнообразие типов рецепторов позволяет ацетилхолину вызывать различные реакции в зависимости от того, какие типы рецепторов активированы, и позволяет ацетилхолину динамически регулировать физиологические процессы. Рецепторы АХ родственны рецепторам 5-НТ3 ( серотонина ), ГАМК и глицина как по последовательности, так и по структуре, что убедительно свидетельствует о том, что они имеют общее эволюционное происхождение. [26]
В 1867 году Адольф фон Байер определил структуры холина и ацетилхолина и синтезировал их оба, назвав последний в своем исследовании « ацетилнейрином ». [27] [28] Холин является предшественником ацетилхолина. Вот почему Фредерик Уокер Мотт и Уильям Добинсон Халлибертон в 1899 году отметили, что инъекции холина снижают кровяное давление животных. [29] [28] Биологическая активность ацетилхолина была впервые отмечена в 1906 году, когда Рид Хант (1870–1948) и Рене де М. Таво обнаружили, что он снижает кровяное давление в исключительно малых дозах. [30] [28] [31]
В 1914 году Артур Дж. Юинс первым извлек ацетилхолин из природы. По просьбе Генри Халлетта Дейла он идентифицировал его как снижающий кровяное давление примесь из некоторых экстрактов спорыньи Claviceps purpurea . [28] Позже, в 1914 году, Дейл описал действие ацетилхолина на различные типы периферических синапсов, а также отметил, что он снижает кровяное давление кошек при подкожных инъекциях даже в дозах в один нанограмм . [32] [28]
Концепция нейротрансмиттеров была неизвестна до 1921 года, когда Отто Леви во время работы профессором в Университете Граца заметил, что блуждающий нерв секретирует вещество, которое ингибирует сердечную мышцу . Он назвал его vagusstoff («блуждающее вещество»), отметил, что это структурный аналог холина, и предположил, что это ацетилхолин. [33] [34] В 1926 году Лоуи и Э. Навратил пришли к выводу, что это соединение, вероятно, представляет собой ацетилхолин, поскольку вагустофф и синтетический ацетилхолин теряли свою активность аналогичным образом при контакте с лизатами тканей , которые содержали ферменты, разлагающие ацетилхолин (теперь известные как быть холинэстеразы ). [35] [36] Этот вывод был широко принят. Более поздние исследования подтвердили функцию ацетилхолина как нейромедиатора . [34]
В 1936 году Х. Х. Дейл и О. Лоуи получили Нобелевскую премию по физиологии и медицине за исследования ацетилхолина и нервных импульсов. [28]
Делирий связан только с антагонизмом постсинаптических рецепторов М1, и на сегодняшний день другие подтипы рецепторов не вовлечены.