В химии селективность связывания определяют по отношению к связыванию лигандов с субстратом , образующим комплекс . Селективность связывания описывает, как лиганд может более предпочтительно связываться с одним рецептором , чем с другим. Коэффициент селективности — это константа равновесия реакции замещения одним лигандом другого лиганда в комплексе с субстратом. Селективность связывания имеет большое значение в биохимии [1] и в процессах химического разделения .
Концепция селективности используется для количественной оценки степени, в которой одно химическое вещество A связывает каждое из двух других химических веществ, B и C. Самый простой случай - это когда образующиеся комплексы имеют стехиометрию 1: 1 . Тогда два взаимодействия можно охарактеризовать константами равновесия KAB и KAC . [примечание 1]
Коэффициент селективности определяется как отношение двух констант равновесия.
Легко показать, что то же самое определение применимо и к комплексам разной стехиометрии A p B q и A p C q . Чем больше коэффициент селективности, тем больше лиганд С будет вытеснять лиганд В из комплекса, образованного с субстратом А. Альтернативная интерпретация состоит в том, что чем больше коэффициент селективности, тем меньшая концентрация С необходима для вытеснения В из АВ. . Коэффициенты селективности определяются экспериментально путем измерения двух констант равновесия KAB и KAC .
В биохимии субстрат известен как рецептор. Рецептор — это белковая молекула, встроенная либо в плазматическую мембрану , либо в цитоплазму клетки, с которой могут связываться один или несколько конкретных типов сигнальных молекул. Лигандом может быть пептид или другая небольшая молекула, например нейромедиатор , гормон , фармацевтический препарат или токсин. Специфичность рецептора определяется его пространственной геометрией и способом его связывания с лигандом посредством нековалентных взаимодействий , таких как водородные связи или силы Ван-дер-Ваальса . [2]
Если рецептор можно выделить, можно разработать синтетический препарат либо для стимуляции рецептора ( агонист) , либо для его блокировки ( антагонист) . Лекарство от язвы желудка циметидин было разработано как антагонист H 2 путем химической инженерии молекулы для обеспечения максимальной специфичности к изолированной ткани, содержащей рецептор. Дальнейшее использование количественных соотношений структура-активность (QSAR) привело к разработке других агентов, таких как ранитидин .
Важно отметить, что «селективность» при упоминании лекарственного средства является относительной, а не абсолютной. Например, в более высокой дозе конкретная молекула лекарства может также связываться с другими рецепторами, кроме тех, которые считаются «селективными».
Хелатная терапия — это форма медицинского лечения, при которой хелатирующий лиганд [примечание 2] используется для избирательного удаления металла из организма. Когда металл существует в виде двухвалентного иона, например , свинца , Pb 2+ или ртути , селективность Hg 2+ по отношению к кальцию , Ca 2+ и магнию Mg 2+ важна для того, чтобы обработка не удаляла важные металлы. [3]
Селективность определяется различными факторами. В случае перегрузки железом , которая может возникнуть у людей с β- талессемией , получивших переливание крови , ион целевого металла находится в степени окисления +3 и поэтому образует более прочные комплексы, чем двухвалентные ионы. Он также образует более прочные комплексы с лигандами-донорами кислорода, чем с лигандами-донорами азота. дефероксамин , природный сидерофор , продуцируемый актинобактерией Streptomyces pilosus и первоначально использовавшийся в качестве агента хелатной терапии. Синтетические сидерофоры, такие как деферипрон и деферасирокс , были разработаны с использованием известной структуры дефероксамина в качестве отправной точки. [4] [5] Хелатирование происходит с двумя атомами кислорода.
Болезнь Вильсона вызвана нарушением метаболизма меди , что приводит к накоплению металлической меди в различных органах тела. Целевой ион в данном случае является двухвалентным Cu 2+ . Этот ион классифицируется как пограничный в схеме Арланда, Чатта и Дэвиса. [6] Это означает, что он образует примерно одинаково прочные комплексы с лигандами, донорными атомами которых являются N, O или F, и с лигандами, донорными атомами которых являются P, S или Cl. Пеницилламин , содержащий донорные атомы азота и серы, используется, поскольку этот тип лиганда сильнее связывается с ионами меди, чем с ионами кальция и магния.
Лечение отравлений тяжелыми металлами, такими как свинец и ртуть, более проблематично, поскольку используемые лиганды не обладают высокой специфичностью по отношению к кальцию. Например, ЭДТА можно применять в виде соли кальция, чтобы уменьшить удаление кальция из кости вместе с тяжелым металлом. Факторы, определяющие селективность свинца по отношению к цинку, кадмию и кальцию, были рассмотрены [7] .
При колоночной хроматографии смесь веществ растворяют в подвижной фазе и пропускают на колонке через неподвижную фазу. Фактор селективности определяется как соотношение коэффициентов распределения , которые описывают равновесное распределение аналита между неподвижной фазой и подвижной фазой. Коэффициент селективности равен коэффициенту селективности с добавленным предположением, что активность неподвижной фазы, в данном случае субстрата, равна 1, что является стандартным предположением для чистой фазы. [8] Разрешение хроматографической колонки RS связано с коэффициентом селективности следующим образом :
где α — коэффициент селективности, N — количество теоретических тарелок, k A и k B — коэффициенты удерживания двух аналитов. Коэффициенты удержания пропорциональны коэффициентам распределения. На практике можно разделить вещества с коэффициентом селективности, очень близким к 1. Это особенно актуально для газожидкостной хроматографии , где возможна длина колонки до 60 м, что обеспечивает очень большое количество теоретических тарелок.
В ионообменной хроматографии коэффициент селективности определяется несколько иначе [9]
Экстракцию растворителем [10] применяют для извлечения отдельных элементов лантаноидов из смесей, встречающихся в природе в таких рудах, как монацит . В одном процессе ионы металлов в водном растворе образуют комплексы с трибутилфосфатом (ТБФ), которые экстрагируются органическим растворителем, таким как керосин . Полное разделение достигается с помощью метода противоточного обмена . Ряд ячеек расположены каскадом . После уравновешивания водный компонент каждой ячейки переносится в предыдущую ячейку, а органический компонент переносится в следующую ячейку, которая изначально содержит только воду. Таким образом, ион металла с наиболее стабильным комплексом проходит вниз по каскаду в органической фазе, а металл с наименее стабильным комплексом проходит вверх по каскаду в водной фазе. [11]
Если растворимость в органической фазе не имеет значения, коэффициент селективности равен отношению констант устойчивости комплексов ТБФ двух ионов металлов. Для элементов-лантаноидов, соседних в таблице Менделеева, это соотношение не намного превышает 1, поэтому в каскаде необходимо много ячеек.
Коэффициент потенциометрической селективности определяет способность ионоселективного электрода отличать один конкретный ион от других. Коэффициент селективности K B,C оценивается посредством отклика ЭДС ионоселективного электрода в смешанных растворах первичного иона B и мешающего иона C (метод фиксированной интерференции) или, что менее желательно, в отдельных растворах B и C (метод раздельного решения). [12] Например, в мембранном электроде , селективном к ионам калия , используется встречающийся в природе макроциклический антибиотик валиномицин . В этом случае полость в макроциклическом кольце имеет правильный размер, чтобы инкапсулировать ион калия, но слишком велика, чтобы прочно связать ион натрия, что, скорее всего, является помехой.
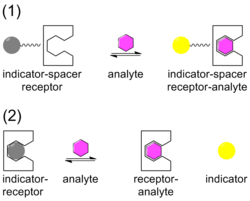
Химические сенсоры , [13] [14] разрабатываются для конкретных целевых молекул и ионов, в которых мишень (гость) образует комплекс с сенсором (хозяином). Датчик разработан таким образом, чтобы идеально соответствовать размеру и форме мишени, чтобы обеспечить максимальную селективность связывания. С датчиком связан индикатор, который претерпевает изменения, когда мишень образует комплекс с датчиком. Изменение индикатора обычно представляет собой изменение цвета (от серого до желтого на рисунке), наблюдаемое в оптической плотности или, при большей чувствительности, в люминесценции . Индикатор может быть прикреплен к датчику через проставку в исполнении ISR или может быть смещен от датчика в исполнении IDA.