Болезнь Вильсона — генетическое заболевание , при котором в организме накапливается избыток меди . Симптомы обычно связаны с мозгом и печенью . Симптомы, связанные с печенью, включают рвоту , слабость, скопление жидкости в животе , отеки ног , желтоватую кожу и зуд . Симптомы, связанные с мозгом, включают тремор , ригидность мышц, проблемы с речью, изменения личности, тревогу и психоз . [1]
Болезнь Вильсона вызвана мутацией гена белка болезни Вильсона ( ATP7B ) . Этот белок транспортирует избыток меди в желчь , где она выводится с отходами. Заболевание является аутосомно-рецессивным ; Чтобы люди пострадали, они должны унаследовать мутированную копию гена от обоих родителей. Диагностика может быть трудной и часто включает сочетание анализов крови, мочи и биопсии печени . Генетическое тестирование может использоваться для проверки членов семей заболевших. [1]
Болезнь Вильсона обычно лечат изменением диеты и приемом лекарств. Диетические изменения включают в себя диету с низким содержанием меди и отказ от использования медной посуды. Используемые лекарства включают хелатирующие агенты , такие как триентин и d-пеницилламин , а также добавки цинка . Осложнения болезни Вильсона могут включать печеночную недостаточность и проблемы с почками . Трансплантация печени может быть полезна тем, у кого другие методы лечения неэффективны или при возникновении печеночной недостаточности. [1]
Болезнь Вильсона встречается примерно у одного из 30 000 человек. [1] Симптомы обычно появляются в возрасте от 5 до 35 лет. [1] Впервые он был описан в 1854 году немецким патологом Фридрихом Теодором фон Фрерихсом и назван в честь британского невролога Сэмюэля Уилсона . [4]
Основными местами накопления меди являются печень и головной мозг , и, следовательно, заболевание печени и нервно-психические симптомы являются основными признаками, которые позволяют поставить диагноз. [5] Люди с проблемами печени, как правило, обращаются за медицинской помощью раньше, обычно в детстве или подростковом возрасте, чем люди с неврологическими и психиатрическими симптомами, которым обычно около 20 лет и старше. Некоторые из них выявляются только потому, что у родственников была диагностирована болезнь Вильсона; При тестировании у многих из них выяснилось, что у них наблюдаются симптомы этого заболевания, но им не поставили диагноз. [6]
Заболевания печени могут проявляться усталостью , желтухой , [7] повышенной склонностью к кровотечениям или спутанностью сознания (из-за печеночной энцефалопатии ) и портальной гипертензией . Последнее состояние, при котором давление в воротной вене заметно повышается, приводит к варикозному расширению вен пищевода , кровеносным сосудам пищевода , которые могут кровоточить опасным для жизни образом, а также к увеличению селезенки ( спленомегалии ) и накоплению жидкость в брюшной полости ( асцит ). При осмотре могут наблюдаться признаки хронического заболевания печени, такие как паукообразные ангиомы (небольшие расширенные кровеносные сосуды, обычно на груди). Хронический активный гепатит в большинстве случаев вызывает цирроз печени к моменту появления симптомов. Хотя у большинства людей с циррозом печени повышен риск развития гепатоцеллюлярной карциномы (рака печени), при болезни Вильсона этот риск относительно очень низок. [5]
Около 5% всех людей диагностируют только тогда, когда у них развивается молниеносная острая печеночная недостаточность , часто на фоне гемолитической анемии (анемии вследствие разрушения эритроцитов). Это приводит к нарушениям в производстве белка (определяемом по нарушению коагуляции ) и метаболизме в печени. Нарушение белкового обмена приводит к накоплению в кровотоке продуктов жизнедеятельности, таких как аммиак . Когда они раздражают мозг, у человека развивается печеночная энцефалопатия (путаница сознания, кома, судороги и, наконец, опасный для жизни отек мозга ). [5]

Около половины людей с болезнью Вильсона имеют неврологические или психиатрические симптомы. У большинства изначально наблюдаются легкие когнитивные нарушения и неуклюжесть, а также изменения в поведении. Затем обычно следуют специфические неврологические симптомы, часто в виде паркинсонизма (наиболее распространенными признаками паркинсонизма являются ригидность зубчатого колеса, брадикинезия или замедление движений и отсутствие равновесия [8] ) с типичным тремором рук или без него , замаскированной мимикой, невнятностью и невнятностью. речь, атаксия (нарушение координации) или дистония (скручивание и повторяющиеся движения частей тела). Судороги и мигрень, по-видимому, более распространены при болезни Вильсона. [5] Характерный тремор, описываемый как «тремор взмахов крыльев», встречается у многих людей с синдромом Вильсона; в покое оно отсутствует, но может быть спровоцировано отведением рук и сгибанием локтей к средней линии. [9]
Познавательные способности также могут быть нарушены при болезни Вильсона в двух, не исключающих друг друга, категориях: расстройство лобных долей (может проявляться как импульсивность , нарушение суждений, распущенность , апатия и исполнительная дисфункция с плохим планированием и принятием решений) и подкорковая деменция (может проявляется замедленным мышлением, потерей памяти и исполнительной дисфункцией без признаков афазии , апраксии или агнозии ). Считается, что эти когнитивные нарушения связаны и тесно связаны с психиатрическими проявлениями заболевания. [8]
Психиатрические проблемы, связанные с болезнью Вильсона, могут включать изменения в поведении, депрессию , тревожные расстройства и психоз . [5] Психиатрические симптомы обычно наблюдаются в сочетании с неврологическими симптомами и редко проявляются сами по себе. Эти симптомы часто плохо выражены и иногда могут быть связаны с другими причинами. По этой причине диагноз болезни Вильсона редко ставится при наличии только психиатрических симптомов. [8]
Заболевания связаны с накоплением меди при болезни Вильсона:

Ген болезни Вильсона ( ATP7B ) находится на хромосоме 13 (13q14.3) и экспрессируется преимущественно в печени, почках и плаценте . Ген кодирует АТФазу Р -типа (фермент транспорта катионов) , которая транспортирует медь в желчь и включает ее в церулоплазмин . [5] Мутации можно обнаружить в 90% случаев. Большинство (60%) гомозиготны по мутациям ATP7B (две аномальные копии), а 30% имеют только одну аномальную копию. Около 10% не имеют обнаруживаемой мутации. [6]
Хотя описано 300 мутаций ATP7B , в большинстве популяций случаи болезни Вильсона обусловлены небольшим количеством мутаций, специфичных для этой популяции. Например, в западных популяциях мутация H1069Q (замена гистидина глютамином в положении 1069 белка) присутствует в 37–63% случаев, тогда как в Китае эта мутация встречается очень редко и R778L ( аргинин в лейцин на 778) встречается чаще. Относительно мало известно об относительном влиянии различных мутаций, хотя, согласно некоторым исследованиям, мутация H1069Q, по-видимому, предсказывает более позднее начало и преимущественно неврологические проблемы. [5] [15] WilsonGen — всеобъемлющий клинически аннотированный ресурс, предоставляющий клиническую классификацию вариантов в соответствии с недавними рекомендациями ACMG и AMP [16].
Нормальная вариация гена PRNP может изменить течение заболевания, задерживая возраст начала заболевания и влияя на тип развивающихся симптомов. Этот ген производит прионный белок , который активен в мозге и других тканях, а также, по-видимому, участвует в транспортировке меди. [17] Роль гена ApoE первоначально подозревалась, но не могла быть подтверждена. [15]
Заболевание наследуется по аутосомно-рецессивному типу. Чтобы унаследовать его, оба родителя человека должны нести пораженный ген. У большинства из них нет семейной истории этого заболевания. [15] Люди только с одним аномальным геном называются носителями (гетерозиготами) и могут иметь легкие, но незначимые с медицинской точки зрения нарушения метаболизма меди. [14]
Болезнь Вильсона — наиболее распространенная из группы наследственных заболеваний, вызывающих перегрузку медью в печени. Все они могут вызвать цирроз печени в молодом возрасте. Другими членами группы являются индийский детский цирроз печени (ИКЦ), эндемический тирольский детский цирроз печени и идиопатический токсикоз меди. Они не связаны с мутациями ATP7B ; например, ICC связан с мутациями в генах KRT8 и KRT18 . [15]

Медь необходима организму для ряда функций , преимущественно в качестве кофактора для ряда ферментов, таких как церулоплазмин, цитохром с-оксидаза , дофамин-β-гидроксилаза , супероксиддисмутаза и тирозиназа . [15]
Медь попадает в организм через пищеварительный тракт . Белок-транспортер на клетках тонкой кишки , мембранный транспортер меди 1 (Ctr1; SLC31A1), переносит медь внутрь клеток, где некоторая ее часть связывается с металлотионеином , а часть переносится с помощью ATOX1 в органеллу, известную как транс-сеть Гольджи . Здесь, в ответ на повышение концентрации меди, фермент под названием ATP7A (белок Менкеса) высвобождает медь в воротную вену печени. Клетки печени также несут белок CMT1, а металлотионеин и ATOX1 связывают его внутри клетки, но здесь ATP7B связывает медь с церулоплазмином и высвобождает ее в кровоток, а также удаляет избыток меди, секретируя ее в желчь. Обе функции ATP7B нарушаются при болезни Вильсона. Медь накапливается в ткани печени; Церулоплазмин все еще секретируется, но в форме, в которой отсутствует медь (называемой апоцерулоплазмин), и она быстро разлагается в кровотоке. [15]
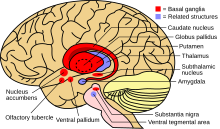
Когда количество меди в печени превышает количество белков, которые обычно связывают ее, это вызывает окислительное повреждение в результате процесса, известного как химия Фентона ; это повреждение в конечном итоге приводит к хроническому активному гепатиту , фиброзу (отложению соединительной ткани) и циррозу печени . Печень также выделяет в кровоток медь, не связанную с церулоплазмином. Эта свободная медь осаждается по всему телу, но особенно в почках, глазах и мозге. В головном мозге большая часть меди откладывается в базальных ганглиях , особенно в скорлупе и бледном шаре (вместе называемых чечевицеобразным ядром ); эти области обычно участвуют в координации движений и играют значительную роль в нейрокогнитивных процессах, таких как обработка стимулов и регуляция настроения. Повреждение этих областей, опять же химическим действием Фентона, вызывает нейропсихиатрические симптомы, наблюдаемые при болезни Вильсона. [15]
Почему болезнь Вильсона вызывает гемолиз, неясно, но различные данные свидетельствуют о том, что высокий уровень свободной (несвязанной с церулоплазмином) меди оказывает прямое влияние либо на окисление гемоглобина , ингибирование энергоснабжающих ферментов в эритроцитах , либо прямое влияние. повреждение клеточных мембран . [18]
Заподозрить болезнь Вильсона можно на основании любого из симптомов, упомянутых выше, или при обнаружении болезни Вильсона у близкого родственника. У большинства из них наблюдаются незначительные отклонения в функциональных показателях печени , такие как повышение уровня аспартатаминотрансферазы , аланинаминотрансферазы и билирубина . Если повреждение печени существенное, уровень альбумина может снизиться из-за неспособности поврежденных клеток печени вырабатывать этот белок; аналогичным образом, протромбиновое время (тест коагуляции ) может быть увеличено, поскольку печень не способна вырабатывать белки, известные как факторы свертывания крови. [5] Уровни щелочной фосфатазы относительно низкие у пациентов с острой печеночной недостаточностью, связанной с синдромом Вильсона. [19] Если наблюдаются неврологические симптомы, обычно проводят магнитно-резонансную томографию головного мозга; это показывает гиперинтенсивность в части мозга, называемой базальными ганглиями, в режиме Т2 . [14] МРТ также может демонстрировать характерный рисунок «лица большой панды» . [20]
Полностью надежных тестов на болезнь Вильсона не известно, но уровни церулоплазмина и меди в крови, а также количество меди, выделяемой с мочой в течение 24 часов, вместе используются для формирования впечатления о количестве меди в крови. тело. Золотой стандарт – или самый идеальный тест – это биопсия печени . [5]

Уровни церулоплазмина аномально низкие (<0,2 г/л) в 80–95% случаев. [5] Однако он может присутствовать на нормальном уровне у людей с продолжающимся воспалением , поскольку это белок острой фазы . Низкий уровень церулоплазмина также обнаруживается при болезни Менкеса и ацерулоплазминемии , которые родственны, но гораздо реже, чем болезнь Вильсона. [5] [14] Сочетание неврологических симптомов, глазных признаков и низкого уровня церулоплазмина считается достаточным для диагностики болезни Вильсона. Однако во многих случаях необходимы дополнительные тесты. [14]
В сыворотке крови низкий уровень меди, что может показаться парадоксальным, учитывая, что болезнь Вильсона – это болезнь избытка меди. Однако 95% меди плазмы переносится церулоплазмином, уровень которого при болезни Вильсона часто бывает низким. Медь в моче повышается при болезни Вильсона, и ее собирают в течение 24 часов в бутыль с вкладышем, не содержащим меди. Уровни выше 100 мкг/24 часа (1,6 мкмоль/24 часа) подтверждают болезнь Вильсона, а уровни выше 40 мкг/24 часа (0,6 мкмоль/24 часа) являются строго показательными. [5] Высокий уровень меди в моче характерен не только для болезни Вильсона; их иногда наблюдают при аутоиммунном гепатите и при холестазе (любом заболевании, препятствующем оттоку желчи из печени в тонкую кишку). [14]
У детей можно использовать тест на пеницилламин . Вводят перорально 500 мг пеницилламина и собирают мочу в течение 24 часов. Если он содержит более 1600 мкг (25 мкмоль), это надежный индикатор болезни Вильсона. [ нужны разъяснения ] Этот тест не был проверен на взрослых. [14]
Глаза пациента исследуют с помощью щелевой лампы для поиска колец Кайзера-Флейшера , которые тесно связаны с болезнью Вильсона и вызваны отложением меди на внутренней поверхности роговицы в десцеметовой мембране . [10]
Если другие исследования выявили болезнь Вильсона, идеальным тестом является удаление небольшого количества ткани печени посредством биопсии печени. Это оценивается микроскопически на предмет степени стеатоза и цирроза печени, а гистохимия и количественный анализ меди используются для измерения тяжести накопления меди. Уровень 250 мкг меди на грамм высушенной ткани печени подтверждает болезнь Вильсона. Иногда обнаруживаются более низкие уровни меди; в этом случае сочетание результатов биопсии со всеми другими тестами все равно может привести к официальному диагнозу болезни Вильсона. [5]
На более ранних стадиях заболевания биопсия обычно показывает стеатоз (отложение жирового материала), увеличение гликогена в ядре и участки некроза (гибель клеток). На более поздних стадиях заболевания наблюдаемые изменения весьма аналогичны тем, которые наблюдаются при аутоиммунном гепатите, например, инфильтрация воспалительными клетками, частичный некроз и фиброз (рубцовая ткань). Наконец, при поздних стадиях заболевания основным признаком является цирроз печени. При острой печеночной недостаточности наблюдается дегенерация клеток печени и коллапс архитектуры печеночной ткани, обычно на фоне цирротических изменений. Гистохимические методы обнаружения меди противоречивы и ненадежны, а сами по себе считаются недостаточными для установления диагноза. [14]
Можно провести мутационный анализ гена ATP7B , а также других генов, связанных с накоплением меди в печени. После подтверждения мутации члены семьи могут пройти обследование на наличие заболевания в рамках семейного консультирования по клинической генетике . [5] Важно следить за региональным распределением генов, связанных с болезнью Вильсона, поскольку это может помочь врачам разработать соответствующие стратегии скрининга. Поскольку мутации гена ATP7B различаются в разных популяциях, исследования и генетические тесты, проводимые в таких странах, как США или Великобритания, могут создавать проблемы, поскольку в них, как правило, более смешанные популяции. [21]
В целом рекомендуется диета с низким содержанием медьсодержащих продуктов, избегая грибов , орехов , шоколада , сухофруктов , печени, семян кунжута и кунжутного масла, а также моллюсков . [5]
Для лечения болезни Вильсона доступны медицинские методы лечения. Некоторые увеличивают выведение меди из организма, а другие препятствуют усвоению меди из рациона.
Обычно пеницилламин используется в первую очередь. Это связывает медь ( хелатирование ) и приводит к выведению меди с мочой. Следовательно, можно контролировать количество меди в моче, чтобы убедиться, что принята достаточно высокая доза. Пеницилламин не без проблем; около 20% испытывают побочные эффекты или осложнения лечения пеницилламином, такие как лекарственная волчанка (вызывающая боли в суставах и кожную сыпь) или миастения (нервное заболевание, приводящее к мышечной слабости). У тех, у кого наблюдались неврологические симптомы, почти у половины наблюдалось парадоксальное ухудшение симптомов. Хотя это явление наблюдается и при других методах лечения синдрома Вильсона, оно обычно рассматривается как показание к отмене пеницилламина и началу лечения второй линии. [5] [14] При непереносимости пеницилламина вместо этого можно начать прием триентина гидрохлорида , который также обладает хелатирующими свойствами. Некоторые рекомендуют триентин в качестве лечения первой линии, но опыт применения пеницилламина более обширен. [14] Еще одним агентом, находящимся в стадии клинических исследований Wilson Therapeutics , с известной активностью при болезни Вильсона, является тетратиомолибдат . Это считается экспериментальным, [14] хотя некоторые исследования показали положительный эффект. [5]
Как только все результаты вернутся к норме, цинк (обычно в виде рецепта на ацетат цинка под названием Галзин) можно использовать вместо хелаторов для поддержания стабильного уровня меди в организме. Цинк стимулирует металлотионеин , белок в клетках кишечника, который связывает медь и предотвращает ее всасывание и транспортировку в печень. Терапию цинком продолжают до тех пор, пока симптомы не возобновятся или если не увеличится выведение меди с мочой. [14]
В редких случаях, когда ни один из пероральных препаратов не эффективен, особенно при тяжелых неврологических заболеваниях, иногда необходим димеркапрол (британский антилюизит). Это лечение вводится внутримышечно (в мышцу) каждые несколько недель и имеет неприятные побочные эффекты, такие как боль. [22]
Людей, у которых нет симптомов (например, тех, у кого диагноз был диагностирован в ходе семейного скрининга или только в результате аномальных результатов анализов), обычно лечат, поскольку накопление меди может вызвать долгосрочный ущерб в будущем. Неясно, лучше ли этих людей лечить пеницилламином или ацетатом цинка. [14]
Больным с неврологической формой заболевания полезны физиотерапия и эрготерапия. Лечение медь-хелатированием может занять до шести месяцев, чтобы начать действовать, и эти методы лечения могут помочь справиться с атаксией , дистонией и тремором, а также предотвратить развитие контрактур , которые могут возникнуть в результате дистонии. [23]
Трансплантация печени является эффективным методом лечения болезни Вильсона, но используется только в определенных случаях из-за рисков и осложнений, связанных с этой процедурой. Он используется в основном у людей с фульминантной печеночной недостаточностью, которые не реагируют на медикаментозное лечение, или у людей с запущенным хроническим заболеванием печени. Трансплантации печени избегают при тяжелых нервно-психических заболеваниях, при которых ее польза не доказана. [5] [14]
При отсутствии лечения болезнь Вильсона имеет тенденцию прогрессировать и в конечном итоге приводит к летальному исходу. Серьезные осложнения включают цирроз печени, острую почечную недостаточность и психоз. Могут возникнуть рак печени и холангиокарцинома , но они встречаются реже, чем другие хронические заболевания печени, и риск значительно снижается при лечении. [13] При раннем выявлении и лечении большинство пострадавших могут жить относительно нормальной жизнью и иметь ожидаемую продолжительность жизни, близкую к продолжительности жизни населения в целом. [13] Повреждения печени и неврологические нарушения, возникшие до лечения, могут улучшиться, но зачастую они остаются необратимыми. [24] Фертильность обычно нормальная, а осложнения беременности не увеличиваются у женщин с болезнью Вильсона, которую лечат. [13]
Заболевание носит имя британского врача Сэмюэля Александра Киннера Уилсона (1878–1937), невролога , который описал это состояние, включая патологические изменения в мозге и печени, в 1912 году . далее, сообщения немецкого невролога Карла Вестфаля (в 1883 г.), который назвал это заболевание «псевдосклерозом»; британский невролог Уильям Гауэрс (в 1888 г.); [26] финский невропатолог Эрнст Александр Хомен (в 1889–1892 гг.), отмечавший наследственный характер заболевания; [27] и Адольфом Стрюмпелем (в 1898 г.), отметившим цирроз печени. [26] Невропатолог Джон Натаниэль Камингс установил связь с накоплением меди как в печени, так и в мозге в 1948 году. [28] Возникновение гемолиза было отмечено в 1967 году. [29]
В 1951 году Камингс и новозеландский невролог Дерек Денни-Браун , работавший в США, одновременно сообщили о первом эффективном лечении с использованием хелатора металлов британского антилюизита . [30] [31] Это лечение должно было быть инъекционным, но оно было одним из первых методов лечения, доступных в области неврологии, области, которая классически могла наблюдать и диагностировать, но предлагала мало методов лечения. [26] [32] Первый эффективный пероральный хелатирующий агент, пеницилламин , был открыт в 1956 году британским неврологом Джоном Уолшем. [33] В 1982 году Уолш также представил триентин [34] и был первым, кто разработал тетратиомолибдат для клинического использования. [35] Терапия ацетатом цинка первоначально появилась в Нидерландах, где врачи Шувинк и Хугенраад использовали ее в 1961 и 1970-х годах соответственно, но позже она была развита Брюером и коллегами из Мичиганского университета . [22] [36]
Генетическая основа болезни Вильсона и ее связь с мутациями ATP7B были выяснены несколькими исследовательскими группами в 1980-х и 1990-х годах. [37] [38]
Наследственное накопление меди было описано у бедлингтон-терьеров [39] , где оно обычно поражает только печень. Это связано с мутациями в гене COMMD1 (или MURR1 ). [40] Несмотря на эти результаты, мутации COMMD1 не могут быть обнаружены у людей с невильсоновскими состояниями накопления меди (такими как индийский детский цирроз печени ), чтобы объяснить их генетическое происхождение. [41]