Никель -кадмиевая батарея ( Ni-Cd батарея или NiCad батарея ) — это тип аккумуляторной батареи , в которой в качестве электродов используется гидроксид оксида никеля и металлический кадмий . Аббревиатура Ni–Cd происходит от химических символов никеля (Ni) и кадмия ( Cd ): аббревиатура NiCad является зарегистрированной торговой маркой SAFT Corporation , хотя эта торговая марка обычно используется для описания всех Ni–Cd аккумуляторов.
Никель -кадмиевые батареи с мокрыми элементами были изобретены в 1899 году. Никель-кадмиевые батареи имеют напряжение на клеммах во время разряда около 1,2 В, которое мало снижается почти до конца разряда. Максимальная электродвижущая сила , создаваемая никель-кадмиевым элементом, составляет 1,3 В. Ni-Cd батареи производятся в широком диапазоне размеров и емкостей: от портативных герметичных типов, взаимозаменяемых с сухими углеродно-цинковыми элементами, до больших вентилируемых элементов, используемых для резервного питания. и движущая сила. По сравнению с другими типами перезаряжаемых элементов они обеспечивают хороший срок службы и производительность при низких температурах с достаточной емкостью, но их существенным преимуществом является способность обеспечивать практически полную номинальную емкость при высоких скоростях разряда (разрядка за один час или меньше). Однако материалы дороже, чем у свинцово-кислотных аккумуляторов , а элементы имеют высокую скорость саморазряда.
Герметичные Ni–Cd элементы когда-то широко использовались в портативных электроинструментах, фотооборудовании, фонариках , аварийном освещении, радиоуправляемых устройствах для хобби и портативных электронных устройствах. Превосходная емкость никель-металлогидридных батарей и недавняя более низкая стоимость в значительной степени вытеснили использование Ni-Cd. Кроме того, воздействие утилизации токсичного металлического кадмия на окружающую среду в значительной степени способствовало сокращению его использования. В пределах Европейского Союза Ni–Cd аккумуляторы теперь могут поставляться только для замены или для определенных типов нового оборудования, например медицинского оборудования. [2]
Ni-Cd батареи с мокрыми элементами с вентиляцией большего размера используются в аварийном освещении, резервном питании, источниках бесперебойного питания и других приложениях.
Первая Ni-Cd батарея была создана Вальдемаром Юнгнером из Швеции в 1899 году. В то время единственным прямым конкурентом была свинцово-кислотная батарея , которая была менее физически и химически прочной. После незначительных усовершенствований первых прототипов плотность энергии быстро увеличилась примерно до половины от плотности энергии первичных батарей и значительно превысила плотность свинцово-кислотных батарей. Юнгнер экспериментировал с заменой кадмия железом в различных количествах, но обнаружил, что составов железа не хватает. Работа Юнгнера была практически неизвестна в Соединенных Штатах. Томас Эдисон запатентовал никель- или кобальт-кадмиевую батарею в 1902 году [3] и адаптировал ее конструкцию, когда представил никель-железную батарею в США через два года после того, как Юнгнер построил ее. В 1906 году Юнгнер основал завод недалеко от Оскарсхамна, Швеция, по производству никель-кадмиевых аккумуляторов затопленной конструкции.
В 1932 году активные материалы были осаждены внутри пористого никелированного электрода, а пятнадцать лет спустя начались работы над герметичной никель-кадмиевой батареей.
Первое производство в Соединенных Штатах началось в 1946 году. До этого момента батареи были «карманного типа», состоящими из карманов из никелированной стали, содержащих активные материалы никеля и кадмия . Примерно в середине двадцатого века никель-кадмиевые аккумуляторы со спеченными пластинами становились все более популярными. Сплавление никелевого порошка при температуре значительно ниже его точки плавления и под высоким давлением позволяет получить спеченные пластины. Сформированные таким образом пластины имеют высокую пористость, около 80 процентов по объему. Положительные и отрицательные пластины изготавливаются путем пропитки никелевых пластин активными никелем и кадмием материалами соответственно. Спеченные пластины обычно намного тоньше пластин карманного типа, что приводит к большей площади поверхности на единицу объема и более высоким токам. В общем, чем больше площадь поверхности реактивного материала в батарее, тем ниже ее внутреннее сопротивление .
С 2000-х годов все потребительские Ni-Cd аккумуляторы имеют желейную форму. [ нужна цитата ]
Максимальная скорость разряда Ni–Cd аккумулятора зависит от его размера. Для обычного элемента размера AA максимальная сила разряда составляет примерно 1,8 ампер; для батареи размера D скорость разряда может достигать 3,5 ампер. [ нужна цитата ]
Производители моделей самолетов и лодок часто потребляют гораздо большие токи, до ста ампер или около того, от специально сконструированных никель-кадмиевых батарей, которые используются для привода главных двигателей. 5–6 минут работы модели легко достижимы от достаточно небольших аккумуляторов, благодаря чему достигается достаточно высокий показатель удельной мощности, сравнимый с двигателями внутреннего сгорания , хотя и меньшей продолжительности работы. Однако в этом отношении их в значительной степени вытеснили литий-полимерные (LiPo) и литий-железо-фосфатные батареи (LiFe), которые могут обеспечивать еще более высокую плотность энергии.
Ni-Cd элементы имеют номинальный потенциал элемента 1,2 вольта (В). Это ниже, чем 1,5 В щелочных и углеродно-цинковых первичных элементов, и, следовательно, они не подходят в качестве замены во всех приложениях. Однако напряжение 1,5 В первичного щелочного элемента относится к его начальному, а не среднему напряжению. В отличие от щелочных и цинк-углеродных первичных элементов, напряжение на клеммах Ni-Cd элемента меняется лишь незначительно по мере его разряда. Поскольку многие электронные устройства предназначены для работы с первичными элементами, которые могут разряжаться до уровня от 0,90 до 1,0 В на ячейку, относительно стабильного напряжения 1,2 В никель-кадмиевого элемента достаточно для работы. Некоторые сочтут почти постоянное напряжение недостатком, поскольку из-за него трудно обнаружить низкий заряд батареи.
Ni-Cd батареи, используемые для замены батарей на 9 В, обычно имеют только шесть ячеек с напряжением на клеммах 7,2 В. Хотя большинство карманных радиоприемников будут удовлетворительно работать при этом напряжении, некоторые производители, такие как Varta, создали семиэлементные батареи на 8,4 В для более важных приложений.
Ni-Cd аккумуляторы можно заряжать с разной скоростью, в зависимости от того, как был изготовлен элемент. Скорость заряда измеряется на основе процентной доли емкости в ампер-часах, на которую подается постоянный ток в течение всего времени зарядки. Независимо от скорости зарядки, в аккумулятор должно подаваться больше энергии, чем его фактическая емкость, чтобы учесть потери энергии во время зарядки, причем более быстрая зарядка более эффективна. Например, «ночная» зарядка может состоять из подачи тока, равного одной десятой номинального значения ампер-часа (C / 10), в течение 14–16 часов; то есть аккумулятор емкостью 100 мАч потребляет ток 10 мА в течение 14 часов, всего для зарядки с такой скоростью получается 140 мАч. При скорости быстрой зарядки, выполняемой при 100 % номинальной емкости аккумулятора за 1 час (1С), аккумулятор удерживает примерно 80 % заряда, поэтому для зарядки аккумулятора емкостью 100 мАч требуется 125 мАч (то есть примерно 1 час пятнадцать минут). Некоторые специализированные аккумуляторы можно заряжать всего за 10–15 минут при скорости зарядки 4C или 6C, но это случается очень редко. Это также значительно увеличивает риск перегрева и вентиляции элементов из-за внутреннего избыточного давления: скорость повышения температуры элемента определяется его внутренним сопротивлением и квадратом скорости зарядки. При скорости 4С количество тепла, выделяемого в ячейке, в шестнадцать раз превышает количество тепла при скорости 1С. Обратной стороной более быстрой зарядки является более высокий риск перезарядки , которая может повредить аккумулятор. и повышенные температуры, которые приходится выдерживать клетке (что потенциально сокращает ее жизнь).
Безопасный диапазон температур при использовании составляет от −20 °C до 45 °C. Во время зарядки температура аккумулятора обычно остается низкой, примерно такой же, как температура окружающей среды (реакция зарядки поглощает энергию), но по мере того, как аккумулятор приближается к полной зарядке, температура повышается до 45–50 °C. Некоторые зарядные устройства обнаруживают это повышение температуры, чтобы прекратить зарядку и предотвратить чрезмерную зарядку.
Когда никель-кадмиевый аккумулятор не находится под нагрузкой и не заряжается, он саморазряжается примерно на 10 % в месяц при температуре 20 °C и до 20 % в месяц при более высоких температурах. Примечание; В 2022 году предыдущее предложение, безусловно, было верным, когда был представлен NiCad, и даже 50 лет назад. Однако продолжающиеся улучшения, наблюдаемые около 40 лет назад, привели к 5% в месяц, а сегодня NiCad-аккумуляторы имеют значительно более низкий саморазряд, порядка 1% или 2% в месяц. Можно выполнить капельный заряд при уровнях тока, достаточно высоких, чтобы компенсировать эту скорость разряда; чтобы аккумулятор оставался полностью заряженным. Однако, если аккумулятор будет храниться неиспользованным в течение длительного периода времени, его следует разряжать максимум до 40% емкости (некоторые производители рекомендуют полностью разряжать и даже закорачивать после полной разрядки [ нужна ссылка ] ), и хранить в прохладном, сухом месте.
Герметичные Ni-Cd элементы состоят из сосуда под давлением, который должен содержать любое количество газов кислорода и водорода до тех пор, пока они не смогут рекомбинироваться обратно в воду. Такое генерирование обычно происходит во время быстрой зарядки и разрядки, а особенно в условиях перезаряда. Если давление превышает предел срабатывания предохранительного клапана, вода в виде газа теряется. Поскольку сосуд предназначен для содержания точного количества электролита, эта потеря быстро повлияет на емкость элемента и его способность получать и передавать ток. Чтобы обнаружить все условия перезаряда, требуется большая сложность схемы зарядки, а дешевое зарядное устройство в конечном итоге повредит даже самые качественные аккумуляторы. [4]
Полностью заряженный Ni-Cd элемент содержит:
Ni–Cd аккумуляторы обычно имеют металлический корпус с уплотнительной пластиной, оснащенной самоуплотняющимся предохранительным клапаном . Пластины положительного и отрицательного электрода, изолированные друг от друга сепаратором, свернуты внутри корпуса по спирали. Это известно как конструкция с желейными валками и позволяет никель-кадмиевому элементу обеспечивать гораздо более высокий максимальный ток, чем щелочной элемент эквивалентного размера. Щелочные элементы имеют катушечную конструкцию, в которой корпус элемента заполнен электролитом и содержит графитовый стержень, который действует как положительный электрод. Поскольку относительно небольшая площадь электрода контактирует с электролитом (в отличие от конструкции с желеобразными валками), внутреннее сопротивление щелочной ячейки эквивалентного размера выше, что ограничивает максимальный ток, который может быть доставлен.
Химические реакции на кадмиевом электроде во время разряда:
На оксидноникелевом электроде происходят следующие реакции:
Суммарная реакция во время разряда равна
Во время перезарядки реакции идут справа налево. Щелочной электролит (обычно КОН) не расходуется в этой реакции, и поэтому его удельный вес , в отличие от свинцово-кислотных аккумуляторов, не является показателем состояния его заряда.
Когда Юнгнер создал первые Ni-Cd батареи, он использовал оксид никеля в положительном электроде, а материалы из железа и кадмия — в отрицательном. Лишь позже стали использовать чистый металлический кадмий и гидроксид никеля. Примерно до 1960 года химическая реакция не была полностью понята. Было несколько предположений относительно продуктов реакции. Окончательно спор разрешился с помощью инфракрасной спектроскопии , которая выявила гидроксид кадмия и гидроксид никеля.
Другой исторически важной вариацией базового Ni-Cd элемента является добавление гидроксида лития к электролиту гидроксида калия. В это верили [ кем? ] для продления срока службы, делая элемент более устойчивым к электрическому воздействию. В любом случае Ni–Cd аккумулятор в его современном виде чрезвычайно устойчив к злоупотреблениям электрическим током, поэтому эта практика была прекращена.

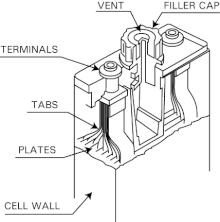
Никель-кадмиевые аккумуляторы с вентилируемыми элементами ( мокрые элементы , затопленные элементы ) используются, когда требуются большие емкости и высокие скорости разряда. Обычные никель-кадмиевые аккумуляторы относятся к герметичному типу, что означает, что зарядный газ обычно рекомбинируется и они не выделяют газ, если только они не сильно перезаряжены или не возникнет неисправность. В отличие от типичных никель-кадмиевых элементов, которые герметичны, вентилируемые элементы имеют вентиляционный клапан или клапан сброса низкого давления , который выпускает образующиеся газообразные кислород и водород при чрезмерной зарядке или быстрой разрядке. Поскольку аккумулятор не является сосудом под давлением , он безопаснее, весит меньше и имеет более простую и экономичную конструкцию. Это также означает, что батарея обычно не повреждается из-за чрезмерной перезарядки, разрядки или даже отрицательного заряда.
Они используются в авиации, железнодорожном и общественном транспорте, резервном питании для телекоммуникаций, запуске двигателей резервных турбин и т. д. Использование никель-кадмиевых батарей с вентилируемыми элементами приводит к уменьшению размеров, веса и требований к техническому обслуживанию по сравнению с другими типами батарей. Ni-Cd аккумуляторы с вентилируемыми элементами имеют длительный срок службы (до 20 лет и более, в зависимости от типа) и работают при экстремальных температурах (от –40 до 70 °C).
Стальной аккумуляторный ящик содержит элементы, соединенные последовательно для получения желаемого напряжения (номинальное 1,2 В на элемент). Элементы обычно изготавливаются из легкого и прочного полиамида ( нейлона ) с несколькими сваренными между собой никель-кадмиевыми пластинами для каждого электрода внутри. Сепаратор или вкладыш из силиконовой резины действует как изолятор и газовый барьер между электродами. Ячейки заливаются электролитом из 30% водного раствора гидроксида калия ( КОН ). Удельный вес электролита не указывает на то, разряжен аккумулятор или полностью заряжен, а изменяется главным образом при испарении воды. В верхней части элемента имеется пространство для избытка электролита и отверстие для сброса давления. Большие никелированные медные шпильки и толстые соединительные перемычки обеспечивают минимальное эквивалентное последовательное сопротивление батареи.
Выпуск газов означает, что аккумулятор либо разряжается с высокой скоростью, либо заряжается со скоростью, превышающей номинальную. Это также означает, что электролит, потерянный во время вентиляции, необходимо периодически заменять в рамках планового технического обслуживания. В зависимости от циклов зарядки-разрядки и типа аккумулятора период обслуживания может составлять от нескольких месяцев до года.
Напряжение вентилируемого элемента быстро возрастает в конце зарядки, что позволяет использовать очень простую схему зарядного устройства. Обычно аккумулятор заряжается постоянным током со скоростью 1 CA до тех пор, пока все элементы не достигнут напряжения не менее 1,55 В. Далее следует следующий цикл зарядки со скоростью 0,1 CA, снова до тех пор, пока все элементы не достигнут напряжения 1,55 В. Заряд завершается выравниванием или верхним напряжением. предоплата, обычно не менее 4 часов по тарифу 0,1 CA. Целью избыточного заряда является удаление как можно большего количества (если не всех) газов, собранных на электродах: водорода на отрицательном полюсе и кислорода на положительном, а некоторые из этих газов воссоединяются с образованием воды, что, в свою очередь, повышает уровень заряда. уровень электролита до максимального уровня, после чего можно безопасно отрегулировать уровень электролита. Во время перезаряда или подзарядки напряжение элемента превысит 1,6 В, а затем начнет медленно падать. Ни в одном элементе напряжение не должно подниматься выше 1,71 В (сухой элемент) или опускаться ниже 1,55 В (газовый барьер нарушен). [ нужна цитата ]
В самолетной установке с электрической системой плавающей батареи напряжение регулятора устанавливается для зарядки батареи при постоянном потенциале заряда (обычно 14 или 28 В). Если это напряжение установлено слишком высоким, это приведет к быстрой потере электролита. Неисправный регулятор заряда может привести к тому, что напряжение заряда поднимется значительно выше этого значения, что приведет к сильному перезаряду с выкипанием электролита. [ нужна цитата ]

Герметичные Ni-Cd элементы можно использовать индивидуально или собирать в аккумуляторные блоки, содержащие два или более элементов. Маленькие элементы используются для портативной электроники и игрушек (например, садовых фонарей на солнечных батареях), часто с использованием элементов, изготовленных тех же размеров, что и первичные элементы . Когда Ni-Cd батареи заменяются первичными элементами, более низкое напряжение на клеммах и меньшая емкость в ампер-часах могут снизить производительность по сравнению с первичными элементами. Миниатюрные кнопочные элементы иногда используются в фототехнике, ручных фонарях (фонариках или фонариках), резервной памяти компьютера, игрушках и новинках.
Специальные никель-кадмиевые батареи используются в беспроводных и беспроводных телефонах, аварийном освещении и других устройствах. Благодаря относительно низкому внутреннему сопротивлению они могут выдавать большие импульсные токи . Это делает их выгодным выбором для электрических моделей самолетов, лодок и автомобилей с дистанционным управлением, а также для беспроводных электроинструментов и фотовспышек.
Залитые элементы большего размера используются для запуска аккумуляторов самолетов , электромобилей и резервного питания .
Достижения в технологиях производства аккумуляторов во второй половине двадцатого века сделали производство аккумуляторов все более дешевым. Популярность устройств с батарейным питанием в целом возросла. По состоянию на 2000 год ежегодно производилось около 1,5 миллиарда никель-кадмиевых батарей. [5] Вплоть до середины 1990-х годов Ni–Cd аккумуляторы занимали подавляющую часть рынка аккумуляторных батарей для бытовой электроники.
В какой-то момент на долю Ni–Cd батарей приходилось 8% всех продаж портативных вторичных (перезаряжаемых) батарей в ЕС, в Великобритании — 9,2% (утилизация), а в Швейцарии — 1,3% всех продаж портативных батарей. [6] [7] [8]
В ЕС Директива о батареях 2006 года ограничила продажу никель-кадмиевых батарей потребителям для портативных устройств.
Ni-Cd элементы доступны в тех же размерах, что и щелочные батареи , от AAA до D, а также в нескольких размерах с несколькими элементами, включая эквивалент 9-вольтовой батареи. Полностью заряженный одиночный Ni-Cd элемент без нагрузки имеет разность потенциалов от 1,25 до 1,35 В, которая остается относительно постоянной по мере разряда аккумулятора. Поскольку напряжение щелочной батареи, почти полностью разряженной, может упасть до 0,9 В, Ni-Cd-элементы и щелочные элементы обычно взаимозаменяемы для большинства применений.
Помимо одиночных элементов, существуют батареи, содержащие до 300 элементов (номинальное напряжение 360 В, фактическое напряжение без нагрузки от 380 до 420 В). Эта многоячеечная конструкция в основном используется в автомобильной и тяжелой промышленности. Для портативных устройств количество ячеек обычно не превышает 18 (24 В). Доступны затопленные аккумуляторы промышленного размера емкостью от 12,5 Ач до нескольких сотен Ач.
В последнее время никель-металлогидридные и литий-ионные батареи стали коммерчески доступны и дешевле, причем первый тип теперь конкурирует по стоимости с Ni-Cd батареями. Там, где плотность энергии важна, Ni-Cd батареи сейчас находятся в невыгодном положении по сравнению с никель-металлогидридными и литий-ионными батареями. Тем не менее, Ni–Cd аккумулятор по-прежнему очень полезен в приложениях, требующих очень высокой скорости разряда, поскольку он может выдерживать такой разряд без повреждений или потери емкости.
По сравнению с другими типами аккумуляторов никель-кадмиевые аккумуляторы имеют ряд явных преимуществ:
Основным недостатком никель-кадмиевых батарей является их более высокая стоимость и использование кадмия. Этот тяжелый металл представляет опасность для окружающей среды и очень токсичен для всех высших форм жизни. Они также дороже свинцово-кислотных аккумуляторов, поскольку никель и кадмий стоят дороже. Одним из самых больших недостатков является то, что батарея имеет очень выраженный отрицательный температурный коэффициент. Это означает, что при повышении температуры элемента внутреннее сопротивление падает. Это может создать значительные проблемы с зарядкой, особенно при использовании относительно простых систем зарядки, используемых для аккумуляторов свинцово-кислотного типа. В то время как свинцово-кислотные аккумуляторы можно заряжать, просто подключив к ним динамо-машину с помощью простой системы электромагнитного отключения на случай, если динамо-машина неподвижна или возникает перегрузка по току, Ni-Cd аккумулятор при аналогичной схеме зарядки будет проявлять термическую выход из-под контроля, при котором зарядный ток будет продолжать расти до тех пор, пока не сработает предохранитель перегрузки по току или батарея не разрушится сама. Это основной фактор, препятствующий его использованию в качестве аккумуляторов для запуска двигателей. Сегодня с системами зарядки на основе генератора переменного тока с полупроводниковыми регуляторами построение подходящей системы зарядки было бы относительно простым, но производители автомобилей не хотят отказываться от проверенной технологии. [9]
Ni–Cd аккумуляторы могут страдать от « эффекта памяти », если их разряжать и перезаряжать до одного и того же уровня заряда сотни раз. Очевидным симптомом является то, что батарея «запоминает» точку цикла разрядки, в которой началась перезарядка, и во время последующего использования в этой точке происходит внезапное падение напряжения, как если бы батарея была разряжена. Емкость аккумулятора существенно не уменьшается. Некоторая электроника, предназначенная для питания от никель-кадмиевых батарей, способна выдерживать такое пониженное напряжение достаточно долго, чтобы напряжение вернулось в нормальное состояние. Однако, если устройство не сможет работать в течение этого периода пониженного напряжения, оно не сможет получить достаточно энергии от батареи, и для всех практических целей батарея окажется «разряженной» раньше, чем обычно.
Есть свидетельства того, что история с эффектом памяти возникла на орбитальных спутниках, где они одинаково заряжались и разряжались на каждом витке вокруг Земли в течение нескольких лет. [10] По прошествии этого времени было обнаружено, что ёмкости аккумуляторов значительно снизились, но всё ещё были пригодны к использованию. Маловероятно, что такая точная повторяющаяся зарядка (например, 1000 зарядов/разрядов с изменчивостью менее 2%) когда-либо сможет быть воспроизведена людьми, использующими электротовары. Оригинальная статья, описывающая эффект памяти, была написана учеными GE из их отдела аккумуляторного бизнеса в Гейнсвилле, штат Флорида, и позже ими отозвана, но ущерб был нанесен. [11]
Аккумулятор выдерживает тысячи циклов зарядки/разрядки. Также уменьшить эффект памяти можно, полностью разряжая батарею примерно раз в месяц. [ нужна цитация ] Таким образом, очевидно, что аккумулятор не «помнит» точку в цикле зарядки.
Эффектом, симптомы которого схожи с эффектом памяти, является так называемое снижение напряжения или эффект ленивой батареи . Это происходит в результате неоднократной перезарядки; Симптомом является то, что аккумулятор выглядит полностью заряженным, но быстро разряжается уже после короткого периода работы. В редких случаях большую часть потерянной емкости можно восстановить за несколько циклов глубокой разрядки — функция, которую часто обеспечивают автоматические зарядные устройства. Однако этот процесс может сократить срок хранения батареи. [ нужна цитата ] При правильном обращении Ni-Cd аккумулятор может прослужить 1000 циклов и более, прежде чем его емкость упадет ниже половины первоначальной емкости. Многие домашние зарядные устройства заявляют, что являются «умными зарядными устройствами», которые отключаются и не повреждают батарею, но это, похоже, распространенная проблема. [ нужна цитата ]
Ni–Cd аккумуляторы содержат от 6% (для промышленных аккумуляторов) до 18% (для коммерческих аккумуляторов) кадмия , который является токсичным тяжелым металлом и поэтому требует особой осторожности при утилизации аккумуляторов.
В США ожидаемая стоимость переработки аккумулятора (которая будет использована для надлежащей утилизации в конце срока службы) включена в стоимость покупки аккумулятора.
В соответствии с так называемой «директивой о батареях» ( 2006/66/EC ) продажа потребительских никель-кадмиевых батарей теперь запрещена на территории Европейского Союза, за исключением использования в медицинских целях; системы сигнализации; аварийное освещение; и переносные электроинструменты. Эта последняя категория была запрещена с 2016 года. [12] Согласно той же директиве ЕС, использованные промышленные никель-кадмиевые батареи должны собираться их производителями для переработки на специализированных предприятиях.