В химии молекулярные оксогалогениды ( оксигалогениды ) — группа химических соединений , в которых атомы кислорода и галогена присоединены к другому химическому элементу А в одной молекуле . Они имеют общую формулу AO m X n , где X — галоген . Известные оксогалогениды содержат в своих молекулах фтор (F), хлор (Cl), бром (Br) и/или йод (I). Элемент А может быть элементом основной группы , переходным элементом , редкоземельным элементом или актинидом . Термин оксогалогенид или оксигалогенид может также относиться к минералам и другим кристаллическим веществам с той же общей химической формулой, но имеющим ионную структуру.

Оксогалогениды можно рассматривать как промежуточные соединения между оксидами и галогенидами . Существует три основных метода синтеза: [1]
Кроме того, различные оксогалогениды могут быть получены реакциями обмена галогенов, и эта реакция также может привести к образованию смешанных оксогалогенидов, таких как POFCl 2 и CrO 2 FCl .
По отношению к оксиду или галогениду, для данной степени окисления элемента А, если два атома галогена заменяют один атом кислорода или наоборот , общий заряд молекулы не изменяется, а координационное число центрального атома уменьшается на единицу. . Например, как оксихлорид фосфора ( POCl 3 ), так и пентахлорид фосфора ( PCl 5 ) являются нейтральными ковалентными соединениями фосфора в степени окисления +5 . Если атом кислорода просто заменить атомом галогена, заряд увеличится на +1, но координационное число не изменится. Это иллюстрируется реакцией смеси хромата или дихромата и хлорида калия с концентрированной серной кислотой .
Полученный хромилхлорид не имеет электрического заряда и представляет собой летучую ковалентную молекулу , которую можно отогнать из реакционной смеси. [2]
Оксогалогениды элементов в высоких степенях окисления являются сильными окислителями с окислительной способностью, аналогичной соответствующему оксиду или галогениду. Большинство оксогалогенидов легко гидролизуются . Например, хромилхлорид гидролизуется до хромата в обратной реакции синтеза, описанной выше. Движущей силой этой реакции является образование связей АО, которые более прочны, чем связи A-Cl. Это дает благоприятный вклад энтальпии в изменение свободной энергии Гиббса реакции [3]
Многие оксогалогениды могут действовать как кислоты Льюиса . Это особенно справедливо для оксогалогенидов с координационным числом 3 или 4, которые, принимая одну или несколько электронных пар от основания Льюиса , становятся 5- или 6-координационными. Оксогалогенид-анионы, такие как [VOCl 4 ] 2-, можно рассматривать как кислотно-основные комплексы оксогалогенида ( VOCl 2 ) с большим количеством галогенид-ионов, действующих как основания Льюиса. Другим примером является VOCl 2 , который образует тригонально-бипирамидальный комплекс VOCl 2 (N(CH 3 ) 3 ) 2 с основанием триметиламином . [4]
Подробно определены колебательные спектры многих оксогалогенидов . Они дают полезную информацию об относительной прочности связи. Например, в CrO 2 F 2 валентные колебания Cr–O находятся при 1006 см –1 и 1016 см –1 , а валентные колебания Cr–F – при 727 см –1 и 789 см –1 . Разница слишком велика, чтобы быть обусловленной разной массой атомов O и F. Скорее, это показывает, что связь Cr–O намного прочнее связи Cr–F. Связи M–O обычно считаются двойными , и это подтверждается измерениями длин связей M–O. Это означает, что элементы A и O химически связаны между собой σ-связью и π-связью. [5]
Оксогалогениды элементов в высоких степенях окисления интенсивно окрашены из-за переходов с переносом заряда от лиганда к металлу (LMCT). [6]


Углерод образует оксогалогениды COX 2 , X = F , Br и очень токсичный фосген (X = Cl), который получают в промышленности катализируемой углеродом реакцией окиси углерода с хлором . Это полезный реагент в органической химии для образования карбонильных соединений . [7] Например:
Тетрафторид кремния реагирует с водой с образованием плохо изученных оксифторидных полимеров, но медленная и осторожная реакция при -196 ° C также дает оксифторид гексафтордисилоксан. [8]
Азот образует с азотом два ряда оксогалогенидов в степенях окисления 3, NOX, X = F , Cl , Br и 5, NO 2 X , X = F , Cl. Их получают путем галогенирования оксидов азота. Обратите внимание , что NO 2 F изоэлектронен нитрат - иону NO .−3. Известны только оксогалогениды фосфора (V). [9]
Сера образует оксогалогениды [10] в степени окисления +4, например тионилхлорид , SOCl 2 и степени окисления +6, например, сульфурилфторид ( SO 2 F 2 ), сульфурилхлорид ( SO 2 Cl 2 ) и тионилтетрафторид ( SOF) . 4 ). Все они легко гидролизуются. Действительно, тионилхлорид можно использовать в качестве агента дегидратации, поскольку молекулы воды превращаются в газообразные продукты, оставляя после себя безводный твердый хлорид. [11]
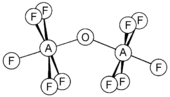
Селен и теллур образуют сходные соединения, а также оксо-мостиковые соединения F 5 AOAF 5 (A = S, Se, Te). Они нелинейны с углом АОА 142,5, 142,4 и 145,5° для S, Se и Te соответственно. [12] Анион теллура F 5 TeO - , известный как тефлат , представляет собой крупный и довольно стабильный анион, полезный для образования стабильных солей с крупными катионами. [11]
Галогены образуют различные оксофториды с формулами XO 2 F ( хлорилфторид ), XO 3 F ( перхлорилфторид ) и XOF 3 с X = Cl, Br и I. Известны также IO 2 F 3 и IOF 5 . [13]
Ксенон образует окситетрафторид ксенона ( XeOF 4 ), диоксидифторид ксенона ( XeO 2 F 2 ) и оксидифторид ксенона ( XeOF 2 ).

Ниже представлена подборка известных оксогалогенидов переходных металлов , а более подробные списки доступны в литературе. [15] X обозначает различные галогениды, чаще всего F и Cl.

Высокие степени окисления металла диктуются тем, что кислород , как и фтор, является сильным окислителем . Бром и йод являются относительно слабыми окислителями, поэтому известно меньше оксобромидов и оксоиодидов. Структуры соединений с конфигурацией d 0 предсказываются теорией VSEPR . Так, CrO 2 Cl 2 тетраэдрический , OsO 3 F 2 тригонально - бипирамидальный , XeOF 4 квадратно - пирамидальный и OsOF 5 октаэдрический . [18] Комплекс d 1 ReOCl 4 имеет квадратно-пирамидальную форму.
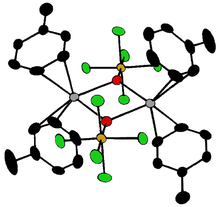
Соединения [Ta 2 OX 10 ] 2- и [M 2 OCl 10 ] 4- (M = W, Ru, Os) имеют две группы MX 5 , соединенные мостиковым атомом кислорода. [19] Каждый металл имеет октаэдрическое окружение. Необычная линейная структура M-O-M может быть объяснена с точки зрения теории молекулярных орбиталей , что указывает на наличие d π — p π- связи между атомами металла и кислорода. [20] Кислородные мостики присутствуют в более сложных конфигурациях, таких как M(cp) 2 (OTeF 5 ) 2 (M = Ti, Zr, Hf, Mo или W; cp = циклопентадиенил , η 5 -C 5 H 5 ) [21] или [AgOTeF 5 -(C 6 H 5 CH 3 ) 2 ] 2 . [17]
В ряду актинидов такие соединения уранила , как уранилхлорид ( UO 2 Cl 2 ) и [UO 2 Cl 4 ] 2-, хорошо известны и содержат линейный фрагмент UO 2 . Подобные виды существуют для нептуния и плутония .

Оксохлорид висмута (BiOCl, бисмоклит ) — редкий пример минерала оксогалогенида. Кристаллическая структура имеет тетрагональную симметрию и может рассматриваться как состоящая из слоев ионов Cl - , Bi 3+ и O 2- в порядке Cl-Bi-O-Bi-Cl-Cl-Bi-O-Bi- кл. Эта слоистая графитоподобная структура приводит к относительно низкой твердости бисмоклита ( 2–2,5 по шкале Мооса ) и большинства других оксогалогенидных минералов. [22] Эти другие минералы включают терлингуаит Hg 2 OCl , образовавшийся в результате выветривания ртутьсодержащих минералов. [23] Мендипит , Pb 3 O 2 Cl 2 , образовавшийся из исходного месторождения сульфида свинца в несколько стадий, является еще одним примером вторичного оксогалоидного минерала.
Элементы железо , сурьма , висмут и лантан образуют оксохлориды общей формулы MOCl. MOBr и MOI также известны Sb и Bi. Многие из их кристаллических структур были определены. [24]
{{cite journal}}: CS1 maint: несколько имен: список авторов ( ссылка ). Структура проиллюстрирована в Housectroft & Sharpe, рис. 22.5.