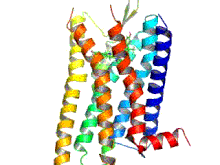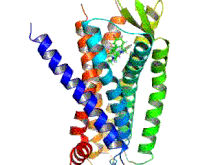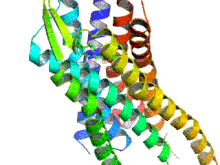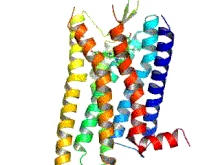
Опиоидные рецепторы представляют собой группу ингибирующих рецепторов, связанных с G-белком, с опиоидами в качестве лигандов . [1] [2] [ 3 ] Эндогенными опиоидами являются динорфины , энкефалины , эндорфины , эндоморфины и ноцицептин . Опиоидные рецепторы примерно на 40% идентичны рецепторам соматостатина (SSTR). Опиоидные рецепторы широко распространены в головном и спинном мозге , на периферических нейронах и в пищеварительном тракте .
К середине 1960-х годов в результате фармакологических исследований стало очевидно, что опиоиды , вероятно, будут оказывать свое действие на определенные рецепторные участки и что таких участков, вероятно, будет несколько. [4] Ранние исследования показали, что опиаты накапливаются в мозге. [5] Рецепторы были впервые идентифицированы как специфические молекулы с помощью исследований связывания, в которых было обнаружено, что опиаты, помеченные радиоизотопами , связываются с гомогенатами мембран головного мозга . Первое такое исследование было опубликовано в 1971 году с использованием 3 H - левофанола . [6] В 1973 году Кэндис Перт и Соломон Х. Снайдер опубликовали первое детальное исследование связывания того, что впоследствии оказалось мю-опиоидным рецептором , с использованием 3 H - налоксона . [7] Это исследование получило широкое признание как первое окончательное открытие опиоидного рецептора, хотя вскоре за ним последовали еще два исследования. [8] [9]
Очистка рецептора дополнительно подтвердила его существование. Первая попытка очистить опиоидный рецептор включала использование нового опиоидного антагониста под названием хлорналтрексамин , который, как было продемонстрировано, связывается с опиоидным рецептором. [10] Позже Карузо очистил экстрагированный детергентом компонент мембраны мозга крысы, который элюировался специфически связанным 3 H -хлорналтрексамином. [11]
Существует четыре основных подтипа опиоидных рецепторов. [12] OGFr был первоначально открыт и назван новым опиоидным рецептором дзета (ζ). Однако впоследствии было обнаружено, что он имеет небольшое сходство последовательностей с другими опиоидными рецепторами и имеет совершенно другую функцию.
(Я). Имя на основе порядка открытия
Семейство опиоидных рецепторов (OR) возникло в результате двух случаев дупликации одного предкового опиоидного рецептора на ранних этапах эволюции позвоночных. Филогенетический анализ показывает, что семейство опиоидных рецепторов уже присутствовало у происхождения челюстных позвоночных более 450 миллионов лет назад. У людей этот паралогон, возникший в результате двойной тетраплоидизации, привел к тому, что рецепторные гены оказались расположены на хромосомах 1, 6, 8 и 20. События тетраплоидизации часто приводят к потере одного или нескольких дуплицированных генов, но в этом случае почти все виды сохраняют все четыре опиоидных рецептора, что указывает на биологическую значимость этих систем. Стефано проследил совместную эволюцию ОР и иммунной системы, лежащую в основе того факта, что эти рецепторы помогали животным на ранних стадиях пережить болевой и воспалительный шок в агрессивной среде. [16]
Семейства рецепторов дельта, каппа и мю демонстрируют идентичность друг другу на 55–58% и гомологию с рецептором ноцицептина на 48–49% . В совокупности это указывает на то, что ген рецептора NOP, OPRL1, имеет такое же эволюционное происхождение, но более высокую частоту мутаций, чем другие гены рецептора. [17]
Хотя семейства опиоидных рецепторов имеют много общего, их структурные различия приводят к функциональным различиям. Таким образом, мю-опиоидные рецепторы вызывают расслабление, доверие, удовлетворение и анальгезию. [18] [19] Эта система также может помочь установить стабильные, эмоционально преданные отношения. Эксперименты с молодыми морскими свинками показали, что социальная привязанность опосредована опиоидной системой. Эволюционная роль передачи опиоидных сигналов в этом поведении была подтверждена на собаках, курах и крысах. [18] Опиоидные рецепторы также играют роль в брачном поведении. [20] Однако мю-опиоидные рецепторы не только контролируют социальное поведение, они также заставляют людей чувствовать себя расслабленными в широком диапазоне других ситуаций. [ нужна цитата ]
Каппа- и дельта-опиоидные рецепторы могут быть менее связаны с релаксацией и анальгезией, поскольку каппа-опиоидный рецептор подавляет активацию мю-опиоидного рецептора, а дельта-опиоидный рецептор по-разному взаимодействует с агонистами и антагонистами. Каппа-опиоидные рецепторы участвуют в перцептивной мобилизации хронической тревоги, тогда как дельта-опиоидные рецепторы вызывают инициацию действий, импульсивность и поведенческую мобилизацию. [19] [21] Эти различия привели некоторые исследования к предположению, что повышение или понижение регуляции внутри трех семейств опиоидных рецепторов являются основой различной диспозиционной эмоциональности, наблюдаемой при психических расстройствах. [22] [23] [24]
Специфические для человека когнитивные особенности, модулированные опиоидами, объясняются не различиями в кодировании рецепторов или лигандов, которые имеют 99% сходства с приматами, а регуляторными изменениями в уровнях экспрессии. [25] [26]
Рецепторы были названы по первой букве первого лиганда , который, как было обнаружено, связывался с ними. Морфин был первым химическим веществом, которое, как было показано, связывается с «мю»-рецепторами . Первая буква препарата морфий — m , отображается как соответствующая греческая буква μ. Подобным же образом впервые было показано, что препарат, известный как кетоциклазоцин , прикрепляется к κ- (каппа)-рецепторам, тогда как δ-рецептор (дельта) был назван в честь ткани семявыносящего протока мыши , в которой рецептор был впервые охарактеризован. [28] Позже был идентифицирован и клонирован дополнительный опиоидный рецептор на основании гомологии с кДНК . Этот рецептор известен как ноцицептиновый рецептор или ORL1 (опиатный рецептор-подобный 1).
Типы опиоидных рецепторов идентичны почти на 70%, различия расположены на N- и C-концах. Рецептор μ, пожалуй, самый важный. Считается, что белок G связывается с третьей внутриклеточной петлей всех опиоидных рецепторов. И у мышей , и у людей гены различных подтипов рецепторов расположены на отдельных хромосомах.
В тканях человека идентифицированы отдельные подтипы опиоидных рецепторов. Исследования до сих пор не смогли выявить генетические доказательства существования этих подтипов, и считается, что они возникают в результате посттрансляционной модификации клонированных типов рецепторов. [29]
Подкомитет IUPHAR [30] [31] рекомендовал, чтобы подходящей терминологией для трех классических (μ, δ, κ) рецепторов и неклассического (ноцицептинового) рецептора была MOP (« M u OP iate receptor» ) , ДОП, КОП и НОП соответственно.
Сигма (σ)-рецепторы когда-то считались опиоидными рецепторами из-за противокашлевого действия многих опиоидных препаратов, опосредованного через σ-рецепторы, а первые селективные σ-агонисты были производными опиоидных препаратов (например, аллилнорметазоцина ). Однако было обнаружено, что σ-рецепторы не активируются эндогенными опиоидными пептидами и сильно отличаются от других опиоидных рецепторов как по функциям, так и по последовательности генов, поэтому в настоящее время их обычно не классифицируют как опиоидные рецепторы.
Существование дополнительных опиоидных рецепторов (или подтипов рецепторов) также было предложено на основании фармакологических доказательств действия эндогенных опиоидных пептидов, но показано, что они не опосредованы ни одним из четырех известных подтипов опиоидных рецепторов. Существование подтипов рецепторов или дополнительных рецепторов, отличных от классических опиоидных рецепторов (μ, δ, κ), основано на ограниченных доказательствах, поскольку идентифицированы только три гена трех основных рецепторов. [32] [33] [34] Единственный из этих дополнительных рецепторов, который был окончательно идентифицирован, - это дзета (ζ) опиоидный рецептор, который, как было показано, является модулятором клеточного фактора роста, а эндогенным лигандом является мет-энкефалин . Этот рецептор сейчас чаще всего называют рецептором опиоидного фактора роста (OGFr) . [35] [36]
Другим постулируемым опиоидным рецептором является ε-опиоидный рецептор. Существование этого рецептора было заподозрено после того, как было показано, что эндогенный опиоидный пептид бета-эндорфин оказывает дополнительные действия, которые, по-видимому, не опосредуются ни одним из известных опиоидных рецепторов. [37] [38] Активация этого рецептора вызывает сильную аналгезию и высвобождение мет-энкефалина ; Было показано , что ряд широко используемых опиоидных агонистов, таких как µ-агонист эторфин и κ-агонист бремазоцин , действуют как агонисты этого эффекта (даже в присутствии антагонистов их более известных целей), [39] в то время как бупренорфин Было показано, что он действует как антагонист эпсилона. В настоящее время доступно несколько селективных агонистов и антагонистов предполагаемого рецептора эпсилон; [40] [41] однако попытки найти ген для этого рецептора оказались безуспешными, а эпсилон-опосредованные эффекты отсутствовали у мышей с «тройным нокаутом» μ/δ/κ , [42] предполагая, что рецептор эпсилон, вероятно, либо вариант сплайсинга , полученный в результате альтернативной посттрансляционной модификации, либо гетеромер , полученный в результате гибридизации двух или более известных опиоидных рецепторов.
Опиоидные рецепторы представляют собой тип рецептора, связанного с G-белком (GPCR). Эти рецепторы распределены по всей центральной нервной системе и в периферических тканях нервного и неневрального происхождения. Они также расположены в высоких концентрациях в околоводопроводном сером слое , голубом пятне и ростральном вентромедиальном мозговом веществе . [43] Рецепторы состоят из внеклеточного N-конца аминокислоты , семи трансмембранных спиральных петель, трех внеклеточных петель, трех внутриклеточных петель и внутриклеточного карбоксильного С-конца. Три внеклеточные петли GPCR обеспечивают пространство, к которому могут прикрепляться сигнальные молекулы для генерации ответа. Гетеротримерный G-белок содержит три различные субъединицы, которые включают субъединицу альфа (α), субъединицу бета (β) и субъединицу гамма (γ). [44] Гамма- и бета-субъединицы постоянно связаны друг с другом, образуя одну субъединицу Gβγ. Гетеротримерные G-белки действуют как «молекулярные переключатели», которые играют ключевую роль в передаче сигнала, поскольку передают информацию от активированных рецепторов соответствующим эффекторным белкам. Все α-субъединицы G-белка содержат пальмитат, который представляет собой насыщенную жирную кислоту с 16 атомами углерода, которая присоединена вблизи N-конца посредством лабильной обратимой тиоэфирной связи к аминокислоте цистеину. Именно пальмитоилирование позволяет белку G взаимодействовать с фосфолипидами мембран из-за гидрофобной природы альфа-субъединиц. Гамма-субъединица также модифицирована липидами и также может прикрепляться к плазматической мембране. Эти свойства двух субъединиц позволяют G-белку опиоидного рецептора постоянно взаимодействовать с мембраной через липидные якоря. [45]
Когда агонистический лиганд связывается с опиоидным рецептором, происходит конформационное изменение, и молекула GDP высвобождается из субъединицы Gα. Этот механизм сложен и является основным этапом пути передачи сигнала. Когда молекула GDP присоединена, субъединица Gα находится в неактивном состоянии, а карман связывания нуклеотидов закрыт внутри белкового комплекса. Однако при связывании лиганда рецептор переключается в активную конформацию, что обусловлено межмолекулярной перестройкой между трансмембранными спиралями. Активация рецептора высвобождает «ионный замок», который удерживает вместе цитоплазматические стороны третьей и шестой трансмембранных спиралей, заставляя их вращаться. Это конформационное изменение обнажает внутриклеточные рецепторные домены на цитозольной стороне, что в дальнейшем приводит к активации G-белка. Когда молекула GDP диссоциирует от субъединицы Gα, молекула GTP связывается со свободным нуклеотидсвязывающим карманом, и G-белок становится активным. Образуется комплекс Gα(GTP), который имеет более слабое сродство к субъединице Gβγ, чем комплекс Gα(GDP), в результате чего субъединица Gα отделяется от субъединицы Gβγ, образуя две части G-белка. . Субъединицы теперь могут свободно взаимодействовать с эффекторными белками; однако они все еще прикреплены к плазматической мембране с помощью липидных якорей. [46] После связывания активные субъединицы G-белка диффундируют внутри мембраны и действуют на различные внутриклеточные эффекторные пути. Это включает в себя ингибирование активности аденилатциклазы нейронов, а также усиление гиперполяризации мембран. Когда стимулируется ферментный комплекс аденилатциклазы , это приводит к образованию циклического аденозин-3',5'-монофосфата (цАМФ) из аденозин-5'-трифосфата (АТФ). цАМФ действует как вторичный мессенджер, поскольку он перемещается из плазматической мембраны в клетку и передает сигнал. [47]
цАМФ связывается и активирует цАМФ-зависимую протеинкиназу А (PKA), которая расположена внутриклеточно в нейроне. ПКА состоит из холофермента – соединения, которое становится активным благодаря соединению фермента с коферментом. Фермент PKA также содержит две каталитические субъединицы PKS-Cα и регуляторный димер субъединицы PKA-R. Холофермент PKA неактивен в нормальных условиях, однако, когда молекулы цАМФ, которые производятся ранее в рамках механизма передачи сигнала, объединяются с ферментом, PKA претерпевает конформационные изменения. Это активирует его, придавая ему способность катализировать фосфорилирование субстрата. [48] CREB (белок, связывающий элемент ответа цАМФ) принадлежит к семейству транскрипционных факторов и расположен в ядре нейрона. Когда PKA активируется, она фосфорилирует белок CREB (добавляет высокоэнергетическую фосфатную группу) и активирует его. Белок CREB связывается с элементами ответа цАМФ CRE и может либо увеличивать, либо уменьшать транскрипцию определенных генов. Описанный выше сигнальный путь цАМФ/ПКА/CREB имеет решающее значение для формирования памяти и модуляции боли. [49] Он также важен для индукции и поддержания долгосрочной потенциации — явления, лежащего в основе синаптической пластичности — способности синапсов усиливаться или ослабевать с течением времени.
Потенциал-зависимые кальциевые каналы (VDCC) играют ключевую роль в деполяризации нейронов и играют важную роль в стимулировании высвобождения нейротрансмиттеров. Когда агонисты связываются с опиоидными рецепторами, G-белки активируются и диссоциируют на составляющие их субъединицы Gα и Gβγ. Субъединица Gβγ связывается с внутриклеточной петлей между двумя трансмембранными спиралями VDCC. Когда субъединица связывается с потенциал-зависимым кальциевым каналом, она производит потенциал-зависимый блок, который ингибирует канал, предотвращая поток ионов кальция в нейрон. В клеточную мембрану также встроен связанный с G-белком калиевый канал, выпрямляющий внутрь . Когда молекула Gβγ или Gα(GTP) связывается с С-концом калиевого канала, она становится активной, и ионы калия выкачиваются из нейрона. [50] Активация калиевого канала и последующая дезактивация кальциевого канала вызывает гиперполяризацию мембраны . Это когда происходит изменение потенциала мембраны, так что он становится более отрицательным. Уменьшение количества ионов кальция приводит к уменьшению высвобождения нейромедиаторов, поскольку кальций необходим для возникновения этого события. [51] Это означает, что нейротрансмиттеры, такие как глутамат и вещество Р, не могут высвобождаться из пресинаптических окончаний нейронов. Эти нейротрансмиттеры жизненно важны для передачи боли, поэтому активация опиоидных рецепторов снижает высвобождение этих веществ, создавая тем самым сильный обезболивающий эффект.
Некоторые формы мутаций δ-опиоидных рецепторов приводят к постоянной активации рецепторов. [52]