Опухоль надпочечника или масса надпочечника [2] — это любые доброкачественные или злокачественные новообразования надпочечника , некоторые из которых отличаются тенденцией к избыточной выработке эндокринных гормонов . Рак надпочечника — это наличие злокачественных опухолей надпочечника, включающее нейробластому , адренокортикальную карциному и некоторые феохромоцитомы надпочечника . Большинство феохромоцитом надпочечника и все адренокортикальные аденомы являются доброкачественными опухолями, которые не метастазируют и не проникают в близлежащие ткани, но могут вызывать значительные проблемы со здоровьем, нарушая баланс гормонов.
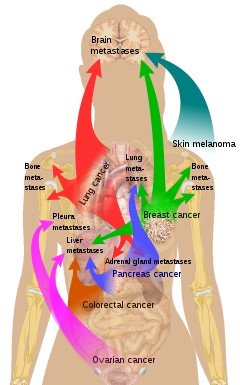
Метастазы в один или оба надпочечника являются наиболее распространенной формой злокачественного поражения надпочечников и второй по распространенности опухолью надпочечников после доброкачественных аденом. [4] Первичные опухоли в таких случаях чаще всего возникают из-за рака легких (39%), рака молочной железы (35%), злокачественной меланомы , рака желудочно-кишечного тракта , рака поджелудочной железы и рака почек . [4]
Кора надпочечников состоит из трех отдельных слоев эндокринных клеток, которые вырабатывают критически важные стероидные гормоны . К ним относятся глюкокортикоиды , которые имеют решающее значение для регуляции уровня сахара в крови и иммунной системы , а также для ответа на физиологический стресс ; минералкортикоид альдостерон , который регулирует кровяное давление и функцию почек ; и некоторые половые гормоны . Как доброкачественные , так и злокачественные опухоли коры надпочечников могут вырабатывать стероидные гормоны, что имеет важные клинические последствия. [ необходима цитата ]
Адренокортикальные аденомы — доброкачественные опухоли коры надпочечников, которые встречаются чрезвычайно часто (присутствуют у 1–10% людей при аутопсии). Их не следует путать с адренокортикальными «узелками», которые не являются истинными новообразованиями. Адренокортикальные аденомы редко встречаются у пациентов моложе 30 лет и встречаются с одинаковой частотой у обоих полов. [ необходима цитата ] Клиническое значение этих новообразований двояко. Во-первых, они были обнаружены как случайные находки с возрастающей частотой в последние годы из-за все более широкого использования КТ и магнитно-резонансной томографии в различных медицинских учреждениях. Это может привести к дорогостоящим дополнительным исследованиям и инвазивным процедурам для исключения незначительной возможности ранней адренокортикальной карциномы . Во-вторых, меньшинство (около 15%) адренокортикальных аденом являются «функциональными», что означает, что они вырабатывают глюкокортикоиды , минералкортикоиды и/или половые стероиды , что приводит к эндокринным расстройствам, таким как синдром Кушинга , синдром Конна (гиперальдостеронизм), вирилизация женщин или феминизация мужчин. Функциональные адренокортикальные аденомы излечиваются хирургическим путем. [ необходима цитата ]
Большинство адренокортикальных аденом имеют размер менее 2 см в наибольшем измерении и вес менее 50 граммов. Однако размер и вес опухолей надпочечников больше не считаются надежным признаком доброкачественности или злокачественности. Грубо говоря, адренокортикальные аденомы представляют собой инкапсулированные, четко очерченные, одиночные опухоли с твердой, однородной желтой поверхностью. Некроз и кровоизлияние встречаются редко. [ необходима цитата ]
Адренокортикальная карцинома (АКК) — редкий, очень агрессивный рак клеток коры надпочечников, который может возникнуть как у детей, так и у взрослых. АКК могут быть «функциональными», вырабатывая стероидные гормоны и вызывая эндокринную дисфункцию, подобную той, что наблюдается во многих адренокортикальных аденомах, но многие из них таковыми не являются. Из-за своего расположения глубоко в забрюшинном пространстве большинство адренокортикальных карцином не диагностируются, пока не вырастут достаточно большими. Они часто проникают в крупные сосуды, такие как почечная вена и нижняя полая вена , а также метастазируют через лимфатическую систему и кровь в легкие и другие органы. Наиболее эффективным лечением является хирургическое вмешательство , хотя для многих пациентов это невыполнимо, и общий прогноз заболевания неблагоприятный. Химиотерапия , лучевая терапия и гормональная терапия также могут использоваться для лечения этого заболевания. [ необходима цитата ]
Мозговое вещество надпочечников анатомически расположено в центре каждого надпочечника и состоит из нейроэндокринных (хромаффинных) клеток, которые вырабатывают и выделяют эпинефрин (адреналин) в кровоток в ответ на активацию симпатической нервной системы . Нейробластома и феохромоцитома являются двумя наиболее важными опухолями, которые возникают из мозгового вещества надпочечников. Обе опухоли могут также возникать из экстра-надпочечниковых участков, в частности, в параганглиях симпатической цепи . [ необходима цитата ]
Нейробластома — агрессивный рак незрелых нейробластических клеток (предшественников нейронов ) и один из самых распространенных видов рака у детей , средний возраст постановки диагноза — два года. [5] Нейробластома надпочечников обычно проявляется быстро увеличивающейся брюшной массой. Хотя опухоль часто распространяется на отдаленные части тела на момент постановки диагноза, этот рак необычен тем, что во многих случаях он хорошо поддается лечению, когда распространение ограничивается печенью , кожей и /или костным мозгом (стадия IVS). Связанные, но менее агрессивные опухоли, состоящие из более зрелых нервных клеток, включают ганглионейробластому и ганглионейрому . Нейробластические опухоли часто производят повышенные уровни метаболитов катехоламиновых гормонов, таких как ванилилминдальная кислота (ВМК) и гомованилиновая кислота , и могут вызывать сильную водянистую диарею за счет продукции вазоактивного кишечного пептида . Лечение нейробластомы включает хирургию и лучевую терапию при локализованном заболевании и химиотерапию при метастатическом заболевании. [6]
Феохромоцитома — это новообразование , состоящее из клеток, похожих на хромаффинные клетки зрелого мозгового вещества надпочечников. Феохромоцитомы встречаются у пациентов всех возрастов и могут быть спорадическими или связанными с наследственным раковым синдромом , таким как множественная эндокринная неоплазия (МЭН) типов IIA и IIB, нейрофиброматоз типа I или синдром фон Гиппеля-Линдау . Только 10% феохромоцитом надпочечников являются злокачественными , в то время как остальные являются доброкачественными опухолями . Наиболее клинически важной особенностью феохромоцитом является их тенденция вырабатывать большое количество катехоламиновых гормонов эпинефрина ( адреналина) и норадреналина . Это может привести к потенциально опасному для жизни высокому кровяному давлению или сердечной аритмии , а также многочисленным симптомам, таким как головная боль , сердцебиение , приступы тревоги , потливость , потеря веса и тремор . Диагноз легче всего подтвердить с помощью измерения в моче метаболитов катехоламинов , таких как ВМА и метанефрины . Большинство феохромоцитом изначально лечат антиадренергическими препаратами для защиты от перегрузки катехоламинами, а хирургическое вмешательство применяют для удаления опухоли, как только состояние пациента стабилизируется. [7]
Инциденталома надпочечника — это опухоль надпочечника, обнаруженная случайно без клинических симптомов или подозрений. Это одна из наиболее распространенных неожиданных находок, обнаруженных с помощью компьютерной томографии (КТ), магнитно-резонансной томографии (МРТ) или ультрасонографии. [8]
В этих случаях часто используется тест подавления дексаметазона для выявления избытка кортизола , а метанефрины или катехоламины — для выявления избытка этих гормонов . Опухоли размером менее 3 см обычно считаются доброкачественными и лечатся только при наличии оснований для диагностики синдрома Кушинга или феохромоцитомы . [9] Рентгеноплотность дает подсказку в оценке риска злокачественности, при этом опухоль с 10 единицами Хаунсфилда или менее на неусиленной КТ, вероятно, является аденомой, богатой липидами. [10]
При КТ доброкачественные аденомы обычно имеют низкую рентгенографическую плотность (из-за содержания жира) и показывают быстрое вымывание контрастного вещества (50% или более контрастного вещества вымывается за 10 минут). Если гормональная оценка отрицательная и визуализация предполагает доброкачественность, следует рассмотреть возможность последующего наблюдения с визуализацией через 6, 12 и 24 месяца и повторить гормональную оценку ежегодно в течение 4 лет. [11]
КТ и МРТ, предназначенные для исследования надпочечников, могут быть выполнены для различения доброкачественных аденом от потенциально злокачественных новообразований. [12] [13] Онлайн-калькуляторы помогают рентгенологам рассчитывать вымывание контраста в узелках надпочечников на КТ [14] и химический сдвиг на МРТ. [15]
Также может быть полезна гормональная оценка, которая включает: [11]
Хирургический
Для карцином надпочечников наиболее эффективным лечением является хирургическое вмешательство , хотя для многих пациентов это невыполнимо, а общий прогноз заболевания неблагоприятный. Химиотерапия , лучевая терапия и гормональная терапия также могут использоваться при лечении этого заболевания.
Систематический обзор Cochrane 2018 года сравнивал два различных типа хирургического вмешательства: лапароскопическую ретропериотениальную адреналэктомию и лапароскопическую транспериотенальную адреналэктомию при различных типах опухолей надпочечников. [16] Лапароскопическая ретропериотениальная адреналэктомия, по-видимому, снижает позднюю заболеваемость, время до приема пероральной жидкости или пищи и время до начала ходьбы по сравнению с лапароскопической транспериотенальной адреналэктомией. [16] Однако в этих результатах была неопределенность из-за низкого качества доказательств, а также неубедительных результатов о влиянии любой из операций на общую смертность, раннюю заболеваемость, социально-экономические эффекты, продолжительность операции, операционную кровопотерю, переход на открытую операцию. [16]
Циркулирующие в крови микроРНК (миРНК) были исследованы в последние годы на предмет их потенциала в качестве менее инвазивного биомаркера заболеваний надпочечников. До сих пор в девяти исследованиях изучалось наличие циркулирующих микроРНК в крови у пациентов с диагнозом адренокортикальных опухолей. [17] [18] МикроРНК могут высвобождаться в кровоток тремя различными типами экскреции. [19] Клеточное повреждение с пассивным высвобождением (некроз, воспаление), активной секрецией в форме внеклеточных везикул (ВВ) (микровезикулы, экзосомы и апоптотические тельца) или в ассоциации с липопротеинами высокой плотности (ЛПВП) и белками аргонавтов (AGO). [20] [21] Большинство микроРНК, обнаруженных в крови, находятся в комплексах с AGO. [22] [23] Несмотря на многообещающие результаты, чувствительность потенциальных маркеров циркулирующих микроРНК для адренокортикальных опухолей, по-видимому, является переменной. Повышение чувствительности может быть достигнуто путем нацеливания только на EV-ассоциированные miRNA, поскольку предполагается, что высвобождение miRNA в EV является контролируемым процессом. [24] Таким образом, EV-ассоциированные miRNA могут действовать как более специфичные маркеры злокачественности. [24] Однако, поскольку были значительные различия в результатах проведенных исследований, методологические различия и малое количество пациентов могли способствовать этому несоответствию. Это требует дальнейших исследований на более крупных когортах с едиными методологическими требованиями для выяснения применимости циркулирующих miRNA в качестве биомаркеров прогноза и злокачественности у пациентов с диагнозом адренокортикальные опухоли. [17]
{{cite book}}: |website=проигнорировано ( помощь )