
Пламя (от лат. flamma ) — это видимая, газообразная часть огня . Оно возникает в результате высокоэкзотермической химической реакции, происходящей в тонкой зоне. [1] Когда пламя достаточно горячее, чтобы иметь ионизированные газообразные компоненты достаточной плотности, оно считается плазмой . [ неопределенно ] [2]
Цвет и температура пламени зависят от типа топлива, участвующего в сгорании. Например, когда зажигалку подносят к свече , приложенное тепло заставляет молекулы топлива в воске свечи испаряться. [примечание 1] В этом состоянии они затем могут легко реагировать с кислородом в воздухе, который выделяет достаточно тепла в последующей экзотермической реакции, чтобы испарить еще больше топлива, таким образом поддерживая постоянное пламя. Высокая температура пламени заставляет испаренные молекулы топлива разлагаться , образуя различные продукты неполного сгорания и свободные радикалы , и эти продукты затем реагируют друг с другом и с окислителем, участвующим в реакции следующего пламени (пожара).
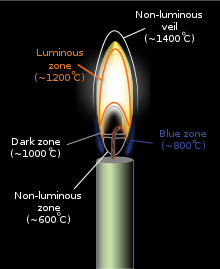
Можно исследовать различные части пламени свечи с помощью холодной металлической ложки: [4] более высокие части пламени производят осаждение водяного пара, результат сгорания, желтые части в середине производят сажу, а область около фитиля свечи производит несгоревший воск. Ювелиры используют более высокие части пламени с металлической паяльной трубкой для плавки золота и серебра. Достаточная энергия в пламени возбудит электроны в некоторых переходных промежуточных продуктах реакции, таких как радикал метилидина (CH) и двухатомный углерод (C2 ) , что приводит к излучению видимого света, поскольку эти вещества высвобождают свою избыточную энергию (см. спектр ниже для объяснения того, какие конкретные виды радикалов производят какие конкретные цвета). По мере увеличения температуры горения пламени (если пламя содержит небольшие частицы несгоревшего углерода или другого материала), увеличивается и средняя энергия электромагнитного излучения, испускаемого пламенем (см. Черное тело ).
Другие окислители, помимо кислорода, могут использоваться для получения пламени. Водород, горящий в хлоре, производит пламя и в процессе выделяет газообразный хлористый водород (HCl) в качестве продукта сгорания. [5] Еще одним из многих возможных химических сочетаний является гидразин и тетраоксид азота , который является гиперголическим и обычно используется в ракетных двигателях. Фторполимеры могут использоваться для подачи фтора в качестве окислителя металлического топлива, например, в составе магний/тефлон/витон .
Химическая кинетика, происходящая в пламени, очень сложна и обычно включает большое количество химических реакций и промежуточных видов, большинство из которых радикалы . Например, известная схема химической кинетики, GRI-Mech, [6] использует 53 вида и 325 элементарных реакций для описания горения биогаза .
Существуют различные методы распределения необходимых компонентов горения в пламени. В диффузионном пламени кислород и топливо диффундируют друг в друга; пламя возникает там, где они встречаются. В предварительно смешанном пламени кислород и топливо предварительно смешиваются, что приводит к другому типу пламени. Пламя свечи (диффузионное пламя) работает за счет испарения топлива, которое поднимается в ламинарном потоке горячего газа, который затем смешивается с окружающим кислородом и сгорает.

Цвет пламени зависит от нескольких факторов, наиболее важными из которых обычно являются излучение черного тела и спектральная полоса излучения, при этом как спектральная линия излучения, так и спектральная линия поглощения играют меньшую роль. В наиболее распространенном типе пламени, углеводородном пламени, наиболее важным фактором, определяющим цвет, является подача кислорода и степень предварительного смешивания топлива с кислородом, что определяет скорость горения и, следовательно, температуру и пути реакции, тем самым создавая различные цветовые оттенки.

В лаборатории при нормальных условиях гравитации и с закрытым воздухозаборником горелка Бунзена горит желтым пламенем (также называемым безопасным пламенем) с пиковой температурой около 2000 К (3100 °F). Желтый цвет возникает из- за раскаливания очень мелких частиц сажи, которые производятся в пламени. Также образуется оксид углерода , и пламя имеет тенденцию забирать кислород с поверхностей, которых оно касается. Когда воздухозаборник открыт, образуется меньше сажи и оксида углерода. При подаче достаточного количества воздуха сажа или оксид углерода не производятся, и пламя становится синим. (Большая часть этого синего цвета ранее была скрыта яркими желтыми выбросами.) Спектр предварительно смешанного (полного сгорания) бутанового пламени справа показывает, что синий цвет возникает именно из-за испускания возбужденных молекулярных радикалов в пламени, которые испускают большую часть своего света значительно ниже ≈565 нанометров в синей и зеленой областях видимого спектра.
Более холодная часть диффузионного (неполного сгорания) пламени будет красной, переходящей в оранжевый, желтый и белый по мере повышения температуры, о чем свидетельствуют изменения в спектре излучения черного тела. Для заданной области пламени, чем ближе к белому на этой шкале, тем горячее эта часть пламени. Переходы часто видны в пожарах, в которых цвет, излучаемый ближе всего к топливу, белый, с оранжевой секцией над ним, и красноватым пламенем, самым высоким из всех. [7] Пламя синего цвета появляется только тогда, когда количество сажи уменьшается и синие излучения от возбужденных молекулярных радикалов становятся доминирующими, хотя синий цвет часто можно увидеть около основания свечей, где сажа в воздухе менее сконцентрирована. [8]
Определенные цвета можно придать пламени путем введения возбудимых видов с яркими линиями спектра излучения . В аналитической химии этот эффект используется в тестах пламени (или спектроскопии эмиссии пламени ) для определения присутствия некоторых ионов металлов. В пиротехнике пиротехнические красители используются для создания ярких цветных фейерверков.

При рассмотрении температуры пламени есть много факторов, которые могут изменяться или применяться. Важным является то, что цвет пламени не обязательно определяет сравнение температур, поскольку излучение черного тела — не единственное, что производит или определяет видимый цвет; поэтому это только оценка температуры. Другие факторы, которые определяют его температуру:
Это приблизительное руководство по температурам пламени для различных распространенных веществ (в воздухе при температуре 20 °C (68 °F) и давлении 1 атм.):
Дицианоацетилен , соединение углерода и азота с химической формулой C4N2 , горит в кислороде ярким сине-белым пламенем при температуре 5260 К (4990 °C; 9010 °F), а в озоне — до 6000 К (5730 °C; 10340 °F) . [10] Такая высокая температура пламени частично обусловлена отсутствием водорода в топливе (дицианоацетилен не является углеводородом), поэтому среди продуктов сгорания нет воды.
Цианоген с формулой (CN) 2 производит второе по температуре известное естественное пламя с температурой более 4525 °C (8177 °F) при горении в кислороде. [11] [12]
При температурах до 120 °C (248 °F) смеси топлива и воздуха могут вступать в химическую реакцию и производить очень слабое пламя, называемое холодным пламенем. Это явление было открыто Гемфри Дэви в 1817 году. Процесс зависит от тонкого баланса температуры и концентрации реагирующей смеси, и при правильных условиях он может инициироваться без какого-либо внешнего источника воспламенения. Циклические изменения в балансе химикатов, особенно промежуточных продуктов реакции, вызывают колебания в пламени с типичным изменением температуры около 100 °C (212 °F) или между «холодным» и полным воспламенением. Иногда изменение может привести к взрыву. [9] [13]

В 2000 году эксперименты НАСА подтвердили, что гравитация играет косвенную роль в образовании и составе пламени. [14] Обычное распределение пламени в условиях нормальной гравитации зависит от конвекции , поскольку сажа имеет тенденцию подниматься к вершине пламени (например, в свече в условиях нормальной гравитации), делая его желтым. В условиях микрогравитации или невесомости , например на орбите, естественная конвекция больше не происходит, и пламя становится сферическим, с тенденцией становиться более синим и более эффективным. Существует несколько возможных объяснений этой разницы, из которых наиболее вероятным является гипотеза о том, что температура достаточно равномерно распределена, чтобы сажа не образовывалась и происходило полное сгорание. [15] Эксперименты НАСА показывают, что диффузионное пламя в условиях микрогравитации позволяет полностью окислить больше сажи после их образования, чем диффузионное пламя на Земле, из-за ряда механизмов, которые ведут себя по-разному в условиях микрогравитации по сравнению с условиями нормальной гравитации. [16] Эти открытия имеют потенциальное применение в прикладной науке и частной промышленности, особенно в отношении эффективности использования топлива .
Пламя не обязательно должно быть вызвано только выделением химической энергии. В звездах дозвуковые фронты горения, вызванные сжиганием легких ядер (таких как углерод или гелий) до тяжелых ядер (вплоть до группы железа), распространяются как пламя. Это важно в некоторых моделях сверхновых типа Ia . В термоядерном пламени теплопроводность доминирует над диффузией видов, поэтому скорость и толщина пламени определяются термоядерным выделением энергии и теплопроводностью (часто в форме вырожденных электронов ). [17]