Пурин — гетероциклическое ароматическое органическое соединение , состоящее из двух колец ( пиримидинового и имидазольного ), слитых вместе. Он водорастворим . Пурины также дают название более широкому классу молекул — пуринам , который включает замещенные пурины и их таутомеры . Это наиболее широко встречающиеся в природе азотсодержащие гетероциклы. [1]
Пурины в высокой концентрации содержатся в мясе и мясных продуктах, особенно во внутренних органах, таких как печень и почки . В целом, растительная диета содержит мало пуринов. [2] К растениям и водорослям с высоким содержанием пуринов относятся некоторые бобовые ( чечевица , соевые бобы и черноглазый горох ) и спирулина . Примеры источников с высоким содержанием пуринов включают: сладкое мясо , анчоусы , сардины , печень, говяжьи почки, мозги , мясные экстракты (например, Oxo , Bovril ), сельдь , скумбрия , морские гребешки , мясо дичи , дрожжи ( пиво , дрожжевой экстракт , пищевые дрожжи ) . и подливка . [3]
Умеренное количество пурина содержится также в красном мясе, говядине , свинине , птице , рыбе и морепродуктах , спарже , цветной капусте , шпинате , грибах , зеленом горошке , чечевице , сушеном горохе, фасоли , овсянке , пшеничных отрубях , зародышах пшеницы и боярышнике . . [4]
Пурины и пиримидины составляют две группы азотистых оснований , в том числе две группы нуклеотидных оснований . Пуриновыми основаниями являются гуанин (G) и аденин (А), которые образуют соответствующие нуклеозиды- дезоксирибонуклеозиды ( дезоксигуанозин и дезоксиаденозин ) с дезоксирибозным фрагментом и рибонуклеозиды ( гуанозин , аденозин ) с рибозным фрагментом. Эти нуклеозиды с фосфорной кислотой образуют соответствующие нуклеотиды (дезоксигуанилат, дезоксиаденилат и гуанилат, аденилат), которые являются строительными блоками ДНК и РНК соответственно. Пуриновые основания также играют важную роль во многих метаболических и сигнальных процессах в составе соединений гуанозинмонофосфата (ГМФ) и аденозинмонофосфата (АМФ).
Для осуществления этих важнейших клеточных процессов клетке необходимы как пурины, так и пиримидины , и в одинаковых количествах. И пурин, и пиримидин обладают самоингибирующими и активирующими свойствами . Когда пурины образуются, они ингибируют ферменты , необходимые для образования большего количества пуринов. Это самоингибирование происходит, поскольку они также активируют ферменты, необходимые для образования пиримидина. Пиримидин одновременно самоингибирует и активирует пурин аналогичным образом. Благодаря этому в клетке всегда присутствует почти одинаковое количество обоих веществ. [5]
Пурин является одновременно очень слабой кислотой ( pK a 8,93) и еще более слабым основанием ( pK a 2,39). [6] При растворении в чистой воде pH находится посередине между этими двумя значениями pKa.
Пурин является ароматическим веществом , имеющим четыре таутомера , каждый из которых имеет водородную связь с одним из четырех атомов азота. Они обозначены как 1-H, 3-H, 7-H и 9-H (см. изображение пронумерованного кольца). Обычная кристаллическая форма предпочитает таутомер 7-H, тогда как в полярных растворителях преобладают таутомеры 9-H и 7-H. [7] Заместители в кольцах и взаимодействия с другими молекулами могут сместить равновесие этих таутомеров. [8]
В природе много пуринов. К ним относятся нуклеиновые основания аденин ( 2 ) и гуанин ( 3 ). В ДНК эти основания образуют водородные связи с комплементарными им пиримидинами , тимином и цитозином соответственно. Это называется комплементарным спариванием оснований. В РНК аденину вместо тимина является урацил .
Другими известными пуринами являются гипоксантин , ксантин , теофиллин , теобромин , кофеин , мочевая кислота и изогуанин .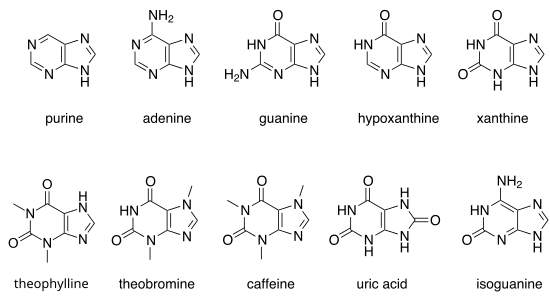 [ противоречивый ]
[ противоречивый ]

Помимо решающей роли пуринов (аденина и гуанина) в ДНК и РНК, пурины также являются важными компонентами ряда других важных биомолекул, таких как АТФ , ГТФ , циклический АМФ , НАДН и кофермент А. Сам пурин ( 1 ) в природе не обнаружен, но его можно получить путем органического синтеза .
Они также могут действовать непосредственно как нейротрансмиттеры , воздействуя на пуринергические рецепторы . Аденозин активирует аденозиновые рецепторы .
Слово пурин ( чистая моча ) [9] было придумано немецким химиком Эмилем Фишером в 1884 году. [10] [11] Впервые он синтезировал его в 1898 году. [11] Исходным материалом для последовательности реакций была мочевая кислота. ( 8 ), который был выделен из камней в почках Карлом Вильгельмом Шееле в 1776 году. [12] Мочевая кислота (8) подвергалась реакции с PCl 5 с образованием 2,6,8-трихлорпурина ( 10 ), который превращался с помощью HI и PH 4 I для получения 2,6-дийодпурина ( 11 ). Продукт восстанавливали до пурина ( 1 ) с помощью цинковой пыли.
Многие организмы имеют метаболические пути синтеза и расщепления пуринов.
Пурины биологически синтезируются в виде нуклеозидов (оснований, присоединенных к рибозе ).
Накопление модифицированных пуриновых нуклеотидов нарушает различные клеточные процессы, особенно те, которые затрагивают ДНК и РНК . Чтобы быть жизнеспособными, организмы обладают рядом дезоксипуринфосфогидролаз, которые гидролизуют эти производные пурина, удаляя их из активных пулов NTP и dNTP . Дезаминирование пуриновых оснований может приводить к накоплению таких нуклеотидов, как ITP , dITP, XTP и dXTP. [13]
Дефекты ферментов, которые контролируют выработку и расщепление пуринов, могут серьезно изменить последовательности ДНК клеток, что может объяснить, почему люди, несущие определенные генетические варианты пуриновых метаболических ферментов, имеют более высокий риск развития некоторых типов рака .
Организмы во всех трех сферах жизни — эукариоты , бактерии и археи — способны осуществлять биосинтез пуринов de novo . Эта способность отражает необходимость пуринов для жизни. Биохимический путь синтеза очень похож у эукариот и бактерий, но более изменчив у архей. [14] Было установлено, что почти полный или полный набор генов, необходимых для биосинтеза пуринов, присутствует у 58 из 65 изученных видов архей. [14] Однако также были идентифицированы семь видов архей, у которых полностью или почти полностью отсутствовали гены, кодирующие пурин. По-видимому, виды архей, неспособные синтезировать пурины, способны приобретать экзогенные пурины для роста [14] и, таким образом, аналогичны пуриновым мутантам эукариот, например, пуриновым мутантам гриба Ascomycete Neurospora crassa [15] , которым также необходимы экзогенные пурины для роста. рост.
Более высокий уровень потребления мяса и морепродуктов связан с повышенным риском развития подагры , тогда как более высокий уровень потребления молочных продуктов связан со снижением риска. Умеренное потребление богатых пуринами овощей или белков не связано с повышенным риском развития подагры. [16] Аналогичные результаты были получены в отношении риска гиперурикемии .
Помимо синтеза пуринов in vivo при пуриновом обмене , пурин также можно синтезировать искусственно.
Пурин ( 1 ) получается с хорошим выходом при нагревании формамида в открытом сосуде при 170°C в течение 28 часов. [17]
Эта замечательная реакция и другие подобные ей обсуждались в контексте происхождения жизни . [18]
Запатентованный 20 августа 1968 года признанный в настоящее время метод производства аденина в промышленных масштабах представляет собой модифицированную форму формамидного метода. В этом методе формамид нагревается при температуре 120 градусов Цельсия в закрытой колбе в течение 5 часов с образованием аденина. Количество реакции значительно увеличивается при использовании оксихлорида фосфора (фосфорилхлорида) или пентахлорида фосфора в качестве кислотного катализатора и солнечного или ультрафиолетового излучения. По прошествии 5 часов и остывании раствора формамид-оксихлорид фосфора-аденин в колбу, содержащую формамид и образовавшийся теперь аденин, наливают воду. Затем водно-формамид-адениновый раствор пропускают через фильтрующую колонку с активированным углем. Молекулы воды и формамида, будучи небольшими молекулами, пройдут через уголь и попадут в колбу для отходов; однако большие молекулы аденина прикрепляются к древесному углю или «адсорбируются» из-за сил Ван-дер-Ваальса, которые взаимодействуют между аденином и углеродом в древесном угле. Поскольку древесный уголь имеет большую площадь поверхности, он способен захватывать большинство молекул, которые проходят через него определенного размера (больше, чем вода и формамид). Чтобы извлечь аденин из аденина, адсорбированного углем, газообразный аммиак, растворенный в воде (водный аммиак), выливают на структуру активированный уголь-аденин, чтобы высвободить аденин в водный раствор аммиака. Затем раствор, содержащий воду, аммиак и аденин, оставляют сушиться на воздухе, при этом аденин теряет растворимость из-за потери газообразного аммиака, который ранее делал раствор основным и способным растворять аденин, что приводит к его кристаллизации в чистый белый порошок. что можно хранить. [19]
Оро и Камат (1961) и сотрудники Оргель (1966, 1967) показали, что четыре молекулы HCN тетрамеризуются с образованием диаминомалеодинитрила ( 12 ), который может превращаться почти во все встречающиеся в природе пурины. [20] [21] [22] [23] [24] Например, пять молекул HCN конденсируются в экзотермической реакции с образованием аденина , особенно в присутствии аммиака.
Синтез пуринов Траубе (1900) — классическая реакция (названная в честь Вильгельма Траубе ) между аминозамещенным пиримидином и муравьиной кислотой . [25]
Чтобы понять, как возникла жизнь , необходимы знания о химических путях, которые позволяют формировать ключевые строительные блоки жизни в вероятных пребиотических условиях . Нам и др. (2018) [26] продемонстрировали прямую конденсацию пуриновых и пиримидиновых азотистых оснований с рибозой с образованием рибонуклеозидов в водных микрокапельках, что является ключевым этапом, ведущим к образованию РНК. Кроме того, Becker et al. представили возможный пребиотический процесс синтеза пуриновых рибонуклеозидов. (2016). [27]