Пропионил-КоА представляет собой производное кофермента А пропионовой кислоты . Он состоит из 24 углеродных цепей (без кофермента это 3-углеродная структура), и его производство и метаболическая судьба зависят от того, в каком организме он присутствует. [1] К его производству могут привести несколько различных путей, например: путем катаболизма определенных аминокислот или окисления жирных кислот с нечетной цепью . [2] Позже он может расщепляться пропионил-КоА-карбоксилазой или посредством метилцитратного цикла. [3] Однако в различных организмах пропионил-КоА может быть изолирован в контролируемых областях, чтобы снизить его потенциальную токсичность за счет накопления. [4] Генетические недостатки, связанные с выработкой и распадом пропионил-КоА, также имеют большое клиническое и человеческое значение. [5]
Существует несколько различных путей производства пропионил-КоА:
Метаболическая (катаболическая судьба) пропионил-КоА зависит от того , в какой среде он синтезируется. Следовательно, пропионил-КоА в анаэробной среде может иметь другую судьбу, чем в аэробном организме . Множественные пути, либо катаболизм пропионил-КоА-карбоксилазы, либо метилцитратсинтазы, также зависят от присутствия различных генов. [7]
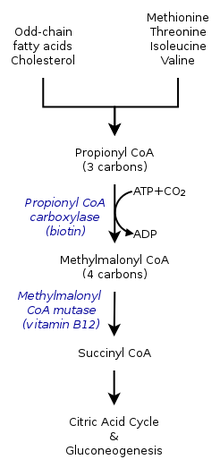
В цикле лимонной кислоты у человека пропионил-КоА, который взаимодействует с оксалоацетатом с образованием метилцитрата, также может катализироваться с образованием метилмалонил-КоА посредством карбоксилирования пропионил -КоА-карбоксилазой (PCC). Метилмалонил-КоА позже трансформируется в сукцинил-КоА для дальнейшего использования в цикле трикарбоновых кислот . PCC не только катализирует карбоксилирование пропионил-КоА в метилмалонил-КоА, но также действует на несколько различных ацил-КоА. Тем не менее, его наибольшая аффинность связывания наблюдается с пропионил-КоА. Далее было показано, что трансформация пропионил-КоА ингибируется отсутствием нескольких маркеров ТСА , таких как глутамат . Механизм показан на рисунке слева. [2]
У млекопитающих пропионил-КоА превращается в ( S ) -метилмалонил-КоА под действием пропионил-КоА-карбоксилазы , биотин -зависимого фермента, также требующего бикарбоната и АТФ .
Этот продукт превращается в ( R )-метилмалонил-КоА под действием метилмалонил-КоА рацемазы .
( R )-Метилмалонил-КоА превращается в сукцинил-КоА , промежуточное соединение в цикле трикарбоновых кислот , под действием метилмалонил-КоА-мутазы , фермента, требующего

кобаламин катализирует миграцию углерод-углеродных связей.
Механизм мутазы метилмалонил -КоА начинается с разрыва связи между 5'- СН
2- 5'-дезоксиаденозила и кобальта, находящегося в степени окисления 3+ (III), который дает 5'- дезоксиаденозильный радикал и кобаламин в восстановленной степени окисления Co(II).
Затем этот радикал отрывает атом водорода от метильной группы метилмалонил-КоА, в результате чего образуется радикал метилмалонил-КоА. Считается, что этот радикал образует углерод-кобальтовую связь с коферментом, за которой затем следует перестройка углеродного скелета субстрата, образуя радикал сукцинил-КоА. Затем этот радикал отрывает водород от ранее полученного 5'-дезоксиаденозина, снова создавая дезоксиаденозильный радикал, который атакует кофермент, реформируя исходный комплекс.
Дефект фермента мутазы метилмалонил-КоА приводит к метилмалоновой ацидурии — опасному заболеванию, которое вызывает снижение pH крови. [8]

Накопление пропионил-КоА может оказаться токсичным для различных организмов. Поскольку были предложены различные циклы превращения пропионил-КоА в пируват, одним из изученных механизмов является метилцитратный цикл . Начальной реакцией является бета-окисление с образованием пропионил-КоА, который далее расщепляется в ходе цикла. В этом пути участвуют ферменты, связанные как с циклом метилцитрата, так и с циклом лимонной кислоты . Все это способствует общей реакции по детоксикации бактерий от вредного пропионил-КоА. Его также считают результатом катаболизма жирных кислот в микобактериях. [3] Чтобы продолжить, ген prpC кодирует метилцитратсинтазу, и если он отсутствует, метилцитратный цикл не произойдет. Вместо этого катаболизм протекает через пропионил-КоА-карбоксилазу. [7] Этот механизм показан ниже слева вместе с участвующими реагентами, продуктами, промежуточными соединениями и ферментами.
На окисление пропионил-КоА с образованием пирувата влияет его необходимость в микобактериях туберкулеза . Накопление пропионил-КоА может привести к токсическим эффектам. Было высказано предположение, что у Mycobacterium Tuberculosis метаболизм пропионил-КоА участвует в биогенезе клеточной стенки . Таким образом , отсутствие такого катаболизма может повысить восприимчивость клетки к различным токсинам, особенно к антимикробным механизмам макрофагов . Другая гипотеза относительно судьбы пропионил-КоА в M. Tuberculosis заключается в том, что, поскольку пропионил-КоА образуется в результате катаболизма жирных кислот с нечетной цепью бета, впоследствии активируется метилцитратный цикл, чтобы свести на нет любую потенциальную токсичность, действуя как буферный механизм. [11]
Пропионил-КоА может оказывать множество неблагоприятных и токсических воздействий на различные виды, включая бактерии . Например, ингибирование пируватдегидрогеназы накоплением пропионил-КоА у Rhodobacter sphaeroides может оказаться смертельным. Кроме того, как и в случае с E. coli , приток пропионил-КоА у миобактерий может привести к токсичности, если не принять меры немедленно. Эта токсичность вызвана действием липидов, образующих клеточную стенку бактерий . Используя этерификацию длинноцепочечных жирных кислот, избыток пропионил-КоА может быть изолирован и сохранен в липиде триацилглицерине (ТАГ), что приводит к регулированию повышенных уровней пропионил-КоА. Такой процесс метильного разветвления жирных кислот заставляет их действовать как стоки для накопления пропиона [4].
В исследовании, проведенном Луо и др., штаммы Escherichia coli использовались для изучения того, как метаболизм пропионил-КоА потенциально может привести к выработке 3-гидроксипропионовой кислоты (3-HP). Было показано, что мутация ключевого гена, участвующего в этом пути, сукцинат-КоА-трансферазы, приводит к значительному увеличению 3-HP. [7] Однако эта область все еще находится в стадии развития, и информация по этой теме ограничена. [12]
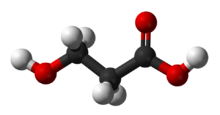
Метаболизм аминокислот в растениях считается спорным вопросом из-за отсутствия конкретных доказательств существования какого-либо конкретного пути. Однако было высказано предположение, что в этом участвуют ферменты, связанные с производством и использованием пропионил-КоА. С этим связан метаболизм изобутирил-КоА . Эти две молекулы считаются промежуточными продуктами метаболизма валина . Поскольку пропионат состоит в форме пропионил-КоА, было обнаружено, что пропионил-КоА превращается в β-гидроксипропионат посредством пероксисомального ферментативного пути β-окисления . Тем не менее, у растения Arabidopsis не наблюдалось ключевых ферментов превращения валина в пропионил-КоА. В ходе различных экспериментов, проведенных Лукасом и др., было высказано предположение, что у растений посредством пероксисомальных ферментов пропионил-КоА (и изобутирил-КоА ) участвуют в метаболизме многих различных субстратов (идентичность в настоящее время оценивается), а не просто валин . [13]

Производство пропионил-КоА посредством катаболизма жирных кислот также связано с тиоэтерификацией . В исследовании, касающемся Aspergillus nidulans , было обнаружено, что при ингибировании гена метилцитратсинтазы mcsA описанного выше пути также ингибируется продукция отдельных поликетидов . Следовательно, утилизация пропионил-КоА через метилцитратный цикл снижает его концентрацию, одновременно увеличивая концентрацию поликетидов. Поликетид — это структура, обычно встречающаяся у грибов, состоящая из ацетил- и малонил -КоА, образующая продукт с чередующимися карбонильными и метиленовыми группами . Поликетиды и производные поликетидов часто имеют очень сложную структуру, а некоторые из них очень токсичны. Это привело к исследованиям по ограничению токсичности поликетидов для сельскохозяйственных культур через фитопатогенные грибы . [14]
Пропионил-КоА также является субстратом для посттрансляционной модификации белков путем реакции с остатками лизина на белках, реакция, называемая пропионилированием белка . [15] [16] Из-за структурного сходства ацетил-КоА и пропионил-КоА считается, что в реакции пропионилирования используются многие из тех же ферментов, которые используются для ацетилирования белков. [16] Хотя функциональные последствия пропионилирования белка в настоящее время до конца не изучены, пропионилирование in vitro фермента пропионил-КоА-синтетазы контролирует его активность. [17]
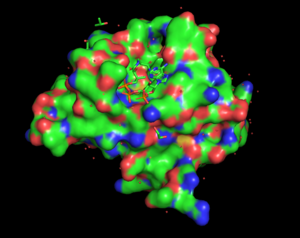
Подобно тому, как пероксисомальные ферменты растений связывают пропионил-КоА и изобутирил-КоА, Gen5, ацетилтрансфераза у человека, связывается с пропионил-КоА и бутирил-КоА . Они специфически связываются с каталитическим доменом Gen5L2 . Эта консервативная ацетилтрансфераза отвечает за регуляцию транскрипции путем ацетилирования лизина N-концевых хвостов гистонов . Эта функция ацетилирования имеет гораздо более высокую скорость реакции, чем пропионилирование или бутирилирование. Из-за структуры пропионил-КоА Gen5 различает разные молекулы ацил-КоА . Фактически было обнаружено, что пропильная группа бутирл-КоА не может связываться из-за отсутствия стереоспецифичности с активным сайтом связывания Gen5 из-за ненасыщенных ацильных цепей . С другой стороны, третий углерод пропионил-КоА может вписаться в активный центр Gen5 с правильной ориентацией. [18]
На этапах развития новорожденного пропионовая ацидемия , которая представляет собой медицинскую проблему, определяемую как недостаток пропионил-КоА-карбоксилазы, может вызывать нарушения, умственную отсталость и множество других проблем. Это вызвано накоплением пропионил-КоА, поскольку он не может быть преобразован в метилмалонил-КоА . Новорожденных проверяют на повышенный уровень пропионилкарнитина. Дальнейшие способы диагностики этого заболевания включают анализ мочи. Используемые лекарства помогают обратить вспять и предотвратить повторение симптомов, включая использование добавок для снижения выработки пропионата . [5]