Репликация вируса — это образование биологических вирусов в процессе инфицирования в целевых клетках-хозяевах. Вирусы должны сначала попасть в клетку, прежде чем вирусная репликация сможет произойти. Путем генерации обильных копий своего генома и упаковки этих копий вирус продолжает заражать новых хозяев. Репликация между вирусами сильно различается и зависит от типа генов, вовлеченных в них. Большинство ДНК-вирусов собираются в ядре, тогда как большинство РНК-вирусов развиваются исключительно в цитоплазме. [1]
Вирусы размножаются только в живых клетках. Клетка- хозяин должна предоставить энергию , синтетические машины и низкомолекулярные предшественники для синтеза вирусных белков и нуклеиновых кислот. [2]
Репликация вируса происходит в семь стадий:
Это первый шаг вирусной репликации. Некоторые вирусы прикрепляются к клеточной мембране клетки -хозяина и вводят свою ДНК или РНК в хозяина, чтобы инициировать инфекцию. Прикрепление к клетке-хозяину часто достигается с помощью белка прикрепления вируса, который простирается от белковой оболочки, также известной как капсид , вируса. Этот белок отвечает за связывание с поверхностным рецептором на плазматической мембране (или мембранных углеводах) клетки-хозяина. Вирусы могут использовать обычные функции клеточных рецепторов, чтобы обеспечить присоединение, имитируя молекулы, которые связываются с рецепторами клетки-хозяина. Например, риновирус использует свой белок прикрепления вируса для связывания с рецептором ICAM-1 на клетках-хозяевах, который обычно используется для облегчения адгезии между другими клетками-хозяевами. [3]
Вход, или проникновение, является вторым этапом репликации вируса. Этот этап характеризуется прохождением вируса через плазматическую мембрану клетки-хозяина. Наиболее распространенным способом проникновения вируса в клетку-хозяина является рецептор-опосредованный эндоцитоз , который происходит без энергетических затрат для вируса, а только для клетки-хозяина. Рецептор-опосредованный эндоцитоз происходит, когда молекула (в данном случае вирус) связывается с рецептором на мембране клетки. Серия химических сигналов от этого связывания заставляет клетку обернуть прикрепленный вирус в плазматическую мембрану вокруг него, образуя содержащую вирус везикулу внутри клетки. [3]
Вирусы проникают в клетки хозяина, используя различные механизмы, включая эндоцитарный и неэндоцитарный пути. [4] Они также могут сливаться с плазматической мембраной и могут распространяться внутри хозяина посредством слияния или слияния клеток друг с другом. [5] Вирусы прикрепляются к белкам на поверхности клеток хозяина, известным как клеточные рецепторы или факторы прикрепления, чтобы облегчить проникновение. [6] Имеются данные, что вирусы используют ионные каналы на клетках хозяина во время проникновения вируса. Слияние: внешние вирусные белки способствуют слиянию вириона с плазматической мембраной. [7] Это образует пору в мембране хозяина, и после проникновения вирион становится непокрытым, а его геномный материал затем переносится в цитоплазму. [8] Слияние клеток с клетками: некоторые вирусы вызывают специфическую экспрессию белков на поверхности инфицированных клеток для привлечения неинфицированных клеток. [9] Это взаимодействие заставляет неинфицированную клетку сливаться с инфицированной клеткой при более низких уровнях pH, образуя многоядерную клетку, известную как синцитий. [10] Эндоцитарные пути: процесс, посредством которого внутриклеточная везикула формируется путем инвагинации мембраны, что приводит к поглощению внеклеточных и связанных с мембраной компонентов, в данном контексте вируса. [11] Неэндоцитарные пути: процесс, посредством которого вирусные частицы высвобождаются в клетку путем слияния внеклеточной вирусной оболочки и мембраны клетки-хозяина. [4]
Раздевание — это третий этап репликации вируса. Раздевание определяется удалением белковой «оболочки» вириона и высвобождением его генетического материала. Этот этап происходит в той же области, где происходит вирусная транскрипция. У разных вирусов есть различные механизмы для раздевания. Некоторые РНК-вирусы, такие как риновирусы, используют низкий pH в эндосомах клетки-хозяина для активации своего механизма раздевания. Это включает в себя высвобождение риновирусом белка, который создает отверстия в эндосоме и позволяет вирусу высвобождать свой геном через отверстия. Многие ДНК-вирусы перемещаются в ядро клетки-хозяина и высвобождают свой генетический материал через ядерные поры. [3]
Четвертый этап вирусного цикла — репликация, которая определяется быстрым производством вирусного генома. То, как вирус подвергается репликации, зависит от типа генетического материала, которым обладает вирус. Основываясь на своем генетическом материале, вирусы будут захватывать соответствующий клеточный механизм для этого генетического материала. Вирусы, которые содержат двухцепочечную ДНК (dsDNA), имеют тот же тип генетического материала, что и все организмы, и поэтому могут использовать ферменты репликации в ядре клетки-хозяина для репликации вирусного генома. Многие РНК-вирусы обычно реплицируются в цитозоле и могут напрямую получать доступ к рибосомам клетки-хозяина для производства вирусных белков, как только РНК находится в репликативной форме.
Вирусы могут проходить два типа жизненных циклов: литический цикл и лизогенный цикл. В литическом цикле вирус вводит свой геном в клетку-хозяина и инициирует репликацию, захватывая клеточный аппарат хозяина для создания новых копий вируса. [12] В лизогенном жизненном цикле вирусный геном включается в геном хозяина. Геном хозяина будет проходить свой обычный жизненный цикл, реплицируясь и делясь, реплицируя вирусный геном вместе со своим собственным. [13] Вирусный геном может быть запущен для начала вирусного производства с помощью химических и экологических стимуляторов. [14] Как только лизогенный вирус входит в литический жизненный цикл, он продолжит пути вирусного производства и продолжит транскрипцию / производство мРНК. (например: герпес на губах, вирус простого герпеса (HSV)-1, лизогенные бактериофаги и т. д.)
Сборка — это когда вновь созданные вирусные белки и геномы собираются и объединяются для формирования незрелых вирусов. Как и другие этапы, то, как собирается конкретный вирус, зависит от типа вируса. Сборка может происходить в плазматической мембране, цитозоле, ядре, аппарате Гольджи и других местах внутри клетки-хозяина. Некоторые вирусы вставляют свой геном в капсид только после того, как капсид завершен, в то время как у других вирусов капсид будет оборачиваться вокруг генома по мере его копирования. [2]
Это последний шаг перед формированием компетентного вируса. Обычно это включает модификации капсида, которые обеспечиваются ферментами (кодируемыми хозяином или вирусом). [3]
Последний этап репликации вируса — высвобождение, когда вновь собранные и зрелые вирусы покидают клетку-хозяина. То, как вирус высвобождается из клетки-хозяина, зависит от типа вируса. Одним из распространенных типов высвобождения является почкование. Это происходит, когда вирусы, которые формируют свою оболочку из плазматической мембраны хозяина, изгибают мембрану вокруг капсида. Когда вирус изгибает плазматическую мембрану, он начинает оборачиваться вокруг всего капсида до тех пор, пока вирус больше не будет прикреплен к клетке-хозяину. Другой распространенный способ, которым вирусы покидают клетку-хозяина, — это лизис клетки , когда вирусы лизируют клетку, заставляя ее лопнуть, что высвобождает зрелые вирусы, которые находились в клетке-хозяине. [3]
Вирусы классифицируются на 7 типов генов, каждый из которых имеет свои собственные семейства вирусов, которые в свою очередь имеют различные стратегии репликации. [15] Дэвид Балтимор , биолог, лауреат Нобелевской премии , разработал систему, называемую Балтиморской системой классификации, для классификации различных вирусов на основе их уникальной стратегии репликации. Существует семь различных стратегий репликации, основанных на этой системе (Балтиморский класс I, II, III, IV, V, VI, VII). Семь классов вирусов перечислены здесь кратко и в общих чертах. [16]
Этот тип вируса обычно должен проникнуть в ядро хозяина, прежде чем он сможет реплицироваться. Некоторым из этих вирусов требуются полимеразы клетки хозяина для репликации их генома , в то время как другие, такие как аденовирусы или вирусы герпеса, кодируют свои собственные факторы репликации. Однако в любом случае репликация вирусного генома сильно зависит от клеточного состояния, допускающего репликацию ДНК, и, таким образом, от клеточного цикла . Вирус может заставить клетку принудительно подвергнуться клеточному делению , что может привести к трансформации клетки и, в конечном итоге, к раку . Примером семейства в этой классификации является Adenoviridae .
Есть только один хорошо изученный пример, в котором семейство вирусов класса 1 не реплицируется внутри ядра. Это семейство Poxvirus , которое включает высокопатогенные вирусы, инфицирующие позвоночных .
Вирусы, которые попадают в эту категорию, включают те, которые не так хорошо изучены, но все же имеют большое отношение к позвоночным. Два примера включают Circoviridae и Parvoviridae . Они реплицируются внутри ядра и образуют двухцепочечную ДНК-промежуточную во время репликации. Человеческий анелловирус, называемый TTV , включен в эту классификацию и обнаруживается почти у всех людей, бессимптомно инфицируя их почти в каждом крупном органе .
РНК-вирусы: Полимераза РНК-вирусов не обладает функциями корректуры, которые есть у полимеразы ДНК-вирусов. Это способствовало тому, что РНК-вирусы имели более низкую репликативную точность по сравнению с ДНК-вирусами, что делает РНК-вирусы высокомутагенными, что может увеличить их общую выживаемость. [17] РНК-вирусы не обладают способностью идентифицировать и восстанавливать несовпадающие или поврежденные нуклеотиды, и, таким образом, РНК-геномы подвержены мутациям, вызванным механизмами, внутренними и внешними для репликации вируса. [18] РНК-вирусы представляют собой терапевтический обоюдоострый меч: РНК-вирусы могут противостоять воздействию противовирусных препаратов, вызывать эпидемии и заражать несколько видов хозяев из-за своей мутагенной природы, что затрудняет их лечение. Однако белок обратной транскриптазы, который часто идет с РНК-вирусом, может использоваться в качестве косвенной мишени для РНК-вирусов, предотвращая транскрипцию и синтез вирусных частиц. [19] (Это основа для препаратов против СПИДа и ВИЧ [20] )
Как и большинство вирусов с геномами РНК , вирусы с двухцепочечной РНК не полагаются на полимеразы хозяина для репликации в той степени, в которой это делают вирусы с геномами ДНК . Вирусы с двухцепочечной РНК изучены не так хорошо, как другие классы. Этот класс включает два основных семейства: Reoviridae и Birnaviridae . Репликация моноцистронная и включает отдельные сегментированные геномы, что означает, что каждый из генов кодирует только один белок, в отличие от других вирусов, которые демонстрируют более сложную трансляцию.
Эти вирусы состоят из двух типов, однако оба разделяют тот факт, что репликация происходит в основном в цитоплазме, и что репликация не так зависит от клеточного цикла, как у ДНК-вирусов. Этот класс вирусов также является одним из наиболее изученных типов вирусов, наряду с двухцепочечными ДНК-вирусами.
Вирусы РНК с положительным смыслом и, конечно, все гены, определяемые как гены с положительным смыслом, могут быть напрямую доступны рибосомам хозяина для немедленного формирования белков. Их можно разделить на две группы, обе из которых реплицируются в цитоплазме:
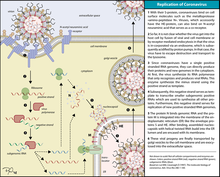
Примерами этого класса являются семейства Coronaviridae , Flaviviridae и Picornaviridae .
Вирусы РНК отрицательного смысла и, конечно, все гены, определяемые как отрицательные, не могут быть напрямую доступны рибосомам хозяина для немедленного формирования белков. Вместо этого они должны быть транскрибированы вирусными полимеразами в «читаемый» комплементарный положительный смысл. Их также можно разделить на две группы:
Примерами этого класса являются семейства Orthomyxoviridae , Paramyxoviridae , Bunyaviridae , Filoviridae и Rhabdoviridae (включая бешенство ).
Хорошо изученное семейство этого класса вирусов включает ретровирусы . Одной из определяющих особенностей является использование обратной транскриптазы для преобразования положительной РНК в ДНК. Вместо использования РНК для шаблонов белков, они используют ДНК для создания шаблонов, которые встраиваются в геном хозяина с помощью интегразы . Затем репликация может начаться с помощью полимераз клетки хозяина.
Эта небольшая группа вирусов, примером которой является вирус гепатита В , имеет двухцепочечный геном с разрывами, который впоследствии заполняется, образуя ковалентно замкнутое кольцо ( cccDNA ), которое служит шаблоном для производства вирусных мРНК и субгеномной РНК. Прегеномная РНК служит шаблоном для вирусной обратной транскриптазы и для производства генома ДНК.