Маннозный рецептор ( кластер D - дифференциации 206, CD206 ) представляет собой лектин С-типа, который в основном присутствует на поверхности макрофагов , незрелых дендритных клеток и синусоидальных эндотелиальных клеток печени, но также экспрессируется на поверхности клеток кожи, таких как дермальные клетки человека. фибробласты и кератиноциты . [1] [2] Это первый член семейства эндоцитарных рецепторов, которое включает Endo180 (CD280) , PLA2R М-типа и DEC-205 (CD205) . [3]
Рецептор распознает терминальные остатки маннозы , N -ацетилглюкозамина и фукозы на гликанах, прикрепленных к белкам [4], обнаруженным на поверхности некоторых микроорганизмов , играющих роль как во врожденной , так и в адаптивной иммунной системе . Дополнительные функции включают выведение из кровообращения гликопротеинов, в том числе сульфатированных гликопротеиновых гормонов и гликопротеинов, высвобождаемых в ответ на патологические события. [5] Рецептор маннозы непрерывно рециркулирует между плазматической мембраной и эндосомальными компартментами клатрин -зависимым образом. [6]

Рецептор маннозы представляет собой трансмембранный белок I типа с внеклеточным N-концом и внутриклеточным С-концом . Сначала он синтезируется как неактивный предшественник, но протеолитически расщепляется до активной формы в аппарате Гольджи . [8] В целом, внеклеточная часть рецептора состоит из 8 последовательных доменов распознавания углеводов (CRD) C-типа, ближайших к плазматической мембране, за которыми следует один повторяющийся домен фибронектина типа II и N-концевой домен, богатый цистеином. . Цитоплазматический хвост не способен изолированно передавать сигнал , поскольку в нем отсутствуют соответствующие сигнальные мотивы. [9]
N-концевой домен, богатый цистеином, гомологичен B-цепи рицина и связывается с фрагментами сульфатированных сахаров, обладая особенно высоким сродством к N -ацетилгалактозамину и остаткам галактозы , сульфатированным в положениях 3 и 4 их пиранозных колец. [10]
Другие лиганды включают хондроитинсульфаты А и В, а также сульфатированные структуры Льюиса x и Льюиса a . [6] Рецептор маннозы является единственным членом семейства, в котором этот домен функционален. [5]
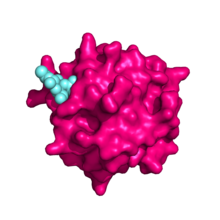
Повторный домен фибронектина типа II консервативен среди всех членов семейства рецепторов маннозы. Коллагены I-IV связываются с этой областью с высоким сродством, тогда как коллаген V связывается лишь слабо. Посредством этого домена рецептор маннозы интернализует коллаген в макрофагах и синусоидных клетках печени независимо от лектиновой активности рецептора. [9] Наряду с N-концевым, богатым цистеином доменом, этот домен является наиболее консервативным у мышей и людей (92%). [8]
8 тандемных CRD во внеклеточной области рецептора маннозы имеют лишь 30% гомологии друг с другом. Каждый из них содержит по крайней мере некоторые аминокислотные остатки, необходимые для связывания Ca 2+ и лиганда, общие для функциональных CRD C-типа. Только CRD 4 и 5 содержат все остатки, необходимые для связывания сахара, образуя устойчивое к протеазам лиганд-связывающее ядро. Наиболее распространенным лигандом являются концевые остатки маннозы, но также связываются N -ацетилглюкозамин и фукоза. [8]
Основное взаимодействие между CRD-4 и его сахарным лигандом происходит посредством прямого лигирования с консервативным Ca 2+ в сайте связывания сахара, аналогично механизму связывания маннан-связывающего лектина (MBL). Однако четверть свободной энергии связывания сахара связана с гидрофобными стопинговыми взаимодействиями, образующимися между одной стороной сахарного кольца и боковой цепью консервативного остатка тирозина в сайте связывания, чего не наблюдается в MBL. Несмотря на сходство связывания маннозы между маннозным рецептором и MBL, эти различия позволяют предположить, что связывание маннозы маннозным рецептором развивалось отдельно от связывания маннозы другими лектинами C-типа. [11]
По отдельности CRD связывают маннозу со слабым сродством. Считается, что связывание с высокой аффинностью является результатом кластеризации нескольких CRD. Эта кластеризация позволяет связывать многовалентные разветвленные лиганды, такие как N-связанные олигосахариды с высоким содержанием маннозы . [12]
Было высказано предположение, что рецептор маннозы может существовать по крайней мере в двух различных структурных конформациях . Каждый CRD C-типа разделен линкерными областями из 10-20 аминокислот, содержащими ряд остатков пролина , чья циклическая боковая цепь довольно жесткая и способствует конформации, в которой N-концевой богатый цистеином домен простирается как можно дальше. из плазматической мембраны, насколько это возможно. [13]
Альтернативно, взаимодействия между соседними CRD могут удерживать их в непосредственной близости друг от друга и вызывать изгиб внеклеточной области рецептора, приводя N-концевой богатый цистеином домен в тесный контакт с CRD. Это позволит расположить CRD 4 и 5 дальше всего от мембраны, чтобы максимизировать их взаимодействие с потенциальными лигандами. Устойчивость к протеолизу, продемонстрированная CRD 4 и 5, предполагает, что физические взаимодействия между двумя доменами действительно происходят, тем самым поддерживая существование этой U-образной конформации. [13]
Считается, что переходы между этими двумя конформациями происходят зависимым от pH образом, регулируя селективность и высвобождение лигандов во время эндоцитоза. Считается, что более низкий и более кислый pH ранних эндосом ответственен за высвобождение лиганда. [13]
Функциональная растворимая форма рецептора маннозы образуется при протеолитическом расщеплении мембраносвязанной формы металлопротеазами , обнаруженными во внеклеточной среде. [14] [15]
Растворимый белок состоит из всей внеклеточной области рецептора и может участвовать в транспортировке маннозилированных белков от очагов воспаления . [9] Было показано, что выделение рецептора маннозы из макрофагов усиливается при распознавании грибковых патогенов , таких как Candida albicans и Aspergillus fumigatus , что позволяет предположить, что растворимая форма может играть роль в распознавании грибковых патогенов. Таким образом, баланс между мембраносвязанными и растворимыми рецепторами маннозы может влиять на нацеливание на грибковые патогены во время инфекции. [16]
Рецептор маннозы сильно гликозилирован, и его N-связанные сайты гликозилирования высоко консервативны у мышей и людей, что указывает на важную роль этой посттрансляционной модификации . Присутствие остатков сиаловой кислоты на N-связанных гликанах маннозного рецептора важно из-за его роли в связывании как сульфатированных, так и маннозилированных гликопротеинов. Сиалилирование регулирует мультимеризацию рецептора, который, как известно, влияет на связывание с сульфатированными гликопротеинами. Также известно, что терминальные остатки сиаловой кислоты необходимы для связывания с маннозилированными гликанами. Отсутствие сиаловой кислоты снижает способность рецепторов связывать и интернализировать маннозилированные гликаны, но не влияет на их локализацию на плазматической мембране или эндоцитарную активность. [9] [17]
Ряд патогенных микроорганизмов, в том числе C. albicans , [15] [18], Pneumocystis carinii [19] [20] и Leishmania donovani [21] [22], содержат на своей поверхности гликаны с концевыми остатками маннозы, которые распознаются C- типа CRD рецептора маннозы, действуя тем самым как маркер чужеродности. После распознавания рецептор интернализует связанный патоген и транспортирует его в лизосомы для деградации по фагоцитарному пути . Таким образом, рецептор маннозы действует как рецептор распознавания образов . Присутствие мотива диароматической последовательности FENTLY (Phe-Glu-Asn-Thr-Leu-Tyr) в цитоплазматическом хвосте рецептора жизненно важно для его клатрин-опосредованной интернализации. [6] Это подтверждается данными о том, что клетки Cos-1, трансфицированные рецептором маннозы, у которого отсутствует С-концевой хвост, неспособны эндоцитозировать C. albicans и P. carinii . [6]
Удивительно, нокаутные мыши по рецептору маннозы не проявляют повышенной восприимчивости к инфекции, что позволяет предположить, что рецептор не важен для фагоцитоза. Однако от его участия нельзя отказаться, поскольку другие механизмы могут компенсировать это. Например, заражение нокаутных мышей P. carinii приводило к усиленному привлечению макрофагов к месту заражения. Кроме того, другие рецепторы, присутствующие на поверхности фагоцитирующих клеток, такие как DC-SIGN , SIGNR1 и Endo180, проявляют аналогичную лиганд-связывающую способность с рецептором маннозы, и поэтому вполне вероятно, что в его отсутствие эти белки способны компенсировать и индуцировать фагоцитоз. . [6]
Считается также, что способность маннозного рецептора способствовать интернализации патогена облегчает заражение Mycobacterium Tuberculosis и Mycobacterium leprae . Эти бактерии обитают и размножаются в макрофагах, предотвращая образование фаголизосом во избежание деградации. Следовательно, опосредуя их вход в макрофаги, блокирование рецептора маннозы помогает этим патогенам инфицировать и расти в клетке-мишени. [6] [23]
CRD-области рецептора маннозы на синусоидальных эндотелиальных клетках печени удаляют ряд отходов, начиная от растворимых макромолекул и заканчивая крупными твердыми частицами. [24] К ним относятся лизосомальные ферменты, [25] α-цепи коллагена, [26] С-концевые пропептиды проколлагенов I типа, [27] и тканевый активатор плазминогена. [28] Исследования показывают, что каждая синусоидальная эндотелиальная клетка печени экспрессирует поверхностный пул из 20 000–25 000 рецепторов маннозы. Маннозный рецептор на синусоидальных эндотелиальных клетках печени представляет собой быстро рециркулирующий рецептор с Ke (константой скорости эндоцитоза) 4,12 мин-1, что соответствует периоду полураспада 10 с для поверхностного пула комплексов рецептор-лиганд. [29]
В отличие от макрофагов, которые используют рецепторы маннозы для фагоцитоза твердых частиц размером более 200 нм, рецептор маннозы на синусоидальных эндотелиальных клетках печени опосредует опосредованный клатрином эндоцитоз макромолекул и наночастиц размером менее 200 нм. [24]
Маннозный рецептор может также играть роль в поглощении и представлении антигена незрелыми дендритными клетками адаптивной иммунной системы. При связывании с рецептором маннозилированные антигены интернализуются и транспортируются в эндоцитарные компартменты внутри клетки для загрузки на молекулы главного комплекса гистосовместимости (MHC) или другие родственные антигенпрезентирующие молекулы. Косвенным примером этого является обработка гликолипидного антигена липоарабиноманнаном , полученным из микобактерий . Липоарабиноманнан (LAM) представлен Т-клеткам в комплексе с CD1b, но также способен связываться с рецептором маннозы. Поскольку присутствие маннана , альтернативного лиганда, ингибирует LAM-зависимую пролиферацию Т-клеток, предполагается, что рецептор связывает внеклеточный LAM, интернализует его, а затем транспортирует в эндоцитарные везикулы для загрузки на CD1b. [8]
Зрелые дендритные клетки и макрофаги используют рецептор маннозы для презентации антигена по-другому. Расщепленный растворимый рецептор связывается с циркулирующими антигенами и направляет их к эффекторным клеткам лимфоидных органов через свой богатый цистеином домен, активируя таким образом адаптивную иммунную систему. [8]
Цитоплазматический хвост маннозного рецептора не содержит никаких сигнальных мотивов, однако было доказано, что рецептор необходим для продукции как про-, так и противовоспалительных цитокинов , что указывает на более пассивную роль рецептора в фагоцитозе патогенов. [6] [8] Это предполагает, что рецептору маннозы помогают другие рецепторы клеточной поверхности, чтобы запустить сигнальный каскад. Например, было показано, что клетки HEK 293 , котрансфицированные человеческим рецептором маннозы и кДНК человеческого Toll-подобного рецептора 2, способны секретировать IL-8 в ответ на инфекцию P. carinii , тогда как клетки, трансфицированные любым рецептором в отдельности, этого не сделали. . [30] Вполне возможно, что два рецептора образуют комплекс на поверхности клетки, который облегчает передачу сигнала при патогенном воздействии.
Другая ключевая роль рецептора маннозы заключается в регулировании уровня молекул, попадающих в кровообращение во время воспалительной реакции. В ответ на патологические события высвобождаются гликопротеины, в том числе лизосомальные гидролазы , тканевой активатор плазминогена и нейтрофильная миелопероксидаза , которые помогают бороться с любыми вторгающимися микроорганизмами. Как только угроза утихнет, эти гликопротеины могут нанести вред тканям хозяина, поэтому их уровень в кровообращении необходимо строго контролировать. [6]
Олигосахариды с высоким содержанием маннозы, присутствующие на поверхности этих гликопротеинов, указывают на их временный характер, поскольку в конечном итоге они распознаются маннозным рецептором и удаляются из кровообращения. Мыши с нокаутом рецептора маннозы менее способны очищать эти белки и демонстрируют повышенные концентрации ряда лизосомальных гидролаз в крови. [5]
В соответствии с этой функцией рецептор маннозы экспрессируется на низких уровнях во время воспаления и на высоких уровнях во время разрешения воспаления, чтобы гарантировать удаление воспалительных агентов из кровообращения только в подходящее время. [5]
N-концевой богатый цистеином домен маннозного рецептора играет важную роль в распознавании сульфатированных гликопротеиновых гормонов и их выведении из кровообращения. [8]
Гликопротеиновые гормоны, такие как лютропин , который вызывает выход яйцеклетки во время овуляции , должны импульсно стимулировать их рецепторы, чтобы избежать десенсибилизации рецепторов . Гликаны на их поверхности покрыты сульфатированным N- ацетилгалактозамином (GalNAc), что делает их лигандами богатого цистеином домена гомологии рицина маннозного рецептора. Эта метка обеспечивает цикл высвобождения, стимуляции и удаления из кровообращения. [7]
Нокаутные мыши, у которых отсутствует фермент, необходимый для добавления сульфатированной закрывающей структуры GalNAc, демонстрируют более длительный период полураспада лутропина, что приводит к повышенной активации рецепторов и выработке эстрогена . Самки нокаутных мышей достигают половой зрелости быстрее, чем их собратья дикого типа, имеют более длительный цикл эструса и производят больше пометов. Таким образом, сульфатированная метка GalNAc очень важна для регуляции концентрации в сыворотке некоторых гликопротеиновых гормонов. [7]
У людей экспрессируются два типа рецепторов маннозы, каждый из которых кодируется собственным геном:
Свойства избирательной интернализации маннозного рецептора указывают на ряд потенциальных применений в здравоохранении и при заболеваниях. Управляя гликозилированием важных биоактивных белков до высокоманнозилированного состояния, можно жестко регулировать их уровни в сыворотке и направлять их специфично на клетки, экспрессирующие рецептор маннозы. Существует также возможность использования рецептора маннозы в качестве мишени для улучшения активации макрофагов и презентации антигена. [5] [8] [31]
MRC2/ Endo180 [32] взаимодействует с Basigin /CD147 через свой четвертый лектиновый домен C-типа, образуя комплекс-супрессор молекулярного эпителиально-мезенхимального перехода , который в случае разрушения приводит к индукции инвазивного поведения эпителиальных клеток простаты , связанного с плохой выживаемостью при раке простаты . [33] Повышенная жесткость базальной мембраны из-за ее гликирования также может вызвать Endo180 -зависимую инвазию эпителиальных клеток простаты , и этот биомеханический механизм связан с плохой выживаемостью при раке простаты . [34] Было высказано предположение, что стабилизация комплекса супрессора эпителиально-мезенхимального перехода Endo180-CD147 и нацеливание на некомплексную форму Endo180 в инвазивные клетки могут иметь терапевтическую пользу в предотвращении прогрессирования рака и метастазирования . [35]