Сиаловые кислоты представляют собой класс альфа-кетокислотных сахаров с девятиуглеродным остовом . [ 1] Термин «сиаловая кислота» (от греч. σίαλον (síalon) « слюна ») был впервые введен шведским биохимиком Гуннаром Бликсом в 1952 году. Наиболее распространенным членом этой группы является N -ацетилнейраминовая кислота (Neu5Ac или NANA), обнаруженная у животных и некоторых прокариот .
Сиаловые кислоты широко распространены в тканях животных, а родственные им формы в меньшей степени встречаются в других организмах, например, в некоторых микроводорослях , [2] бактериях и археях . [3] [4] [5] [6] Сиаловые кислоты обычно входят в состав гликопротеинов , гликолипидов или ганглиозидов , где они украшают концы сахарных цепей на поверхности клеток или растворимых белков. [7] Однако сиаловые кислоты также наблюдались в эмбрионах дрозофилы и других насекомых. [8] Обычно растения, по-видимому, не содержат и не демонстрируют сиаловые кислоты. [9]
У людей мозг имеет самое высокое содержание сиаловой кислоты, где эти кислоты играют важную роль в нейронной передаче и структуре ганглиозидов в синаптогенезе . [7] Известно более 50 видов сиаловой кислоты, все из которых могут быть получены из молекулы нейраминовой кислоты путем замены ее аминогруппы или одной из ее гидроксильных групп. [1] В общем, аминогруппа несет либо ацетильную, либо гликольильную группу, но были описаны и другие модификации. Эти модификации вместе со связями, как было показано, являются тканеспецифичными и регулируемыми в процессе развития выражениями , поэтому некоторые из них встречаются только на определенных типах гликоконъюгатов в определенных клетках. [8] Гидроксильные заместители могут значительно различаться; были обнаружены ацетил , лактил, метил , сульфат и фосфат группы. [10]
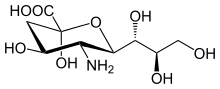
Семейство сиаловых кислот включает в себя множество производных девятиуглеродной сахарной нейраминовой кислоты , но эти кислоты редко встречаются в природе в свободном виде. Обычно их можно обнаружить в качестве компонентов олигосахаридных цепей муцинов, гликопротеинов и гликолипидов, занимающих терминальные, невосстанавливающие положения сложных углеводов как на внешних, так и на внутренних мембранных участках, где они очень уязвимы и развивают важные функции. [7]
Нумерация атомов углерода начинается с углерода карбоксилата и продолжается вдоль цепи. Конфигурация, которая помещает карбоксилат в аксиальное положение, называется альфа-аномером.
Альфа-аномер — это форма, которая обнаруживается, когда сиаловая кислота связана с гликанами. Однако в растворе она в основном (более 90%) находится в бета-аномерной форме. Был обнаружен бактериальный фермент с активностью мутаротазы сиаловой кислоты , NanM, который способен быстро уравновешивать растворы сиаловой кислоты до положения покоящегося равновесия около 90% бета/10% альфа. [11]
В отличие от других животных, люди генетически неспособны производить вариант сиаловой кислоты N-гликолилнейраминовой кислоты (Neu5Gc). Небольшие количества Neu5Gc, обнаруженные в тканях человека, однако, могут быть включены из экзогенных (питательных) источников. [12]
Сиаловая кислота синтезируется глюкозамин-6-фосфатом и ацетил-КоА через трансферазу , в результате чего образуется N - ацетилглюкозамин-6-P. Он становится N- ацетилманнозамин-6-P через эпимеризацию , которая реагирует с фосфоенолпируватом, образуя N -ацетилнейраминовый-9-P (сиаловую кислоту). Для того, чтобы он стал активным и вошел в процесс биосинтеза олигосахаридов в клетке, добавляется монофосфатный нуклеозид, который получается из цитидинтрифосфата , превращая сиаловую кислоту в цитидинмонофосфат-сиаловую кислоту (CMP-сиаловая кислота). Это соединение синтезируется в ядре животной клетки. [13] [14]
В бактериальных системах сиаловые кислоты также могут быть биосинтезированы альдолазой . Этот фермент использует, например, производное маннозы в качестве субстрата, вставляя три углерода из пирувата в полученную структуру сиаловой кислоты. Эти ферменты могут быть использованы для хемоферментативного синтеза производных сиаловой кислоты. [15]
Сиаловая кислота, содержащая гликопротеины ( сиалогликопротеины ), связывает селектин у людей и других организмов. Метастатические раковые клетки часто экспрессируют высокую плотность гликопротеинов, богатых сиаловой кислотой. Эта сверхэкспрессия сиаловой кислоты на поверхностях создает отрицательный заряд на клеточных мембранах. Это создает отталкивание между клетками (клеточное противостояние) [16] и помогает этим раковым клеткам поздней стадии проникать в кровоток. Недавние эксперименты продемонстрировали наличие сиаловой кислоты в секретируемом раком внеклеточном матриксе . [17]
Богатые сиаловой кислотой олигосахариды на гликоконъюгатах (гликолипиды, гликопротеины, протеогликаны), обнаруженные на поверхностных мембранах, помогают удерживать воду на поверхности клеток [ требуется ссылка ] . Области, богатые сиаловой кислотой, способствуют созданию отрицательного заряда на поверхности клеток. Поскольку вода является полярной молекулой с частичными положительными зарядами на обоих атомах водорода, она притягивается к поверхностям клеток и мембранам. Это также способствует поглощению клеточной жидкости.
Остатки сиаловой кислоты присутствуют в гликопротеинах муцина слизи. [18]
Сиаловая кислота может «скрывать» антигены маннозы на поверхности клеток-хозяев или бактерий от лектина, связывающего маннозу. [ необходима ссылка ] Это предотвращает активацию комплемента .
Сиаловая кислота в форме полисиаловой кислоты является необычной посттрансляционной модификацией , которая происходит на молекулах адгезии нейронных клеток (NCAM). В синапсе сильный отрицательный заряд полисиаловой кислоты предотвращает перекрестное связывание NCAM клеток.
Введение эстрогена кастрированным мышам приводит к дозозависимому снижению содержания сиаловой кислоты во влагалище. Наоборот, содержание сиаловой кислоты во влагалище мыши является мерой активности эстрогена. Референтными веществами являются эстрадиол для подкожного применения и этинилэстрадиол для перорального применения. [19]
Сиаловые кислоты обнаружены на поверхности всех клеток позвоночных и некоторых беспозвоночных, а также у некоторых бактерий, которые взаимодействуют с позвоночными.
Многие вирусы, такие как серотип Ad26 [20] аденовирусов ( Adenoviridae ), ротавирусов ( Reoviridae ) и вирусов гриппа ( Orthomyxoviridae ), могут использовать сиалилированные хозяином структуры для связывания с целевой клеткой-хозяином. Сиаловые кислоты являются хорошей мишенью для этих вирусов, поскольку они высококонсервативны и присутствуют в большом количестве практически во всех клетках. Неудивительно, что сиаловые кислоты также играют важную роль в нескольких вирусных инфекциях человека. Вирусы гриппа имеют на своей поверхности гликопротеины гемагглютининовой активности (HA), которые связываются с сиаловыми кислотами, обнаруженными на поверхности эритроцитов человека и на клеточных мембранах верхних дыхательных путей. Это основа гемагглютинации, когда вирусы смешиваются с клетками крови, и проникновения вируса в клетки верхних дыхательных путей. Широко используемые противогриппозные препараты ( осельтамивир и занамивир ) являются аналогами сиаловой кислоты, которые препятствуют высвобождению вновь образующихся вирусов из инфицированных клеток путем ингибирования вирусного фермента нейраминидазы . [21]
Некоторые бактерии также используют сиалилированные хозяином структуры для связывания и распознавания. Например, данные свидетельствуют о том, что свободные сиаловые кислоты могут вести себя как сигнал для некоторых специфических бактерий, таких как Pneumococcus . Свободная сиаловая кислота, возможно, может помочь бактерии распознать, что она достигла среды позвоночных, подходящей для ее колонизации. Модификации Sias, такие как N -гликолильная группа в 5-м положении или O -ацетильные группы в боковой цепи, могут снизить действие бактериальных сиалидаз. [21]
Синтез и деградация сиаловой кислоты распределены в различных компартментах клетки. Синтез начинается в цитозоле, где N -ацетилманнозамин- 6-фосфат и фосфоенолпируват дают начало сиаловой кислоте. Позже, Neu5Ac-9-фосфат активируется в ядре остатком цитидинмонофосфата (CMP) через CMP-Neu5Ac-синтазу. Хотя связь между сиаловой кислотой и другими соединениями, как правило, является α-связью, эта специфическая связь является единственной, которая является β-связью. Затем CMP-Neu5Ac транспортируется в эндоплазматический ретикулум или аппарат Гольджи, где он может быть перенесен в олигосахаридную цепь, становясь новым гликоконъюгатом. Эта связь может быть модифицирована путем O- ацетилирования или O- метилирования . Когда гликоконъюгат созревает, он транспортируется на поверхность клетки.
Сиалидаза является одним из важнейших ферментов катаболизма сиаловой кислоты. Она может вызывать удаление остатков сиаловой кислоты с поверхности клетки или сиалогликоконъюгатов сыворотки. Обычно у высших животных гликоконъюгаты, которые склонны к деградации, захватываются эндоцитозом. После слияния поздней эндосомы с лизосомой лизосомальные сиалидазы удаляют остатки сиаловой кислоты. Действие этих сиалидаз основано на удалении O - ацетильных групп. Свободные молекулы сиаловой кислоты транспортируются в цитозоль через мембрану лизосомы. Там они могут быть рециркулированы и снова активированы для образования другой зарождающейся молекулы гликоконъюгата в аппарате Гольджи. Сиаловые кислоты также могут быть деградированы до ацилманнозамина и пирувата с помощью цитозольного фермента ацилнейраминовой лиазы.
Некоторые тяжелые заболевания могут зависеть от наличия или отсутствия некоторых ферментов, связанных с метаболизмом сиаловой кислоты. Сиалидоз и дефицит сиаловой кислоты с мутациями в гене NANS (см. ниже) могут быть примерами этого типа расстройства. [22]
У крысят, которым давали сиаловую кислоту, во взрослом возрасте улучшились способности к обучению и память. [23] У поросят, которым давали высокие дозы сиаловой кислоты, была обнаружена связь между добавлением в рацион сиаловой кислоты и когнитивной функцией. [24]

Сиаловые кислоты связаны с несколькими различными заболеваниями, наблюдаемыми у людей.
Биаллельные рецессивные мутации в гене синтеза сиаловой кислоты, N-ацетил-нейраминовой кислоты синтазы ( NANS ) у людей могут привести к тяжелому заболеванию, характеризующемуся умственной отсталостью и низким ростом, что подчеркивает важность сиаловой кислоты в развитии мозга. [25] Терапевтическое испытание с краткосрочным добавлением сиаловой кислоты перорально не показало значительного положительного эффекта на биохимические параметры [26]
Болезнь Салла — чрезвычайно редкое заболевание, которое считается самой легкой формой нарушений накопления свободной сиаловой кислоты [27], хотя ее детская форма считается агрессивным вариантом, и люди, страдающие ею, имеют умственную отсталость. [ 28] Это аутосомно-рецессивное заболевание, вызванное мутацией хромосомы 6. [29] Оно в основном поражает нервную систему [27] и вызвано нарушением лизосомального хранения, которое возникает из-за дефицита специфического переносчика сиаловой кислоты, расположенного на лизосомальной мембране [30] В настоящее время не существует лекарства от этого заболевания, и лечение является поддерживающим, сосредоточенным на контроле симптомов. [27]
Субфракции холестерина ЛПНП, которые участвуют в возникновении атеросклероза, имеют пониженные уровни сиаловой кислоты. [31] К ним относятся небольшие частицы ЛПНП высокой плотности и электроотрицательные ЛПНП. [31] Пониженные уровни сиаловой кислоты в небольших частицах ЛПНП высокой плотности увеличивают сродство этих частиц к протеогликанам в стенках артерий . [31]
Всем штаммам вируса гриппа А нужна сиаловая кислота для связи с клетками. Существуют различные формы сиаловых кислот, которые имеют различное сродство к разновидности вируса гриппа А. Это разнообразие является важным фактом, определяющим, какие виды могут быть инфицированы. [32] Когда определенный вирус гриппа А распознается рецептором сиаловой кислоты, клетка стремится эндоцитировать вирус, в результате чего клетка становится инфицированной.
Сиаловые кислоты широко распространены в тканях позвоночных, где они участвуют во многих различных биологических процессах. Первоначально обнаруженные в родословной животных Deuterostome, сиаловые кислоты на самом деле можно рассматривать как подмножество более древнего семейства 9-углеродных моносахаридов, называемых нонулосоновыми кислотами (NulOs), которые совсем недавно были также обнаружены в Eubacteria и Archaea. [33] Многие патогенные бактерии включают сиаловую кислоту в такие особенности поверхности клеток, как их липополисахариды или капсульные полисахариды, что помогает им избегать врожденного иммунного ответа хозяина. [34] Недавнее исследование на уровне генома изучило большой набор секвенированных микробных геномов, которое показало, что биосинтетические пути для производства нонулосоновых кислот (NulOs) гораздо более широко распространены по филогенетическому древу жизни, чем считалось ранее. [35] Это открытие, кроме того, подтверждается недавними исследованиями окрашивания лектина и обзором на молекулярном уровне прокариотических нонулозоновых кислот, показывающими, что также многие непатогенные и чисто экологические штаммы производят бактериальные сиаловые кислоты (NulO). [36] [37] Некоторые ( anammox ) бактерии производят NulO, которые в дополнение к очень кислой альфа-кетокислотной группе также демонстрируют (нейтрализующие) основные группы (свободные амины). [38] Сопоставимые сиаловые кислоты клеточной поверхности были получены путем химического ремоделирования для управления зарядом клеточной поверхности путем производства свободного амина в C5, который нейтрализует отрицательно заряженную карбоксильную группу в C1. [39]
{{cite book}}: CS1 maint: DOI неактивен по состоянию на ноябрь 2024 г. ( ссылка ){{cite book}}: CS1 maint: DOI неактивен по состоянию на ноябрь 2024 г. ( ссылка ) CS1 maint: местоположение ( ссылка )