
В органической химии тиол ( / ˈ θ aɪ ɒ l / ; [1] от древнегреческого θεῖον (theion) ' сера ' [2] ), или производное тиола , представляет собой любое сероорганическое соединение формы R-SH , где R представляет собой алкил или другой органический заместитель . Сама функциональная группа -SH называется либо тиоловой группой , либо сульфгидрильной группой , либо сульфанильной группой . Тиолы представляют собой серный аналог спиртов (то есть сера заменяет кислород в гидроксильной ( -OH ) группе спирта), а это слово представляет собой смесь слов « тио- » и «спирт».
Многие тиолы имеют резкий запах, напоминающий запах чеснока или тухлых яиц. Тиолы используются в качестве одорантов для обнаружения природного газа (который в чистом виде не имеет запаха), а «запах природного газа» обусловлен запахом тиола, используемого в качестве одоранта. Тиолы иногда называют меркаптанами ( / m ər ˈ k æ p t æ n / ) [3] или меркаптосоединениями , [4] [5] [6] — термин, введенный в 1832 году Уильямом Кристофером Зейзе и происходящий от Латинское mercurio captāns («захватывающий ртуть») [7] , потому что тиолатная группа ( RS - ) очень прочно связывается с соединениями ртути . [8]
Тиолы, имеющие структуру R-SH, в которой алкильная группа (R) присоединена к сульфгидрильной группе (SH), называются алкантиолами или алкилтиолами . [9] Тиолы и спирты имеют схожие связи. Поскольку атомы серы больше атомов кислорода, длина связей C-S — обычно около 180 пикометров — примерно на 40 пикометров длиннее, чем типичные связи C-O. Углы C-S-H приближаются к 90 °, тогда как угол для группы C-O-H более тупой. В твердых телах и жидкостях водородные связи между отдельными тиоловыми группами слабы, причем основной силой сцепления являются ван-дер-ваальсовые взаимодействия между высокополяризуемыми центрами двухвалентной серы.
Связь S-H намного слабее, чем связь OH, что отражается в соответствующих энергиях диссоциации связей (BDE). Для CH 3 S-H БДЭ составляет 366 кДж/моль (87 ккал/моль), а для CH 3 O-H БДЭ составляет 440 кДж/моль (110 ккал/моль). [10]
Связь S-H умеренно полярна из-за небольшой разницы в электроотрицательности серы и водорода. Напротив, связи OH в гидроксильных группах более полярны. Тиолы имеют меньший дипольный момент по сравнению с соответствующими спиртами.
Существует несколько способов названия алкилтиолов:
Многие тиолы имеют сильный запах, напоминающий запах чеснока . Запахи тиолов, особенно низкомолекулярных, часто бывают сильными и отталкивающими. Спрей скунсов состоит в основном из низкомолекулярных тиолов и их производных. [11] [12] [13] [14] [15] Эти соединения обнаруживаются человеческим носом в концентрациях всего 10 частей на миллиард. [16] Человеческий пот содержит ( R )/( S )-3-метил-3-меркапто-1-ол (MSH), содержание которого определяется в концентрации 2 части на миллиард и имеет фруктовый луковый запах. (Метилтио)метантиол (MeSCH 2 SH; MTMT) представляет собой летучий тиол с сильным запахом, который также обнаруживается на уровне частей на миллиард и обнаруживается в моче самцов мышей . Лоуренс К. Кац и его коллеги показали, что MTMT действует как семиохимическое вещество , активируя определенные обонятельные сенсорные нейроны мышей, привлекая самок мышей . [17] Было показано, что медь необходима специфическому обонятельному рецептору мыши, MOR244-3, который очень чувствителен к MTMT, а также к различным другим тиолам и родственным соединениям. [18] Был идентифицирован обонятельный рецептор человека, OR2T11 , который в присутствии меди очень чувствителен к одорантам газа (см. ниже) этантиолу и т -бутилмеркаптану , а также другим низкомолекулярным тиолам, включая аллилмеркаптан. обнаружен в чесночном дыхании человека, а также сильно пахнущий циклический сульфид тиетан . [19]
Тиолы также ответственны за класс винных дефектов , вызванных непреднамеренной реакцией между серой и дрожжами и «вонючим» запахом пива, подвергшегося воздействию ультрафиолетового света.
Не все тиолы имеют неприятный запах. Например, фуран-2-илметантиол придает аромат жареного кофе , тогда как меркаптан грейпфрута , монотерпеноидный тиол, отвечает за характерный аромат грейпфрута . Эффект последнего соединения присутствует только при низких концентрациях. Чистый меркаптан имеет неприятный запах.
В Соединенных Штатах дистрибьюторы природного газа были обязаны добавлять тиолы, первоначально этантиол , в природный газ (который, естественно, не имеет запаха) после смертельного взрыва в Нью-Лондонской школе в Нью-Лондоне, штат Техас , в 1937 году. это событие. Большинство используемых в настоящее время одорантов газа содержат смеси меркаптанов и сульфидов, при этом т- бутилмеркаптан является основным компонентом запаха в природном газе и этантиолом в сжиженном нефтяном газе (СНГ, пропан). [20] В ситуациях, когда тиолы используются в коммерческой промышленности, например, в танкерах для сжиженного нефтяного газа и системах погрузки-разгрузки, для уничтожения запаха используется окислительный катализатор . Катализатор окисления на основе меди нейтрализует летучие тиолы и превращает их в инертные продукты.
Тиолы слабо связаны водородными связями как с молекулами воды, так и между собой. Следовательно, они имеют более низкие температуры кипения и менее растворимы в воде и других полярных растворителях , чем спирты с аналогичной молекулярной массой. По этой же причине тиолы и соответствующие изомеры их сульфидных функциональных групп имеют сходные характеристики растворимости и температуры кипения, тогда как этого нельзя сказать о спиртах и соответствующих им изомерных простых эфирах.
Связь S-H в тиолах слаба по сравнению со связью O-H в спиртах. Для CH 3 X−H энтальпии связи равны365,07 ± 2,1 ккал/моль для X = S и440,2 ± 3,0 ккал/моль для X = O. [21] Отщепление атома водорода от тиола дает тиильный радикал с формулой RS • , где R = алкил или арил.
Летучие тиолы легко и почти безошибочно обнаруживаются по характерному запаху. Полезны анализаторы серы для газовых хроматографов . Спектроскопическими индикаторами являются D 2 O -обменный сигнал SH в спектре 1 H ЯМР ( 33 S является ЯМР -активным, но сигналы для двухвалентной серы очень широки и малополезны [22] ). Полоса νSH появляется в ИК-спектре вблизи 2400 см -1 . [4] В реакции нитропруссида свободные тиоловые группы реагируют с нитропруссидом натрия и гидроксидом аммония , образуя красный цвет.
В промышленности метантиол получают реакцией сероводорода с метанолом . Этот метод используется для промышленного синтеза метантиола :
Такие реакции проводятся в присутствии кислотных катализаторов. Другой основной путь получения тиолов включает присоединение сероводорода к алкенам . Такие реакции обычно проводятся в присутствии кислотного катализатора или УФ-света. Также использовалось замещение галогенидов с использованием подходящего органического галогенида и гидросульфида натрия. [23]
Другой метод предполагает алкилирование гидросульфида натрия .
Этот метод используется для производства тиогликолевой кислоты из хлоруксусной кислоты .
В целом в типичном лабораторном масштабе прямая реакция галогеналкана с гидросульфидом натрия неэффективна из-за конкурирующего образования сульфидов. Вместо этого алкилгалогениды превращаются в тиолы посредством S -алкилирования тиомочевины . Этот многоэтапный однореакторный процесс протекает через посредство изотиурониевой соли , которая гидролизуется на отдельной стадии: [24] [25]
Путь тиомочевины хорошо работает с первичными галогенидами, особенно с активированными. Вторичные и третичные тиолы получить труднее. Вторичные тиолы можно получить из кетона через соответствующие дитиокетали . [26] Похожий двухэтапный процесс включает алкилирование тиосульфата с образованием тиосульфоната (« соль Бунте ») с последующим гидролизом. Метод иллюстрируется одним синтезом тиогликолевой кислоты :
Литийорганические соединения и реактивы Гриньяра реагируют с серой с образованием тиолатов, которые легко гидролизуются: [27]
Фенолы можно превратить в тиофенолы путем перегруппировки их O -арилдиалкилтиокарбаматов. [28]
Тиолы получают восстановительным деалкилированием сульфидов, особенно бензильных производных и тиоацеталей. [29]
Тиофенолы получают S -арилированием или заменой уходящей группы диазония сульфгидрильным анионом (SH- ) : [30] [31]
Подобно химии спиртов, тиолы образуют сульфиды , тиоацетали и тиоэфиры , которые аналогичны простым эфирам , ацеталям и сложным эфирам соответственно. Тиолы и спирты также сильно различаются по своей реакционной способности: тиолы легче окисляются, чем спирты. Тиолаты являются более сильными нуклеофилами, чем соответствующие алкоксиды .
Тиолы, или, точнее, сопряженные с ними основания, легко алкилируются с образованием сульфидов:
Тиолы легко депротонируются. [32] По сравнению со спиртами тиолы более кислые. Сопряженное основание тиола называется тиолатом . Бутантиол имеет P K a 10,5 против 15 у бутанола. Тиофенол имеет p K a 6 по сравнению с 10 для фенола . Сильнокислым тиолом является пентафтортиофенол (C 6 F 5 SH) с ap K a 2,68. Так, тиолаты можно получать из тиолов обработкой гидроксидами щелочных металлов.

Тиолы, особенно в присутствии основания, легко окисляются такими реагентами, как бром и йод , с образованием органического дисульфида (R-S-S-R).
Окисление более мощными реагентами, такими как гипохлорит натрия или перекись водорода, также может давать сульфоновые кислоты (RSO 3 H).
Окисление может осуществляться и кислородом в присутствии катализаторов: [33]
Тиолы участвуют в тиол-дисульфидном обмене:
Эта реакция важна в природе.
С ионами металлов тиолаты ведут себя как лиганды, образуя тиолатные комплексы переходных металлов . Термин «меркаптан» происходит от латинского mercurium captans (захватывающий ртуть) [7] , поскольку тиолатная группа очень прочно связывается с соединениями ртути . Согласно теории «жесткая/мягкая кислота/основание» (HSAB) , сера является относительно мягким (поляризующимся) атомом. Это объясняет склонность тиолов связываться с мягкими элементами и ионами, такими как ртуть, свинец или кадмий. Стабильность тиолатов металлов аналогична стабильности соответствующих сульфидных минералов.
Тиолаты реагируют с сероуглеродом с образованием тиоксантогената ( RSCS−
2).
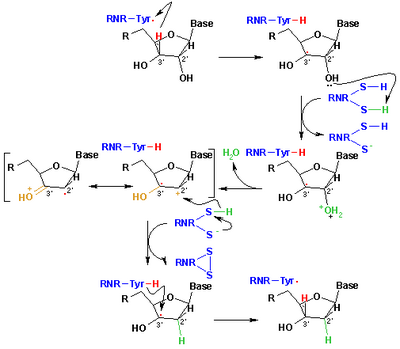
Свободные радикалы , полученные из меркаптанов, называемые тиильными радикалами , обычно используются для объяснения реакций в органической химии и биохимии . Они имеют формулу RS • где R представляет собой органический заместитель, такой как алкил или арил . [6] Они возникают или могут быть созданы различными путями, но основным методом является абстракция атома водорода от тиолов. Другой метод включает гомолиз органических дисульфидов. [34] В биологии тиильные радикалы ответственны за образование дезоксирибонуклеиновых кислот, строительных блоков ДНК . Это превращение катализируется рибонуклеотидредуктазой (см. рисунок). [35] Тиильные промежуточные соединения также производятся путем окисления глутатиона , антиоксиданта в биологии. Тиильные радикалы (сероцентрированные) могут превращаться в углеродцентрированные радикалы посредством равновесия обмена атомов водорода . Образование углеродцентрированных радикалов может привести к повреждению белка за счет образования связей C -C или фрагментации основной цепи. [36]
Из-за слабости связи S-H тиолы могут действовать как поглотители свободных радикалов . [37]
Как функциональная группа аминокислоты цистеина , тиоловая группа играет очень важную роль в биологии. Когда тиоловые группы двух остатков цистеина (как в мономерах или составляющих единицах) приближаются друг к другу в ходе сворачивания белка , реакция окисления может привести к образованию цистиновой единицы с дисульфидной связью (-S-S-). Дисульфидные связи могут вносить вклад в третичную структуру белка, если цистеины являются частью одной и той же пептидной цепи, или вносить вклад в четвертичную структуру многозвенных белков, образуя довольно прочные ковалентные связи между различными пептидными цепями. Физическое проявление цистеин-цистинового равновесия обеспечивают технологии выпрямления волос . [38]
Сульфгидрильные группы в активном центре фермента также могут образовывать нековалентные связи с субстратом фермента , способствуя ковалентной каталитической активности в каталитических триадах . Остатки цистеина в активном центре являются функциональной единицей каталитических триад цистеиновых протеаз . Остатки цистеина могут также реагировать с ионами тяжелых металлов (Zn 2+ , Cd 2+ , Pb 2+ , Hg 2+ , Ag + ) из-за высокого сродства между мягким сульфидом и мягким металлом (см. твердые и мягкие кислоты и основания). ). Это может деформировать и инактивировать белок и является одним из механизмов отравления тяжелыми металлами .
Препараты, содержащие тиоловую группу 6-Меркаптопурин (противораковый) Каптоприл (антигипертензивный) D-пеницилламин (противоартритный) Ауротиолат натрия (противоартритный) [39]
Многие кофакторы (небелковые вспомогательные молекулы) содержат тиолы. Биосинтез и деградация жирных кислот и родственных длинноцепочечных углеводородов проводятся на каркасе, который закрепляет растущую цепь с помощью тиоэфира, полученного из тиолового коэнзима А. Биосинтез метана , основного углеводорода на Земле, возникает в результате реакции, опосредованной коферментом М , 2-меркаптоэтилсульфоновой кислотой. Тиолаты, сопряженные основания, полученные из тиолов, образуют прочные комплексы со многими ионами металлов, особенно с теми, которые относятся к мягким. Стабильность тиолатов металлов аналогична стабильности соответствующих сульфидных минералов.
Защитный спрей скунсов состоит в основном из низкомолекулярных тиолов и их производных с неприятным запахом, что защищает скунса от хищников. Совы способны охотиться на скунсов, так как у них отсутствует обоняние. [40]
{{cite journal}}: CS1 maint: multiple names: authors list (link); Коллективный том , том. 8, с. 302Сульфгидрилы являются поглотителями свободных радикалов, защищая от химического повреждения, вызванного ионизирующим излучением или алкилирующими агентами.