Доставка генов — это процесс введения чужеродного генетического материала, такого как ДНК или РНК , в клетки- хозяева . [1] Доставка генов должна достичь генома клетки-хозяина, чтобы вызвать экспрессию генов . [2] Успешная доставка генов требует, чтобы доставка чужеродного гена оставалась стабильной внутри клетки-хозяина и могла либо интегрироваться в геном , либо реплицироваться независимо от него. [3] Для этого требуется, чтобы чужеродная ДНК была синтезирована как часть вектора , который предназначен для проникновения в нужную клетку-хозяина и доставки трансгена в геном этой клетки. [4] Векторы, используемые в качестве метода доставки генов, можно разделить на две категории: рекомбинантные вирусы и синтетические векторы (вирусные и невирусные). [2] [5]
В сложных многоклеточных эукариотах (точнее, вейсманистах ), если трансген включен в зародышевые клетки хозяина , полученная клетка хозяина может передать трансген своему потомству . Если трансген включен в соматические клетки, трансген останется с соматической клеточной линией, и, таким образом, с организмом хозяина. [6]
Доставка генов является необходимым шагом в генной терапии для введения или подавления гена для содействия терапевтическому результату у пациентов, а также имеет применение в генетической модификации сельскохозяйственных культур. Существует много различных методов доставки генов для различных типов клеток и тканей. [6]
Векторы на основе вирусов появились в 1980-х годах как инструмент для экспрессии трансгенов. В 1983 году Альберт Сигел описал использование вирусных векторов для экспрессии трансгенов растений, хотя вирусная манипуляция посредством клонирования кДНК еще не была доступна. [7] Первым вирусом, который был использован в качестве вектора вакцины, был вирус коровьей оспы в 1984 году как способ защиты шимпанзе от гепатита B. [ 8] О невирусной доставке генов впервые сообщили в 1943 году Эвери и др., которые показали изменение клеточного фенотипа посредством воздействия экзогенной ДНК . [9]

Существует множество методов доставки генов в клетки-хозяева. Когда гены доставляются в бактерии или растения, этот процесс называется трансформацией , а когда он используется для доставки генов животным, он называется трансфекцией . Это связано с тем, что трансформация имеет другое значение по отношению к животным, указывая на прогрессирование в раковое состояние. [10] Для некоторых бактерий не нужны внешние методы для введения генов, поскольку они естественным образом способны поглощать чужеродную ДНК . [11] Большинству клеток требуется какое-то вмешательство, чтобы сделать клеточную мембрану проницаемой для ДНК и позволить ДНК стабильно встраиваться в геном хозяина .
Химические методы доставки генов могут использовать природные или синтетические соединения для формирования частиц, которые облегчают перенос генов в клетки. [2] Эти синтетические векторы обладают способностью электростатически связывать ДНК или РНК и уплотнять генетическую информацию для размещения более крупных генетических переносов. [5] Химические векторы обычно проникают в клетки путем эндоцитоза и могут защищать генетический материал от деградации. [6]
Один из самых простых методов заключается в изменении среды клетки, а затем в ее стрессе путем теплового шока . Обычно клетки инкубируют в растворе, содержащем двухвалентные катионы (часто хлорид кальция ) в условиях холода, перед тем как подвергать их тепловому импульсу. Хлорид кальция частично разрушает клеточную мембрану, что позволяет рекомбинантной ДНК проникнуть в клетку-хозяина. Предполагается, что воздействие двухвалентных катионов на клетки в условиях холода может изменить или ослабить структуру поверхности клетки, сделав ее более проницаемой для ДНК. Считается, что тепловой импульс создает тепловой дисбаланс через клеточную мембрану, что заставляет ДНК проникать в клетки либо через поры клетки, либо через поврежденную клеточную стенку.
Другой простой метод включает использование фосфата кальция для связывания ДНК и последующее воздействие на культивируемые клетки. Раствор вместе с ДНК инкапсулируется клетками , и небольшое количество ДНК может быть интегрировано в геном. [12]
Липосомы и полимеры могут использоваться в качестве векторов для доставки ДНК в клетки. Положительно заряженные липосомы связываются с отрицательно заряженной ДНК, в то время как полимеры могут быть разработаны для взаимодействия с ДНК. [2] Они образуют липоплексы и полиплексы соответственно, которые затем поглощаются клетками. [13] Эти две системы также могут быть объединены. [6] Невирусные векторы на основе полимеров используют полимеры для взаимодействия с ДНК и образования полиплексов. [6]
Использование искусственных неорганических и органических наночастиц является еще одним невирусным подходом к доставке генов. [14] [15]
Искусственная доставка генов может быть осуществлена с помощью физических методов, которые используют силу для введения генетического материала через клеточную мембрану. [2]

Электропорация — это метод повышения компетентности . Клетки подвергаются кратковременному шоку электрическим полем напряженностью 10-20 кВ /см, что, как полагают, создает отверстия в клеточной мембране, через которые может проникнуть плазмидная ДНК. После электрошока отверстия быстро закрываются механизмами восстановления мембраны клетки.

Другой метод, используемый для трансформации растительных клеток, — это биолистика , где частицы золота или вольфрама покрываются ДНК, а затем выстреливаются в молодые растительные клетки или растительные эмбрионы. [16] Некоторый генетический материал проникает в клетки и трансформирует их. Этот метод можно использовать на растениях, которые не восприимчивы к инфекции Agrobacterium , а также позволяет трансформировать растительные пластиды . Растительные клетки также можно трансформировать с помощью электропорации, которая использует электрический шок, чтобы сделать клеточную мембрану проницаемой для плазмидной ДНК. Из-за повреждения, наносимого клеткам и ДНК, эффективность трансформации биолистики и электропорации ниже, чем агробактериальной трансформации. [17]
Микроинъекция – это процесс, при котором ДНК вводится через ядерную оболочку клетки непосредственно в ядро . [11]
Сонопорация — это кратковременное проникновение через клеточные мембраны с помощью ультразвука , как правило, в присутствии газовых микропузырьков . [18] Сонопорация позволяет проникать генетическому материалу в клетки. [19] [20]
Фотопорация — это процесс, при котором лазерные импульсы используются для создания пор в клеточной мембране, через которые проникает генетический материал.
Магнитофекция использует магнитные частицы, соединенные с ДНК, а внешнее магнитное поле концентрирует частицы нуклеиновой кислоты в клетках-мишенях.
Гидродинамический капиллярный эффект можно использовать для управления проницаемостью клеток.
В растениях ДНК часто вставляется с помощью рекомбинации, опосредованной Agrobacterium , [21] используя последовательность T-ДНК Agrobacterium , которая позволяет естественным образом вставлять генетический материал в растительные клетки. [22] Растительная ткань разрезается на небольшие кусочки и замачивается в жидкости, содержащей суспендированную Agrobacterium . Бактерии прикрепляются ко многим растительным клеткам, обнажаемым надрезами. Бактерии используют конъюгацию для переноса сегмента ДНК, называемого T-ДНК, из своей плазмиды в растение. Перенесенная ДНК направляется в ядро растительной клетки и интегрируется в геномную ДНК растения-хозяина. Плазмидная T-ДНК интегрируется полуслучайным образом в геном клетки-хозяина. [23]
Модифицируя плазмиду для экспрессии интересующего гена, исследователи могут стабильно вставлять выбранный ими ген в геном растения. Единственными существенными частями Т-ДНК являются ее два небольших (25 пар оснований) пограничных повтора, по крайней мере один из которых необходим для трансформации растения. [24] [25] Гены, которые должны быть введены в растение, клонируются в вектор трансформации растения , который содержит область Т-ДНК плазмиды . Альтернативным методом является агроинфильтрация . [26] [27]
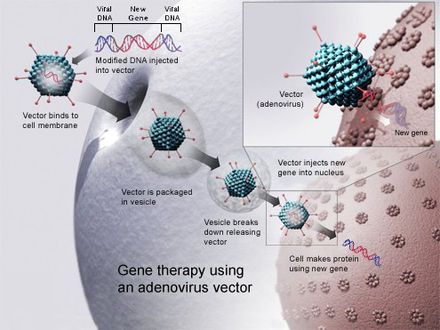
Вирусопосредованная доставка генов использует способность вируса вводить свою ДНК внутрь клетки-хозяина и использует собственную способность вируса реплицироваться и внедрять свой собственный генетический материал. Вирусные методы доставки генов с большей вероятностью вызывают иммунный ответ, но они обладают высокой эффективностью. [6] Трансдукция — это процесс, который описывает вирусопосредованную вставку ДНК в клетку-хозяина. Вирусы являются особенно эффективной формой доставки генов, поскольку структура вируса предотвращает деградацию через лизосомы ДНК, которую он доставляет в ядро клетки-хозяина. [28] В генной терапии ген, предназначенный для доставки, упаковывается в вирусную частицу с дефектом репликации для формирования вирусного вектора . [29] Вирусы, используемые для генной терапии на сегодняшний день, включают ретровирус, аденовирус, аденоассоциированный вирус и вирус простого герпеса. Однако существуют недостатки использования вирусов для доставки генов в клетки. Вирусы могут доставлять в клетки только очень маленькие фрагменты ДНК, это трудоемкий процесс, и существуют риски случайных мест вставки, цитопатических эффектов и мутагенеза. [30]
Доставка генов на основе вирусного вектора использует вирусный вектор для доставки генетического материала в клетку-хозяина. Это делается с помощью вируса, содержащего нужный ген, и удаления части генома вируса, которая является инфекционной. [2] Вирусы эффективны в доставке генетического материала в ядро клетки-хозяина, что жизненно важно для репликации. [2]
Вирусы на основе РНК были разработаны из-за возможности транскрибировать напрямую с инфекционных РНК-транскриптов. Векторы РНК быстро экспрессируются и экспрессируются в целевой форме, поскольку не требуется никакой обработки [необходим источник]. Ретровирусные векторы включают онкоретровирусный, лентивирусный и пенистый вирус человека , являются вирусными векторами на основе РНК, которые осуществляют обратную транскрипцию и интегрируются в геном хозяина, что обеспечивает долгосрочную экспрессию трансгена. [2]
Вирусные векторы на основе ДНК включают Adenoviridae , аденоассоциированный вирус и вирус простого герпеса . [2]
Некоторые из методов, используемых для облегчения доставки генов, имеют применение в терапевтических целях. Генная терапия использует доставку генов для доставки генетического материала с целью лечения заболевания или состояния в клетке. Доставка генов в терапевтических условиях использует неиммуногенные векторы , способные к клеточной специфичности, которые могут доставлять достаточное количество экспрессии трансгена, чтобы вызвать желаемый эффект. [3]
Достижения в области геномики позволили идентифицировать множество новых методов и генных мишеней для возможных приложений. ДНК-микрочипы, используемые в различных методах секвенирования следующего поколения, могут одновременно идентифицировать тысячи генов, с аналитическим программным обеспечением, изучающим паттерны экспрессии генов, и ортологичными генами в модельных видах для идентификации функции. [31] Это позволило идентифицировать множество возможных векторов для использования в генной терапии. В качестве метода создания нового класса вакцин доставка генов использовалась для создания гибридного биосинтетического вектора для доставки возможной вакцины. Этот вектор преодолевает традиционные барьеры для доставки генов, объединяя E. coli с синтетическим полимером для создания вектора, который поддерживает плазмидную ДНК, имея при этом повышенную способность избегать деградации лизосомами целевых клеток. [32]
{{cite book}}: CS1 maint: location (link)