Ферроцен представляет собой металлоорганическое соединение формулы Fe(C 5 H 5 ) 2 . Молекула представляет собой комплекс , состоящий из двух циклопентадиенильных колец, между которыми находится центральный атом железа . Это оранжевое твердое вещество с запахом камфоры, которое сублимируется при температуре выше комнатной и растворимо в большинстве органических растворителей. Он отличается своей стабильностью: не подвержен воздействию воздуха, воды, сильных оснований и может нагреваться до 400 °C без разложения. В окислительных условиях может обратимо реагировать с сильными кислотами с образованием катиона ферроцения Fe(C 5 H 5 ).+2. [7] Ферроцен и катион ферроцения иногда обозначаются сокращенно Fc и Fc + соответственно.
Впервые о синтезе ферроцена сообщалось в 1951 году. Его необычная стабильность озадачила химиков и потребовала разработки новой теории для объяснения его образования и связывания. Открытие ферроцена и его многочисленных аналогов , известных как металлоцены , вызвало волнение и привело к быстрому развитию дисциплины металлоорганической химии . Джеффри Уилкинсон и Эрнст Отто Фишер , оба работавшие над выяснением структуры ферроцена, позже получили Нобелевскую премию по химии 1973 года за работу над металлоорганическими сэндвич-соединениями. Сам по себе ферроцен не имеет крупномасштабного применения, но нашел более нишевое применение в катализе, в качестве топливной добавки и в качестве инструмента в высшем образовании.
Ферроцен был обнаружен случайно дважды. Первый известный синтез, возможно, был осуществлен в конце 1940-х годов неизвестными исследователями из Union Carbide , которые пытались пропустить горячие пары циклопентадиена через железную трубу. Пар вступил в реакцию со стенками трубы, образовав «желтый осадок», который засорил трубу. Спустя годы образец сохраненного ила был получен и проанализирован Юджином О. Бриммом вскоре после прочтения статьи Кили и Посона, и было обнаружено, что он состоит из ферроцена. [7] [8]
Второй раз произошел примерно в 1950 году, когда Сэмюэл А. Миллер, Джон А. Теббот и Джон Ф. Тремейн, исследователи из British Oxygen , пытались синтезировать амины из углеводородов и азота в модификации процесса Габера . Когда они попытались прореагировать циклопентадиен с азотом при 300 °C и атмосферном давлении, они были разочарованы, увидев, что углеводород реагирует с каким-то источником железа, образуя ферроцен. Хотя они тоже отметили его замечательную стабильность, они отложили это наблюдение и не публиковали его до тех пор, пока Паусон не сообщил о своих выводах. [7] [9] [10] Позже Миллер и др. предоставили Кили и Паусону образец . , который подтвердил, что продукты представляют собой одно и то же соединение. [8]
В 1951 году Питер Л. Паусон и Томас Дж. Кили из Университета Дюкен попытались получить фульвален ( (C 5 H 4 ) 2 ) путем окислительной димеризации циклопентадиена ( C 5 H 6 ). С этой целью они провели реакцию соединения Гриньяра циклопентадиенилмагния бромида в диэтиловом эфире с хлоридом железа в качестве окислителя. [7] Однако вместо ожидаемого фульвалена они получили светло-оранжевый порошок «замечательной стабильности» с формулой C 10 H 10 Fe . [8] [11]

Паусон и Кили предположили, что это соединение имеет две циклопентадиенильные группы, каждая из которых имеет одну ковалентную связь от насыщенного атома углерода к атому железа. [7] Однако эта структура не соответствовала существовавшим на тот момент моделям связи и не объясняла неожиданную стабильность соединения, и химики изо всех сил пытались найти правильную структуру. [10] [12]
Структура была выведена и сообщена независимо тремя группами в 1952 году. [13] Роберт Бернс Вудворд и Джеффри Уилкинсон вывели ее, наблюдая, что ферроцен подвергается реакциям, типичным для ароматических соединений, таких как бензол . [14] Эрнст Отто Фишер и Вольфганг Пфаб отметили, что соединение было диамагнитным и центросимметричным, а также синтезировали никельоцен и кобальтоцен и подтвердили, что они имеют одинаковую структуру. [15] Фишер описал эту структуру как Doppelkegelstruktur («структура с двойным конусом»), хотя британские и американские химики предпочитали термин «сэндвич». [16] Филип Франк Эйланд и Раймонд Пепински подтвердили структуру с помощью рентгеновской кристаллографии , а затем с помощью ЯМР . [10] [17] [18] [19]
«Сэндвич»-структура ферроцена была шокирующе новой и требовала новой теории для объяснения. Применение теории молекулярных орбиталей в предположении наличия центра Fe 2+ между двумя циклопентадиенидными анионами C 5 H−5привели к созданию успешной модели Дьюара-Чатта-Дункансона , позволяющей правильно предсказать геометрию молекулы, а также объяснить ее замечательную стабильность. [20] [21]
Ферроцен не был первым открытым металлоорганическим соединением. О соли Цейзе K[PtCl 3 (C 2 H 4 )]·H 2 O сообщалось в 1831 году, [22] [23] Эдвард Франкланд синтезировал диэтилцинк и другие подобные соединения в 1848 году, открытие Мондом Ni(CO) 4 произошло в 1888 году. , [24] и литийорганические соединения были разработаны в 1930-х годах. [25] Однако можно утверждать, что именно открытие ферроцена положило начало металлоорганической химии как отдельной области химии. Это также привело к взрывному интересу к соединениям металлов d-блока с углеводородами. Это открытие было сочтено настолько значительным, что Уилкинсон и Фишер получили Нобелевскую премию по химии 1973 года «за новаторскую работу, выполненную независимо, по химии металлоорганических соединений, называемых сэндвичевыми соединениями ». [26]
Мессбауэровская спектроскопия показывает, что железному центру в ферроцене следует приписать степень окисления +2. Тогда каждому циклопентадиенильному (Cp) кольцу должен быть присвоен один отрицательный заряд. Таким образом, ферроцен можно описать как бис( циклопентадиенид железа(II) , Fe 2+ [C 5 H−5] 2 .
Каждое кольцо имеет шесть π-электронов, что делает их ароматическими согласно правилу Хюккеля . Эти π-электроны затем делятся с металлом посредством ковалентной связи. Поскольку Fe 2+ имеет шесть d -электронов, комплекс приобретает 18-электронную конфигурацию, что обеспечивает его стабильность. В современных обозначениях эта сэндвич-структурная модель молекулы ферроцена обозначается как Fe( η 5 -C 5 H 5 ) 2 , где η обозначает гаптичность , количество атомов, посредством которых связывается каждое кольцо.
Все расстояния связей углерод-углерод вокруг каждого пятичленного кольца составляют 1,40 Å, а все расстояния связей Fe-C составляют 2,04 Å. От комнатной температуры до 164 К рентгеновская кристаллография дает моноклинную пространственную группу; циклопентадиенидные кольца представляют собой шахматную конформацию, в результате чего образуется центросимметричная молекула с группой симметрии D 5d . [17] Однако ниже 110 К ферроцен кристаллизуется в ромбической кристаллической решетке, в которой кольца Cp упорядочены и затмеваются, так что молекула имеет группу симметрии D 5h . [27] В газовой фазе электронограмма [28] и компьютерные исследования [29] показывают, что Cp-кольца затмеваются. Хотя ферроцен не имеет постоянного дипольного момента при комнатной температуре, между 172,8 и 163,5 К молекула демонстрирует «несоизмеримую модуляцию», нарушая симметрию D 5 и приобретая электрический диполь. [30]
Кольца Cp вращаются с низким барьером вокруг оси Cp (центроид) –Fe–Cp (центроид) , как наблюдают измерения на замещенных производных ферроцена с помощью спектроскопии ядерного магнитного резонанса 1 H и 13 C. Например, метилферроцен (CH 3 C 5 H 4 FeC 5 H 5 ) имеет синглет кольца C 5 H 5 . [31]
Было установлено , что в растворе и при комнатной температуре затменный ферроцен D 5h доминирует над расположенным в шахматном порядке конформером D 5d , как предполагают как инфракрасная спектроскопия с преобразованием Фурье , так и расчеты DFT . [32]
В промышленности ферроцен синтезируют реакцией этоксида железа (II) с циклопентадиеном; [33] необходимый этоксид железа(II) получают электрохимическим окислением металлического железа в безводном этаноле . Поскольку реакция между этилатом железа(II) и циклопентадиеном приводит к образованию этанола в качестве побочного продукта, этанол эффективно служит катализатором всей реакции, при этом конечная реакция представляет собой Fe + 2C 5 H 6 → H 2 + Fe(C 5 H 5 ) 2 (см. также ниже)
Первые сообщения о синтезе ферроцена произошли почти одновременно. Паусон и Кили синтезировали ферроцен, используя хлорид железа (III) и реактив Гриньяра, циклопентадиенилмагний бромид. Хлорид железа(III) суспендируют в безводном диэтиловом эфире и добавляют к реактиву Гриньяра. [11] Происходит окислительно -восстановительная реакция с образованием циклопентадиенильного радикала и ионов железа(II). Дигидрофульвален образуется в результате радикально-радикальной рекомбинации, в то время как железо (II) реагирует с реактивом Гриньяра с образованием ферроцена. Окисления дигидрофульвалена до фульвалена железом (III), которого добивались Кили и Паусон, не происходит. [8]

Другой ранний синтез ферроцена был осуществлен Миллером и др. , [9] которые непосредственно реагировали металлическое железо с газофазным циклопентадиеном при повышенной температуре. [34] Также сообщалось о подходе с использованием пентакарбонила железа . [35]
Более эффективные препаративные методы обычно представляют собой модификацию исходной последовательности трансметаллирования с использованием либо коммерчески доступного циклопентадиенида натрия [36], либо свежекрекингового циклопентадиена, депротонированного гидроксидом калия [37] и подвергнутого реакции с безводным хлоридом железа (II) в эфирных растворителях.
Известны современные модификации оригинального подхода Гриньяра Посона и Кили:
Для депротонирования можно использовать даже некоторые аминные основания (например, диэтиламин ), хотя реакция протекает медленнее, чем при использовании более сильных оснований: [36]
Прямое трансметаллирование также можно использовать для получения ферроцена из других металлоценов, таких как манганоцен : [38]

Ферроцен представляет собой устойчивое на воздухе твердое вещество оранжевого цвета с запахом камфоры. Как и ожидалось для симметричных незаряженных частиц, ферроцен растворим в обычных органических растворителях, таких как бензол, но нерастворим в воде. Он устойчив к температурам до 400°C. [39]
Ферроцен легко сублимируется , особенно при нагревании в вакууме. Давление его пара составляет около 1 Па при 25 °C, 10 Па при 50 °C, 100 Па при 80 °C, 1000 Па при 116 °C и 10 000 Па (около 0,1 атм ) при 162 °C. [40] [41]
Ферроцен вступает во многие реакции, характерные для ароматических соединений, что позволяет получать замещенные производные. Обычным студенческим экспериментом является реакция Фриделя-Крафтса ферроцена с уксусным ангидридом (или ацетилхлоридом ) в присутствии фосфорной кислоты в качестве катализатора. В условиях реакции Манниха ферроцен дает N,N-диметиламинометилферроцен .
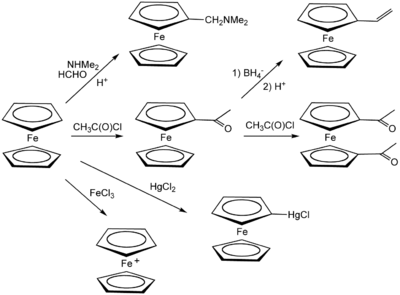
Сам ферроцен можно использовать в качестве основной цепи лиганда, например 1,1'-бис(дифенилфосфино)ферроцена (dppf). Ферроцен сам по себе может окисляться до катиона ферроцения (Fc + ); пара ферроцен/ферроцений часто используется в качестве эталона в электрохимии. [12]
Это ароматическое вещество , которое претерпевает реакции замещения , а не реакции присоединения циклопентадиенильных лигандов. Например, ацилирование ферроцена по Фриделю-Крафтсу уксусным ангидридом дает ацетилферроцен [42], так же как ацилирование бензола в аналогичных условиях дает ацетофенон .
Протонирование ферроцена позволяет выделить [Cp 2 FeH]PF 6 . [43]
В присутствии хлорида алюминия Me 2 NPCl 2 и ферроцен реагируют с образованием ферроценилдихлорфосфина [44] , тогда как при обработке фенилдихлорфосфином в аналогичных условиях образуется P , P -диферроценил- P -фенилфосфин. [45]
Ферроцен реагирует с P 4 S 10 , образуя диферроценилдитиадифосфетандисульфид. [46]
Ферроцен реагирует с бутиллитием с образованием 1,1'-дилитиоферроцена , который является универсальным нуклеофилом . В сочетании с бутиллитием трет -бутиллитий образует монолитиоферроцен. [47]
Ферроцен подвергается одноэлектронному окислению при напряжении около 0,4 В по сравнению с насыщенным каломельным электродом (SCE), превращаясь в ферроцений . Это обратимое окисление использовалось в качестве стандарта в электрохимии при Fc + /Fc = 0,64 В по сравнению со стандартным водородным электродом [48] , однако сообщалось и о других значениях. [49] Тетрафторборат ферроцения является распространенным реагентом. [50] Удивительно обратимое окислительно-восстановительное поведение широко используется для управления процессами переноса электрона в электрохимических [51] [52] и фотохимических [53] [54] системах.
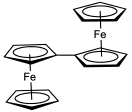
Заместители в циклопентадиенильных лигандах изменяют окислительно-восстановительный потенциал ожидаемым образом: электроноакцепторные группы, такие как карбоновая кислота, смещают потенциал в анодном направлении ( т.е. делают его более положительным), тогда как электроноотдающие группы, такие как метильные группы, сдвигают потенциал в катодное направление (более отрицательное). Таким образом, декаметилферроцен гораздо легче окисляется, чем ферроцен, и даже может окисляться до соответствующего дикатиона. [55] Ферроцен часто используется в качестве внутреннего стандарта для калибровки окислительно-восстановительных потенциалов в неводной электрохимии .
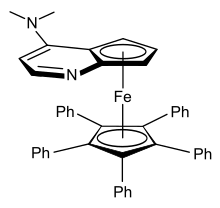
Дизамещенные ферроцены могут существовать в виде 1,2-, 1,3- или 1,1'-изомеров, ни один из которых не является взаимопревращаемым. Хиральными являются ферроцены, асимметрично дизамещенные в одном кольце, например [CpFe(EtC 5 H 3 Me)]. Эта плоская хиральность возникает несмотря на то, что ни один атом не является стереогенным центром . Было показано , что замещенный ферроцен, показанный справа (производное 4-(диметиламино)пиридина), эффективен при использовании для кинетического разделения рацемических вторичных спиртов . [56] Было разработано несколько подходов к асимметричной 1,1'-функционализации ферроцена. [57]
Ферроцен и его многочисленные производные не имеют широкомасштабного применения, но имеют множество нишевых применений, в которых используется необычная структура ( лигандные каркасы, фармацевтические кандидаты ), надежность ( антидетонационные составы , предшественники материалов) и окислительно-восстановительный потенциал (реагенты и окислительно-восстановительные стандарты). .
Хиральные ферроценилфосфины используются в качестве лигандов в реакциях, катализируемых переходными металлами. Некоторые из них нашли промышленное применение при синтезе фармацевтических препаратов и агрохимикатов. Например, дифосфин -1,1'-бис(дифенилфосфино)ферроцен (dppf) является ценным лигандом для реакций сочетания палладия , а лиганд Йозифос полезен для катализа гидрирования. [58] Они названы в честь техника, сделавшего первый, Хози Пулео. [59] [60]
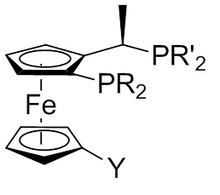
Ферроцен и его производные являются антидетонаторами , используемыми в топливе для бензиновых двигателей . Они безопаснее, чем использовавшийся ранее тетраэтилсвинец . [61] Растворы присадок к бензину, содержащие ферроцен, можно добавлять в неэтилированный бензин, чтобы его можно было использовать в старинных автомобилях, предназначенных для работы на этилированном бензине. [62] Железосодержащие отложения, образующиеся из ферроцена, могут образовывать проводящее покрытие на поверхностях свечей зажигания . Сополимеры ферроцена и полигликоля, полученные путем проведения реакции поликонденсации между производным ферроцена и замещенным дигидроксиспиртом, перспективны в качестве компонента ракетного топлива. Эти сополимеры придают ракетному топливу термостабильность, выступая в качестве связующего вещества и контролируя скорость горения топлива. [63]
Было обнаружено, что ферроцен эффективен в снижении дыма и триоксида серы, образующихся при сжигании угля. Добавление любым практическим способом, пропиткой угля или добавлением ферроцена в камеру сгорания, может значительно снизить количество этих нежелательных побочных продуктов даже при небольшом количестве циклопентадиенильного соединения металла. [64]
Производные ферроцена исследовались в качестве лекарств, [65] одно соединение ферроцерон было одобрено для использования в СССР в 1970-х годах, но сегодня оно больше не продается. [66] В последние годы только один препарат прошел клинические испытания: феррохин (7-хлор-N-(2-((диметиламино)метил)ферроценил)хинолин-4-амин), противомалярийное средство , [ 67] [68] [ 69] , который достиг фазы IIb исследований. [70] Были исследованы системы доставки лекарств на основе ферроценсодержащих полимеров. [71]

Противораковая активность производных ферроцена была впервые исследована в конце 1970-х годов, когда производные, несущие амино- или амидные группы, были протестированы против лимфоцитарной лейкемии . [72] Некоторые соли ферроцения проявляют противораковую активность, но ни одно соединение не прошло клинических исследований. [73] Производные ферроцена обладают сильной ингибирующей активностью в отношении линии клеток рака легких человека A549, линии клеток колоректального рака HCT116 и линии клеток рака молочной железы MCF-7. [74] Сообщалось об экспериментальном препарате, который представляет собой ферроцениловую версию тамоксифена . [75] Идея состоит в том, что тамоксифен будет связываться с сайтами связывания эстрогена , что приводит к цитотоксичности. [75] [76]
Ферроцифены используются для лечения рака французской биотехнологической компанией Feroscan, основанной проф. Жерар Жауэн.
Ферроцен и родственные ему производные используются в качестве мощных катализаторов горения в композитном топливе на основе перхлората аммония . [77]
Аналоги ферроцена можно получить с вариантами циклопентадиенила. Например, бис инденилирон и бисфторенилирон. [60]

Атомы углерода могут быть заменены гетероатомами, как показано Fe( η 5 -C 5 Me 5 )( η 5 -P 5 ) и Fe( η 5 -C 5 H 5 )( η 5 -C 4 H 4 N) (« азаферроцен»). Азаферроцен образуется в результате декарбонилирования Fe( η 5 -C 5 H 5 )(CO) 2 ( η 1 -пиррол) в циклогексане . [78] Это соединение при кипячении с обратным холодильником в бензоле превращается в ферроцен. [79]
Из-за простоты замещения было получено множество необычных по структуре производных ферроцена. Например, пента(ферроценил)циклопентадиенильный лиганд [80] представляет собой циклопентадиенильный анион, дериватизированный пятью ферроценовыми заместителями.


В гексаферроценилбензоле C 6 [( η 5 -C 5 H 4 )Fe( η 5 -C 5 H 5 )] 6 все шесть положений молекулы бензола имеют ферроценильные заместители ( R ). [81] Рентгеноструктурный анализ этого соединения подтверждает, что циклопентадиенильные лиганды не копланарны бензольному ядру, а имеют чередующиеся двугранные углы +30 ° и -80 °. Из-за стерической скученности ферроценилы слегка изогнуты на углы 177° и имеют удлиненные связи C-Fe. Четвертичные атомы углерода циклопентадиенила также имеют пирамидальную форму . Кроме того, бензольное ядро имеет конформацию кресла с двугранными углами 14 ° и демонстрирует изменение длины связи между 142,7 и 141,1 пм, что указывает на стерическое скучивание заместителей.
Сообщалось о синтезе гексаферроценилбензола с использованием сочетания Негиши гексаиодидбензола и диферроценилцинка с использованием трис (дибензилиденацетона) дипалладия (0) в качестве катализатора в тетрагидрофуране : [81]
Выход составляет всего 4%, что является еще одним свидетельством существенного стерического скопления вокруг аренового ядра.

Ферроцен, предшественник наночастиц железа, может быть использован в качестве катализатора для производства углеродных нанотрубок. [83] Винилферроцен может быть получен реакцией Виттига альдегида , фосфониевой соли и гидроксида натрия . [84] Винилферроцен можно превратить в полимер (поливинилферроцен, ПВФ), ферроценильную версию полистирола (фенильные группы заменены ферроценильными группами). Другим полиферроценом , который может быть образован, является поли(2-(метакрилоилокси)этилферроценкарбоксилат), PFcMA. Помимо использования основных цепей органических полимеров, эти боковые ферроценовые звенья были присоединены к неорганическим основным цепям, таким как полисилоксаны , полифосфазены и полифосфинобораны (–PH(R)–BH 2 –) n , и полученные материалы проявляют необычные физические и электронные свойства. относящийся к окислительно-восстановительной паре ферроцен/ферроциний. [82] И PVFc, и PFcMA были прикреплены к пластинам диоксида кремния , а смачиваемость измерялась, когда полимерные цепи не заряжены и когда ферроценовые фрагменты окисляются с образованием положительно заряженных групп. Угол контакта с водой на пластинах, покрытых PFcMA, после окисления был на 70° меньше, тогда как в случае PVFc уменьшение составило 30°, и переключение смачиваемости является обратимым. В случае PFcMA эффект удлинения цепей и, следовательно, введения большего количества ферроценовых групп заключается в значительно большем уменьшении угла смачивания при окислении. [82] [85]