
Гипотетические типы биохимии — это формы биохимии, признанные научно жизнеспособными, но не доказанные на данный момент. [2] Все виды живых организмов, известные в настоящее время на Земле, используют углеродные соединения для основных структурных и метаболических функций, воду в качестве растворителя , а также ДНК или РНК для определения и контроля своей формы. Если жизнь существует на других планетах или лунах , она может быть химически схожей, хотя также возможно, что существуют организмы с совершенно иной химией [3] — например, включающие другие классы углеродных соединений, соединения другого элемента или другой растворитель вместо воды.
Возможность существования форм жизни, основанных на «альтернативной» биохимии, является темой продолжающейся научной дискуссии, основанной на том, что известно о внеземных средах и о химическом поведении различных элементов и соединений. Она представляет интерес для синтетической биологии , а также является распространенной темой в научной фантастике .
Элемент кремний много обсуждался как гипотетическая альтернатива углероду. Кремний находится в той же группе, что и углерод в периодической таблице , и, как и углерод, он четырехвалентен . Гипотетические альтернативы воде включают аммиак , который, как и вода, является полярной молекулой и широко распространен в космосе; и неполярные углеводородные растворители, такие как метан и этан , которые, как известно, существуют в жидкой форме на поверхности Титана .

Теневая биосфера — это гипотетическая микробная биосфера Земли, которая использует радикально иные биохимические и молекулярные процессы, чем известная в настоящее время жизнь. [11] [12] Хотя жизнь на Земле относительно хорошо изучена, теневая биосфера может все еще оставаться незамеченной, поскольку исследование микробного мира нацелено в первую очередь на биохимию макроорганизмов.
Возможно, наименее необычной альтернативной биохимией была бы та, в которой биомолекулы отличаются хиральностью . В известной земной жизни аминокислоты почти всегда имеют L -форму, а сахара — D- форму. Молекулы, использующие D- аминокислоты или L- сахара, могут быть возможны; однако молекулы такой хиральности были бы несовместимы с организмами, использующими молекулы противоположной хиральности. Аминокислоты, хиральность которых противоположна норме, встречаются на Земле, и обычно считается, что эти вещества являются результатом распада организмов с нормальной хиральностью. Однако физик Пол Дэвис предполагает, что некоторые из них могут быть продуктами «антихиральной» жизни. [13]
Однако сомнительно, будет ли такая биохимия действительно чуждой. Хотя это, безусловно, будет альтернативная стереохимия , молекулы, которые в подавляющем большинстве случаев встречаются в одном энантиомере у большинства организмов, тем не менее, часто могут быть найдены в другом энантиомере у различных (часто базальных ) организмов, например, при сравнении представителей Archaea и других доменов , [ требуется ссылка ] делая открытым вопрос о том, является ли альтернативная стереохимия действительно новой.
На Земле все известные живые существа имеют структуру и систему на основе углерода. Ученые размышляли о плюсах и минусах использования элементов, отличных от углерода, для формирования молекулярных структур, необходимых для жизни, но никто не предложил теорию, использующую такие атомы для формирования всех необходимых структур. Однако, как утверждал Карл Саган , очень трудно быть уверенным, будет ли утверждение, применимое ко всей жизни на Земле, применимым ко всей жизни во всей Вселенной. [14] Саган использовал термин « углеродный шовинизм » для такого предположения. [15] Он рассматривал кремний и германий как возможные альтернативы углероду [15] (другие вероятные элементы включают, но не ограничиваются палладием и титаном ); но, с другой стороны, он отметил, что углерод действительно кажется более химически универсальным и более распространенным в космосе. [16] Норман Горовиц разработал эксперименты, чтобы определить, может ли существовать жизнь на Марсе , которые были проведены Viking Lander в 1976 году , первой американской миссией, которая успешно посадила зонд на поверхность Марса. Горовиц утверждал, что большая универсальность атома углерода делает его элементом, наиболее вероятным для предоставления решений, даже экзотических решений, проблем выживания на других планетах. [17] Он считал, что существует лишь отдаленная возможность того, что неуглеродные формы жизни могут существовать с генетическими информационными системами, способными к самовоспроизведению и способностью развиваться и адаптироваться.

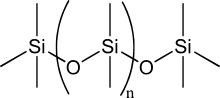

Атом кремния много обсуждался как основа для альтернативной биохимической системы, поскольку кремний имеет много химических сходств с углеродом и находится в той же группе периодической таблицы . Как и углерод, кремний может создавать молекулы, которые достаточно велики, чтобы нести биологическую информацию. [18]
Однако кремний имеет несколько недостатков в качестве альтернативы углероду. Углерод в десять раз более распространен в космосе, чем кремний, и его химия, по-видимому, более сложна. [19] К 1998 году астрономы идентифицировали 84 молекулы, содержащие углерод, в межзвездной среде , но только 8 из них содержали кремний, из которых половина также включала углерод. [20] Несмотря на то, что Земля и другие планеты земной группы исключительно богаты кремнием и бедны углеродом (кремния в земной коре примерно в 925 раз больше, чем углерода), земная жизнь основана на углероде. Она может избегать кремния, потому что соединения кремния менее разнообразны, нестабильны в присутствии воды или блокируют поток тепла. [19]
По сравнению с углеродом кремний имеет гораздо больший атомный радиус и образует гораздо более слабые ковалентные связи с атомами — за исключением кислорода и фтора , с которыми он образует очень прочные связи. [18] Практически никакие множественные связи с кремнием не являются стабильными, хотя кремний демонстрирует различное координационное число . [21] Силаны , кремниевые аналоги алканов , быстро реагируют с водой, а силаны с длинной цепью спонтанно разлагаются. [22] Следовательно, большая часть земного кремния «заперта» в кремнеземе , а не в широком спектре биогенных предшественников. [21]
Силиконы , которые чередуют атомы кремния и кислорода , намного более стабильны, чем силаны, и могут быть даже более стабильны, чем эквивалентные углеводороды в богатых серной кислотой внеземных средах. [22] С другой стороны, слабые связи в кремниевых соединениях могут помочь поддерживать быстрый темп жизни при криогенных температурах. Полисиланолы, кремниевые гомологи сахаров , являются одними из немногих соединений, растворимых в жидком азоте . [23] [ ненадежный источник? ] [21]
Все известные кремниевые макромолекулы являются искусственными полимерами и поэтому «монотонны по сравнению с комбинаторной вселенной органических макромолекул». [18] [21] Тем не менее, некоторые формы жизни на Земле используют биогенный кремний : силикатные скелеты диатомовых водорослей . А. Г. Кэрнс-Смит выдвинул гипотезу, что силикатные минералы в воде играют решающую роль в абиогенезе , поскольку вокруг их кристаллических структур образуются биогенные углеродные соединения. [24] [25] Хотя в природе это не наблюдается, связи углерода и кремния были добавлены в биохимию в ходе направленной эволюции (искусственного отбора): белок цитохрома c из Rhodothermus marinus был разработан для катализа новых связей углерода и кремния между гидросиланами и диазосоединениями . [26]
Мышьяк , который химически похож на фосфор , хотя и ядовит для большинства форм жизни на Земле, включен в биохимию некоторых организмов. [29] Некоторые морские водоросли включают мышьяк в сложные органические молекулы, такие как арсеносахара и арсенобетаины . Грибы и бактерии могут производить летучие метилированные соединения мышьяка. Восстановление арсената и окисление арсенита наблюдались у микробов ( Chrysiogenes arsenatis ). [30] Кроме того, некоторые прокариоты могут использовать арсенат в качестве конечного акцептора электронов во время анаэробного роста, а некоторые могут использовать арсенит в качестве донора электронов для получения энергии.
Было высказано предположение, что самые ранние формы жизни на Земле могли использовать биохимию мышьяка вместо фосфора в структуре своей ДНК. [31] Распространенным возражением против этого сценария является то, что эфиры арсената настолько менее устойчивы к гидролизу, чем соответствующие эфиры фосфорной кислоты , что мышьяк плохо подходит для этой функции. [32]
Авторы геомикробиологического исследования 2010 года, частично поддержанного NASA, предположили, что бактерия, названная GFAJ-1 , собранная в отложениях озера Моно в восточной Калифорнии , может использовать такую «ДНК мышьяка» при культивировании без фосфора. [33] [34] Они предположили, что бактерия может использовать высокие уровни поли-β-гидроксибутирата или другие средства для снижения эффективной концентрации воды и стабилизации ее эфиров арсената. [34] Это утверждение подверглось резкой критике почти сразу после публикации из-за предполагаемого отсутствия надлежащего контроля. [35] [36] Научный писатель Карл Циммер связался с несколькими учеными для оценки: «Я обратился к дюжине экспертов... Почти единогласно они считают, что ученые NASA не смогли обосновать свою позицию». [37] Другие авторы не смогли воспроизвести свои результаты и показали, что в исследовании были проблемы с загрязнением фосфатом, что предполагает, что низкие присутствующие количества могут поддерживать экстремофильные формы жизни. [38] В качестве альтернативы было высказано предположение, что клетки GFAJ-1 растут за счет переработки фосфата из деградировавших рибосом, а не за счет его замены арсенатом. [39]
Помимо соединений углерода, всем известным в настоящее время земным формам жизни также требуется вода в качестве растворителя. Это привело к дискуссиям о том, является ли вода единственной жидкостью, способной выполнять эту роль. Идея о том, что внеземная форма жизни может быть основана на растворителе, отличном от воды, была серьезно воспринята в недавней научной литературе биохимиком Стивеном Беннером [40] и астробиологическим комитетом под председательством Джона А. Барросса. [41] Растворители, обсуждаемые комитетом Барросса, включают аммиак [ 42] серную кислоту [ 43] формамид [44] углеводороды [ 44] и (при температурах намного ниже земных) жидкий азот или водород в форме сверхкритической жидкости [45 ]
Вода как растворитель ограничивает формы, которые может принимать биохимия. Например, Стивен Беннер предлагает полиэлектролитную теорию гена , которая утверждает, что для того, чтобы генетический биополимер , такой как ДНК, функционировал в воде, ему требуются повторяющиеся ионные заряды. [46] Если вода не требуется для жизни, эти ограничения на генетические биополимеры снимаются.
Карл Саган однажды назвал себя одновременно шовинистом углерода и шовинистом воды; [47] однако в другой раз он сказал, что он шовинист углерода, но «не такой уж шовинист воды». [48] Он размышлял об углеводородах, [48] : 11 плавиковой кислоте , [49] и аммиаке [48] [49] как о возможных альтернативах воде.
Некоторые свойства воды, важные для жизненных процессов, включают в себя:
Вода как соединение широко распространена в космосе, хотя большая ее часть находится в форме пара или льда. Подповерхностная жидкая вода считается вероятной или возможной на нескольких внешних лунах: Энцеладе (где были обнаружены гейзеры), Европе , Титане и Ганимеде . Земля и Титан — единственные миры, на поверхности которых в настоящее время известны стабильные тела жидкости.
Однако не все свойства воды обязательно благоприятны для жизни. [50] Например, водяной лед имеет высокое альбедо , [50] что означает, что он отражает значительное количество света и тепла от Солнца. Во время ледниковых периодов , когда отражающий лед накапливается на поверхности воды, эффекты глобального охлаждения усиливаются. [50]
Существуют некоторые свойства, которые делают определенные соединения и элементы гораздо более подходящими, чем другие, в качестве растворителей в успешной биосфере. Растворитель должен быть способен существовать в жидком равновесии в диапазоне температур, с которыми обычно сталкивается планетарный объект. Поскольку точки кипения изменяются в зависимости от давления, вопрос, как правило, заключается не в том, остается ли предполагаемый растворитель жидким, а в том, при каком давлении . Например, цианистый водород имеет узкий температурный диапазон жидкой фазы при 1 атмосфере, но в атмосфере с давлением Венеры , с давлением 92 бара (91 атм), он действительно может существовать в жидкой форме в широком диапазоне температур.
Молекула аммиака (NH 3 ), как и молекула воды, широко распространена во Вселенной, представляя собой соединение водорода (самого простого и распространенного элемента) с другим очень распространенным элементом, азотом. [51] Возможная роль жидкого аммиака как альтернативного растворителя для жизни — это идея, которая восходит по крайней мере к 1954 году, когда Дж. Б. С. Холдейн поднял эту тему на симпозиуме о происхождении жизни. [52]
В растворе аммиака возможны многочисленные химические реакции, а жидкий аммиак имеет химическое сходство с водой. [51] [53] Аммиак может растворять большинство органических молекул, по крайней мере, так же хорошо, как вода, и, кроме того, он способен растворять многие элементарные металлы. Холдейн указал на то, что различные распространенные органические соединения, связанные с водой, имеют аналоги, связанные с аммиаком; например, связанная с аммиаком аминогруппа (−NH 2 ) аналогична связанной с водой гидроксильной группе (−OH). [53]
Аммиак, как и вода, может либо принимать, либо отдавать ион H + . Когда аммиак принимает H + , он образует катион аммония (NH 4 + ), аналогичный гидроксонию (H 3 O + ). Когда он отдает ион H + , он образует амидный анион (NH 2 − ), аналогичный гидроксид- аниону (OH − ). [42] Однако по сравнению с водой аммиак более склонен принимать ион H + и менее склонен отдавать его; он является более сильным нуклеофилом . [42] Аммиак, добавленный к воде, действует как основание Аррениуса : он увеличивает концентрацию аниона гидроксида. И наоборот, используя определение кислотности и основности в системе растворителей, вода, добавленная к жидкому аммиаку, действует как кислота, поскольку она увеличивает концентрацию катиона аммония. [53] Карбонильная группа (C=O), которая широко используется в земной биохимии, не будет стабильной в растворе аммиака, но вместо нее можно использовать аналогичную иминную группу (C=NH). [42]
Однако аммиак имеет некоторые проблемы как основа для жизни. Водородные связи между молекулами аммиака слабее, чем в воде, из-за чего теплота испарения аммиака вдвое меньше, чем у воды, его поверхностное натяжение составляет треть, и снижается его способность концентрировать неполярные молекулы посредством гидрофобного эффекта. Джеральд Файнберг и Роберт Шапиро задавались вопросом, может ли аммиак удерживать пребиотические молекулы вместе достаточно хорошо, чтобы позволить возникнуть самовоспроизводящейся системе. [54] Аммиак также воспламеняется в кислороде и не может существовать устойчиво в среде, подходящей для аэробного метаболизма . [55]

Биосфера на основе аммиака , вероятно, будет существовать при температурах или давлении воздуха, которые крайне необычны по отношению к жизни на Земле. Жизнь на Земле обычно существует между точкой плавления и точкой кипения воды, при давлении, обозначенном как нормальное давление , между 0 и 100 °C (273 и 373 K ). При нормальном давлении точки плавления и кипения аммиака составляют -78 °C (195 K) и -33 °C (240 K) соответственно. Поскольку химические реакции обычно протекают медленнее при более низких температурах, жизнь на основе аммиака, существующая в этом наборе условий, может метаболизироваться медленнее и развиваться медленнее, чем жизнь на Земле. [55] С другой стороны, более низкие температуры также могут позволить живым системам использовать химические виды, которые были бы слишком нестабильны при земных температурах, чтобы быть полезными. [51]
Набор условий, при которых аммиак находится в жидком состоянии при температурах, подобных земным, подразумевает, что он находится под гораздо более высоким давлением. Например, при 60 атм аммиак плавится при температуре −77 °C (196 K) и кипит при температуре 98 °C (371 K). [42]
Аммиак и смеси аммиака с водой остаются жидкими при температурах, значительно ниже точки замерзания чистой воды, поэтому такая биохимия может хорошо подходить для планет и лун, вращающихся за пределами водной зоны обитаемости . Такие условия могут существовать, например, под поверхностью крупнейшего спутника Сатурна Титана . [ 56]
Метан (CH 4 ) — это простой углеводород: то есть соединение двух наиболее распространенных элементов в космосе: водорода и углерода. Его космическое изобилие сопоставимо с аммиаком. [51] Углеводороды могут действовать как растворитель в широком диапазоне температур, но не обладают полярностью . Айзек Азимов, биохимик и писатель-фантаст, предположил в 1981 году, что полилипиды могут образовывать замену белкам в неполярном растворителе, таком как метан. [51] Озера, состоящие из смеси углеводородов, включая метан и этан , были обнаружены на поверхности Титана космическим аппаратом Кассини .
Ведутся споры об эффективности метана и других углеводородов в качестве растворителя для жизни по сравнению с водой или аммиаком. [57] [58] [59] Вода является более сильным растворителем, чем углеводороды, что позволяет легче переносить вещества в клетке. [60] Однако вода также более химически активна и может расщеплять большие органические молекулы посредством гидролиза. [57] Форма жизни, растворителем которой является углеводород, не столкнется с угрозой уничтожения ее биомолекул таким образом. [57] Кроме того, тенденция молекулы воды образовывать сильные водородные связи может мешать внутренним водородным связям в сложных органических молекулах. [50] Жизнь с углеводородным растворителем могла бы больше использовать водородные связи внутри своих биомолекул. [57] Более того, прочность водородных связей внутри биомолекул соответствовала бы низкотемпературной биохимии. [57]
Астробиолог Крис Маккей утверждал, исходя из термодинамических соображений, что если жизнь действительно существует на поверхности Титана, используя углеводороды в качестве растворителя, она, вероятно, также использует более сложные углеводороды в качестве источника энергии, реагируя с ними с водородом, восстанавливая этан и ацетилен до метана. [61] Возможные доказательства этой формы жизни на Титане были выявлены в 2010 году Дарреллом Штробелем из Университета Джонса Хопкинса ; большее обилие молекулярного водорода в верхних слоях атмосферы Титана по сравнению с нижними слоями, что свидетельствует о нисходящей диффузии со скоростью примерно 1025 молекул в секунду и исчезновении водорода вблизи поверхности Титана. Как отметил Штробел, его выводы соответствуют эффектам, которые предсказал Крис Маккей, если бы присутствовали метаногенные формы жизни. [60] [61] [62] В том же году другое исследование показало низкие уровни ацетилена на поверхности Титана, которые были интерпретированы Крисом Маккеем как соответствующие гипотезе организмов, восстанавливающих ацетилен до метана. [60] Переформулируя биологическую гипотезу, Маккей предупредил, что другие объяснения результатов по водороду и ацетилену следует считать более вероятными: возможности еще не идентифицированных физических или химических процессов (например, неживой поверхностный катализатор, позволяющий ацетилену реагировать с водородом) или недостатки в текущих моделях потока материалов. [63] Он отметил, что даже небиологический катализатор, эффективный при 95 К, сам по себе был бы поразительным открытием. [63]
Гипотетическая клеточная мембрана , называемая азотосомой, способная функционировать в жидком метане в условиях Титана, была смоделирована на компьютере в статье, опубликованной в феврале 2015 года. Состоящая из акрилонитрила , небольшой молекулы, содержащей углерод, водород и азот, она, как ожидается, будет иметь стабильность и гибкость в жидком метане, сравнимые со стабильностью и гибкостью фосфолипидного бислоя (тип клеточной мембраны, которым обладает вся жизнь на Земле) в жидкой воде. [64] [65] Анализ данных, полученных с помощью Атакамской большой миллиметровой / субмиллиметровой матрицы (ALMA), завершенный в 2017 году, подтвердил наличие значительных количеств акрилонитрила в атмосфере Титана. [66] [67] Более поздние исследования поставили под сомнение способность акрилонитрила к самоорганизации в азотозомы. [68]
Фтористый водород (HF), как и вода, является полярной молекулой, и из-за своей полярности он может растворять многие ионные соединения. При атмосферном давлении его температура плавления составляет 189,15 К (−84,00 °C), а температура кипения — 292,69 К (19,54 °C); разница между ними составляет чуть больше 100 К. HF также образует водородные связи с соседними молекулами, как это делают вода и аммиак. Он рассматривался как возможный растворитель для жизни такими учеными, как Питер Снит [69] и Карл Саган. [49]
HF опасен для систем молекул, из которых состоит земная жизнь, но некоторые другие органические соединения, такие как парафиновые воски , стабильны с ним. [49] Подобно воде и аммиаку, жидкий фтористый водород поддерживает кислотно-щелочную химию. Используя определение кислотности и основности в системе растворителей, азотная кислота действует как основание, когда ее добавляют к жидкому HF. [70]
Однако фтористый водород в космосе встречается редко, в отличие от воды, аммиака и метана. [71]
Сероводород является ближайшим химическим аналогом воды , [72] но он менее полярен и является более слабым неорганическим растворителем. [73] Сероводород довольно обилен на спутнике Юпитера Ио и может находиться в жидкой форме на небольшом расстоянии от поверхности; астробиолог Дирк Шульце-Макух предположил, что он может быть возможным растворителем для жизни там. [74] На планете с океанами сероводорода источником сероводорода могут быть вулканы, и в этом случае он может быть смешан с небольшим количеством фтороводорода , который может помочь растворить минералы. Жизнь на сероводороде может использовать смесь оксида углерода и диоксида углерода в качестве источника углерода. Они могут производить и жить на оксиде серы , который аналогичен кислороду (O 2 ). Сероводород, как и цианистый водород и аммиак, страдает от небольшого температурного диапазона, в котором он находится в жидком состоянии, хотя этот диапазон, как и у цианистого водорода и аммиака, увеличивается с ростом давления.
Диоксид кремния , также известный как кремнезем и кварц, очень распространен во Вселенной и имеет большой температурный диапазон, в котором он находится в жидком состоянии. Однако его температура плавления составляет от 1600 до 1725 °C (от 2912 до 3137 °F), поэтому было бы невозможно создавать органические соединения при этой температуре, потому что все они разложились бы. Силикаты похожи на диоксид кремния, и некоторые из них имеют более низкие температуры плавления, чем кремнезем. Файнберг и Шапиро предположили, что расплавленная силикатная порода может служить жидкой средой для организмов с химией, основанной на кремнии, кислороде и других элементах, таких как алюминий . [75]

Иногда предлагаются и другие растворители:
Серная кислота в жидкой форме является сильно полярной. Она остается жидкой при более высоких температурах, чем вода, ее жидкий диапазон составляет от 10 °C до 337 °C при давлении 1 атм, хотя выше 300 °C она медленно разлагается. Известно, что серная кислота в изобилии присутствует в облаках Венеры в форме аэрозольных капель. В биохимии, которая использовала серную кислоту в качестве растворителя, алкеновая группа (C=C) с двумя атомами углерода, соединенными двойной связью, могла бы функционировать аналогично карбонильной группе (C=O) в биохимии на основе воды. [43]
Было высказано предположение, что жизнь на Марсе может существовать и использовать смесь воды и перекиси водорода в качестве растворителя. [79] Смесь воды и перекиси водорода с концентрацией 61,2% (по массе) имеет температуру замерзания −56,5 °C и имеет тенденцию к переохлаждению, а не кристаллизации. Она также гигроскопична , что является преимуществом в среде с дефицитом воды. [80] [81]
Сверхкритический диоксид углерода был предложен в качестве кандидата для альтернативной биохимии из-за его способности избирательно растворять органические соединения и способствовать функционированию ферментов, а также потому, что планеты типа «суперземля» или «супервенера» с плотной атмосферой высокого давления могут быть обычным явлением. [76]
Физики отметили, что, хотя фотосинтез на Земле обычно включает зеленые растения, множество растений других цветов также могут поддерживать фотосинтез, необходимый для большинства форм жизни на Земле, и что другие цвета могут быть предпочтительны в местах, которые получают иную смесь звездного излучения, чем Земля. [82] [83] Эти исследования показывают, что синие растения маловероятны; однако желтые или красные растения могут быть относительно распространены. [83]
Многие растения и животные Земли претерпевают серьезные биохимические изменения в течение своего жизненного цикла в ответ на изменяющиеся условия окружающей среды, например, имея споровое или гибернационное состояние, которое может поддерживаться в течение многих лет или даже тысячелетий между более активными стадиями жизни. [84] Таким образом, биохимически было бы возможно поддерживать жизнь в средах, которые лишь периодически соответствуют жизни, какой мы ее знаем.
Например, лягушки в холодном климате могут выживать в течение длительных периодов времени, сохраняя большую часть воды в организме в замороженном состоянии [84] , тогда как пустынные лягушки в Австралии могут становиться неактивными и обезвоживаться в засушливые периоды, теряя до 75% своей жидкости, но возвращаться к жизни, быстро восполняя запасы жидкости во влажные периоды. [85] Любой тип лягушек будет казаться биохимически неактивным (т. е. не живым) во время периодов покоя любому, у кого нет чувствительных средств обнаружения низких уровней метаболизма.

Генетический код мог эволюционировать во время перехода от мира РНК к миру белков . [86] Гипотеза аланинового мира постулирует, что эволюция генетического кода (так называемая фаза GC [87] ) началась всего с четырех основных аминокислот : аланина , глицина , пролина и орнитина (теперь аргинина ). [88] Эволюция генетического кода завершилась 20 протеиногенными аминокислотами . С химической точки зрения большинство из них являются производными аланина, особенно подходящими для построения α-спиралей и β-слоев — основных вторичных структурных элементов современных белков. Прямым доказательством этого является экспериментальная процедура в молекулярной биологии, известная как аланиновое сканирование .
Гипотетический «Пролиновый мир» создал бы возможную альтернативную жизнь с генетическим кодом, основанным на химическом каркасе пролина в качестве белкового остова . Аналогично, «Глициновый мир» и «Орнитиновый мир» также возможны, но природа не выбрала ни один из них. [89] Эволюция жизни с Пролином, Глицином или Орнитином в качестве базовой структуры для протеиноподобных полимеров ( фолдамеров ) привела бы к параллельным биологическим мирам. Они имели бы морфологически радикально отличающиеся планы тела и генетику от живых организмов известной биосферы . [90]
[ сомнительный – обсудить ]
В 2007 году Вадим Н. Цытович и его коллеги предположили, что поведение, подобное поведению живых существ, может демонстрироваться частицами пыли, взвешенными в плазме , в условиях, которые могут существовать в космосе. [91] [92] Компьютерные модели показали, что, когда пыль становится заряженной, частицы могут самоорганизовываться в микроскопические спиральные структуры, и авторы предлагают «грубый набросок возможной модели... воспроизведения спиральной структуры зерен».
В 2020 году Луис А. Анчордок и Юджин М. Чудновский из Городского университета Нью-Йорка выдвинули гипотезу, что космическая жизнь на основе ожерелья, состоящая из магнитных монополей, соединенных космическими струнами, может развиваться внутри звезд. [5] Это будет достигнуто путем растяжения космических струн из-за интенсивной гравитации звезды, что позволит ей принимать более сложные формы и потенциально формировать структуры, похожие на структуры РНК и ДНК, обнаруженные в жизни на основе углерода. Таким образом, теоретически возможно, что такие существа в конечном итоге могут стать разумными и построить цивилизацию, используя энергию, вырабатываемую ядерным синтезом звезды. Поскольку такое использование израсходует часть энергии, вырабатываемой звездой, светимость также упадет. По этой причине считается, что такая жизнь может существовать внутри звезд, которые, как наблюдалось, остывают быстрее или тускнее, чем предсказывают современные космологические модели.
Фрэнк Дрейк предположил в 1973 году, что разумная жизнь может обитать на нейтронных звездах . [93] Физические модели 1973 года подразумевали, что существа Дрейка будут микроскопическими. [ необходима цитата ]
Ученые, которые рассматривали возможные альтернативы биохимии углерода и воды, включают:
{{cite web}}: CS1 maint: неподходящий URL ( ссылка ){{cite journal}}: CS1 maint: несколько имен: список авторов ( ссылка )