В химии фосфат – это анион , соль , функциональная группа или сложный эфир, полученный из фосфорной кислоты . Чаще всего под ним подразумевают ортофосфат , производное ортофосфорной кислоты, она же фосфорная кислота H 3 PO 4 .
Фосфат или ортофосфат - ион [PO
4]3-
получается из фосфорной кислоты путем удаления трех протонов H+
. Удаление одного протона дает ион дигидрофосфата [ H
2ПО
4]−
а удаление двух ионов дает ион гидрофосфата [HPO
4]2-
. Эти названия также используются для солей этих анионов, таких как дигидрофосфат аммония и тринатрийфосфат .
В органической химии фосфат или ортофосфат — органофосфат , сложный эфир ортофосфорной кислоты формы PO .
4RR’R″ , где один или несколько атомов водорода заменены органическими группами. Примером является триметилфосфат ( CH
3)
3ПО
4. Этот термин также относится к трехвалентной функциональной группе OP(O-)
3в таких эфирах. Фосфаты могут содержать серу вместо одного или нескольких атомов кислорода ( тиофосфаты и органотиофосфаты ).
Ортофосфаты занимают особенно важное место среди различных фосфатов из-за их ключевой роли в биохимии , биогеохимии и экологии , а также их экономического значения для сельского хозяйства и промышленности. [2] Добавление и удаление фосфатных групп ( фосфорилирование и дефосфорилирование ) являются ключевыми этапами клеточного метаболизма .
Ортофосфаты могут конденсироваться с образованием пирофосфатов .
Фосфат-ион имеет молярную массу 94,97 г/моль и состоит из центрального атома фосфора , окруженного четырьмя атомами кислорода в тетраэдрическом расположении. Это сопряженное основание иона гидрофосфата H (PO
4)2-
, который, в свою очередь, является сопряженным основанием иона дигидрофосфата H
2(ПО
4)−
, которое, в свою очередь, является сопряженным основанием ортофосфорной кислоты , H
3ПО
4.
Многие фосфаты растворимы в воде при стандартной температуре и давлении . Фосфаты натрия, калия, рубидия , цезия и аммония растворимы в воде. Большинство других фосфатов мало растворимы или нерастворимы в воде. Как правило, водородные и дигидрофосфаты несколько более растворимы, чем соответствующие фосфаты.

В водном растворе ортофосфорная кислота и три ее производных аниона сосуществуют в соответствии с равновесиями диссоциации и рекомбинации, указанными ниже [3]
Значения указаны при температуре 25 °C и ионной силе 0.
Значения p K a представляют собой значения pH , при которых концентрация каждого вида равна концентрации его сопряженных оснований . При pH 1 или ниже фосфорная кислота практически не диссоциирует. При pH 4,7 (середина между первыми двумя значениями p K a ) ион дигидрофосфата [H
2ПО
4]−
, практически единственный присутствующий вид. При pH 9,8 (середина между вторым и третьим значениями p K a ) ион моногидрофосфата [HPO
4]2-
, единственный присутствующий вид. При pH 13 или выше кислота полностью диссоциирует в виде фосфат-иона (PO
4)3-
.
Это означает, что соли моно- и дифосфат-ионов можно избирательно кристаллизовать из водного раствора, установив значение pH на уровне 4,7 или 9,8.
Фактически, Х
3ПО
4, Ч
2(ПО
4)−
и H(PO
4)2-
ведут себя как отдельные слабые кислоты , поскольку последовательные p K a различаются более чем в 4 раза.
Фосфат может образовывать множество полимерных ионов , таких как пирофосфат (P
2О
7)4-
и трифосфат , (P
3О
10)5-
. Различные ионы метафосфата (которые обычно представляют собой длинные линейные полимеры) имеют эмпирическую формулу (PO
3)−
и встречаются во многих соединениях.
В биологических системах фосфор может находиться в виде свободных фосфат-анионов в растворе ( неорганический фосфат ) или в виде связанных с органическими молекулами в виде различных органофосфатов .
Неорганический фосфат обычно обозначается Pi и при физиологическом (гомеостатическом) pH в основном состоит из смеси [HPO
4]2-
и [Ч
2ПО
4]−
ионы. При нейтральном pH, как и в цитозоле (pH = 7,0), концентрации ортофосфорной кислоты и трех ее анионов имеют соотношения
Таким образом, только [H
2ПО
4]−
и [HPO
4]2-
ионы присутствуют в цитозоле в значительных количествах (62% [H
2ПО
4]−
, 38% [ГПО
4]2-
). Во внеклеточной жидкости (рН = 7,4) эта пропорция обратная (61% [HPO
4]2-
, 39% [Н
2ПО
4]−
).
Неорганический фосфат также может присутствовать в виде пирофосфат- анионов [P
2О
7]4-
, которые при гидролизе дают ортофосфат :
Органические фосфаты обычно встречаются в форме сложных эфиров в виде нуклеотидов (например , АМФ , АДФ и АТФ ), а также в ДНК и РНК . Свободные ортофосфат-анионы могут высвобождаться при гидролизе фосфоангидридных связей АТФ или АДФ. Эти реакции фосфорилирования и дефосфорилирования являются непосредственным хранилищем и источником энергии для многих метаболических процессов. АТФ и АДФ часто называют высокоэнергетическими фосфатами , как и фосфагены в мышечной ткани. Подобные реакции существуют и для других нуклеозиддифосфатов и трифосфатов .
Важным явлением фосфатов в биологических системах является структурный материал костей и зубов. Эти структуры состоят из кристаллического фосфата кальция в форме гидроксиапатита . Твердая плотная эмаль зубов млекопитающих может содержать фторапатит , гидроксифосфат кальция, в котором некоторые гидроксильные группы заменены ионами фтора .
Фосфаты – это лекарственные соли фосфора. Некоторые фосфаты, которые помогают вылечить многие инфекции мочевыводящих путей , используются для повышения кислотности мочи. Чтобы избежать развития кальциевых камней в мочевыводящих путях, применяют некоторые фосфаты. [5] Для пациентов, которые не могут получать достаточное количество фосфора в своем ежедневном рационе, фосфаты используются в качестве пищевых добавок, обычно из-за определенных расстройств или заболеваний. [5] Инъекционные фосфаты могут обрабатываться только квалифицированными медицинскими работниками. [5]
Растения поглощают фосфор несколькими путями: арбускулярным микоризным путем и путем прямого поглощения.
Гиперфосфатемия , или высокий уровень фосфатов в крови, связана с повышенной смертностью среди населения в целом. Наиболее распространенной причиной гиперфосфатемии у людей, собак и кошек является почечная недостаточность. В случаях гиперфосфатемии ограничение потребления продуктов, богатых фосфатами, таких как некоторые мясные и молочные продукты, а также продуктов с высоким соотношением фосфатов к белкам, таких как безалкогольные напитки, фаст-фуд, обработанные пищевые продукты, приправы и другие продукты, содержащие фосфат. -рекомендуются солевые добавки. [6]
Фосфаты вызывают кальцификацию сосудов , а высокая концентрация фосфатов в крови оказалась предиктором сердечно-сосудистых событий . [7]


Фосфаты представляют собой природную форму элемента фосфора , который содержится во многих фосфатных минералах . В минералогии и геологии фосфатом называют горную породу или руду, содержащую ионы фосфата. Неорганические фосфаты добывают для получения фосфора для использования в сельском хозяйстве и промышленности. [2]
Крупнейшим мировым производителем и экспортером фосфатов является Марокко . В Северной Америке крупнейшие месторождения находятся в районе долины костей в центральной Флориде , в районе Сода-Спрингс на юго-востоке Айдахо и на побережье Северной Каролины . Меньшие месторождения расположены в Монтане , Теннесси , Джорджии и Южной Каролине . Небольшое островное государство Науру и его соседний остров Банаба , где раньше были огромные залежи фосфатов самого высокого качества, были добыты в чрезмерном количестве. Фосфат также можно найти в Египте, Израиле, Палестине, Западной Сахаре, на острове Навасса , Тунисе, Того и Иордании, странах с крупной промышленностью по добыче фосфатов.
Фосфоритовые рудники в основном находятся в:
По оценкам, в 2007 году при нынешних темпах потребления запасы фосфора исчерпаются через 345 лет. [8] Однако некоторые ученые считали, что « пик фосфора » наступит через 30 лет, а Дана Корделл из Института устойчивого будущего заявила, что «при нынешних темпах запасы будут истощены в ближайшие 50–100 лет». [9] Под резервами понимается сумма, предположительно возмещаемая по текущим рыночным ценам. В 2012 году Геологическая служба США оценила мировые запасы в 71 миллиард тонн, тогда как в 2011 году в мире было добыто 0,19 миллиарда тонн. [10] Фосфор составляет 0,1% по массе средней породы [11] (хотя, для сравнения, его типичная концентрация в растительности составляет от 0,03% до 0,2%), [12] и, следовательно, в земной коре размером 3×10 19 тонн содержится квадриллион тонн фосфора , [13] хотя и в преимущественно более низкой концентрации, чем в месторождениях, считающихся запасами, которые инвентаризируются и их дешевле добывать. извлекать. Если предположить, что фосфатные минералы в фосфоритной породе представляют собой в основном гидроксиапатит и фторапатит, то фосфатные минералы содержат примерно 18,5% фосфора по массе. Если фосфоритная руда содержит около 20% этих минералов, то средняя фосфоритная руда содержит примерно 3,7% фосфора по весу.
Некоторые месторождения фосфоритных пород, такие как Малберри во Флориде [14] , отличаются наличием значительных количеств радиоактивных изотопов урана. Это вызывает беспокойство, поскольку радиоактивность может попасть в поверхностные воды [15] в результате применения полученных фосфатных удобрений .
В 2021 году Норвегия обнаружила залежи фосфатов, почти равные запасам на всей остальной Земле вместе взятых. [16]
В декабре 2012 года компания Cominco Resources объявила об обновленных ресурсах своего проекта Хинда в Конго-Браззавиле, соответствующих требованиям JORC , в размере 531 миллиона тонн, что делает его крупнейшим измеренным и выявленным месторождением фосфатов в мире. [17]
В июле 2022 года Китай объявил о квотах на экспорт фосфатов. [18]
Крупнейшими импортерами фосфатов в миллионах тонн являются Бразилия (3,2), Индия (2,9) и США (1,6). [19]
На три основные страны-производителя фосфатов (Китай, Марокко и США) приходится около 70% мирового производства.
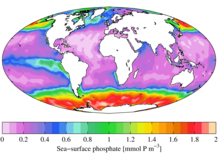

С экологической точки зрения, из-за своей важной роли в биологических системах фосфат является весьма востребованным ресурсом. После использования он часто становится лимитирующим питательным веществом в окружающей среде , и его доступность может определять скорость роста организмов. В целом это справедливо для пресноводной среды, тогда как азот чаще является лимитирующим питательным веществом в морской (морской) среде. Добавление высоких уровней фосфатов в окружающую среду и микросреду, где они обычно встречаются редко, может иметь серьезные экологические последствия. Например, может произойти цветение популяций одних организмов за счет других, а также коллапс популяций, лишенных таких ресурсов, как кислород (см. Эвтрофикация ). В контексте загрязнения фосфаты являются одним из компонентов общего количества растворенных твердых веществ , что является основным показателем качества воды, но не весь фосфор находится в молекулярной форме, которую водоросли могут расщеплять и потреблять. [21]
Вокруг бактерий в аллювиальном верхнем слое почвы можно обнаружить осадки гидроксиапатита кальция и кальцита . [22] Поскольку глинистые минералы способствуют биоминерализации, присутствие бактерий и глинистых минералов приводило к образованию осадков гидроксиапатита кальция и кальцита. [22]
Отложения фосфатов могут содержать значительные количества встречающихся в природе тяжелых металлов. При горнодобывающей деятельности по переработке фосфоритной руды могут образовываться отвалы с повышенным содержанием кадмия , свинца , никеля , меди , хрома и урана . Без тщательного обращения эти отходы могут привести к выщелачиванию тяжелых металлов в грунтовые воды или близлежащие устья рек. Поглощение этих веществ растениями и морскими обитателями может привести к концентрации токсичных тяжелых металлов в пищевых продуктах. [23]
По словам Майкла Бретта, профессора инженерии Университета Вашингтона, [B]ioдоступный фосфор – фосфор, который может быть использован растениями и бактериями – составляет лишь часть от общего количества…