
Фотохимия – это раздел химии , изучающий химические эффекты света. Обычно этот термин используется для описания химической реакции, вызванной поглощением ультрафиолетового ( длина волны от 100 до 400 нм ), видимого света (400–750 нм) или инфракрасного излучения (750–2500 нм). [1]
В природе фотохимия имеет огромное значение, так как лежит в основе фотосинтеза, зрения и образования витамина D под действием солнечного света. [2] Он также ответственен за появление мутаций ДНК, приводящих к раку кожи. [3]
Фотохимические реакции протекают иначе, чем реакции, обусловленные температурой. Фотохимические пути обеспечивают доступ к высокоэнергетическим промежуточным продуктам, которые не могут быть получены термически, тем самым преодолевая большие активационные барьеры за короткий период времени и позволяя проводить реакции, которые иначе были бы недоступны для тепловых процессов. Фотохимия также может быть разрушительной, о чем свидетельствует фоторазложение пластмасс .
Фотовозбуждение — это первый этап фотохимического процесса, при котором реагент переходит в состояние с более высокой энергией, возбужденное состояние . Первый закон фотохимии, известный как закон Гроттуса-Дрейпера (для химиков Теодора Гроттуса и Джона В. Дрейпера ), гласит, что свет должен поглощаться химическим веществом, чтобы произошла фотохимическая реакция . Согласно второму закону фотохимии, известному как закон Штарка-Эйнштейна (для физиков Иоганна Старка и Альберта Эйнштейна ), на каждый фотон света, поглощенный химической системой, для фотохимической реакции активируется не более одной молекулы, как определено по квантовому выходу . [4] [5]
Когда молекула или атом в основном состоянии (S 0 ) поглощает свет, один электрон возбуждается на более высокий орбитальный уровень. Этот электрон сохраняет свой спин в соответствии с правилом выбора спина; другие переходы нарушили бы закон сохранения углового момента . Возбуждение в более высокое синглетное состояние может происходить от ВЗМО до НСМО или до более высокой орбитали, так что возможны синглетные состояния возбуждения S 1 , S 2 , S 3 ... при разных энергиях.
Правило Каши предполагает, что более высокие синглетные состояния будут быстро релаксировать за счет безызлучательного распада или внутреннего преобразования (IC) в S 1 . Таким образом, S 1 обычно, но не всегда, является единственным соответствующим синглетным возбужденным состоянием. Это возбужденное состояние S1 может далее релаксировать до S0 посредством IC, а также посредством разрешенного радиационного перехода от S1 к S0 , который испускает фотон; этот процесс называется флюоресценцией .
Альтернативно, возбужденное состояние S 1 может претерпевать инверсию спина и генерировать триплетное возбужденное состояние T 1 , имеющее два неспаренных электрона с одинаковым спином. Такое нарушение правила спинового отбора возможно за счет интеркомбинационного пересечения (ИСП) колебательных и электронных уровней S 1 и T 1 . Согласно правилу максимальной множественности Хунда , это состояние T1 будет несколько более стабильным, чем S1 .
Это триплетное состояние может релаксировать в основное состояние S 0 посредством безызлучательного IC или путем излучения, называемого фосфоресценцией . Этот процесс подразумевает изменение электронного спина, что запрещено правилами отбора спинов, что делает фосфоресценцию (от T 1 до S 0 ) намного медленнее, чем флуоресценцию (от S 1 до S 0 ). Таким образом, триплетные состояния обычно имеют более продолжительное время жизни, чем синглетные состояния. Эти переходы обычно суммируются в диаграмме энергии состояний или диаграмме Яблонского , парадигме молекулярной фотохимии.
Эти возбужденные частицы, либо S 1 , либо T 1 , имеют полупустую низкоэнергетическую орбиталь и, следовательно, являются более окисляющими, чем основное состояние. Но в то же время они имеют электрон на высокоэнергетической орбитали и, следовательно, являются более восстановительными. В общем, возбужденные частицы склонны участвовать в процессах переноса электронов. [6]

Фотохимические реакции требуют источника света, излучающего волны, соответствующие электронному переходу в реагенте. В ранних экспериментах (и в повседневной жизни) источником света был солнечный свет, хотя он и полихроматичен. [7] Ртутные лампы чаще встречаются в лабораториях. Ртутные лампы низкого давления в основном излучают свет на длине волны 254 нм. Для полихроматических источников диапазоны длин волн можно выбирать с помощью фильтров. Альтернативно, лазерные лучи обычно являются монохроматическими (хотя с помощью нелинейной оптики можно получить две или более длины волн), а светодиоды имеют относительно узкую полосу частот, которую можно эффективно использовать, как и лампы Rayonet, для получения приблизительно монохроматических лучей.

Испускаемый свет, конечно, должен достигать целевой функциональной группы , не блокируясь реактором, средой или другими присутствующими функциональными группами. Во многих случаях кварц используется для реакторов, а также для изоляции лампы. Пирекс поглощает волны короче 275 нм. Растворитель является важным экспериментальным параметром. Растворители являются потенциальными реагентами, поэтому следует избегать использования хлорированных растворителей, поскольку связь C–Cl может привести к хлорированию субстрата. Сильно поглощающие растворители препятствуют попаданию фотонов на подложку. Углеводородные растворители поглощают только короткие волны и поэтому предпочтительны для фотохимических экспериментов, требующих фотонов высокой энергии. Растворители, содержащие ненасыщенность, поглощают более длинные волны и могут эффективно фильтровать короткие волны. Например, циклогексан и ацетон «обрезают» (сильно поглощают) при длинах волн короче 215 и 330 нм соответственно.
Обычно длина волны, используемая для индукции фотохимического процесса, выбирается на основе спектра поглощения реакционноспособных частиц, чаще всего максимума поглощения. Однако за последние годы было продемонстрировано, что в большинстве реакций образования связей спектр поглощения не позволяет выбрать оптимальную длину волны для достижения максимального выхода реакции на основе поглощательной способности. Это фундаментальное несоответствие между поглощательной способностью и реакционной способностью было объяснено с помощью так называемых графиков фотохимического действия. [8] [9]
Фотохимия в непрерывном потоке предлагает множество преимуществ по сравнению с фотохимией в периодическом режиме. Фотохимические реакции определяются количеством фотонов, которые способны активировать молекулы, вызывая желаемую реакцию. Большое соотношение площади поверхности к объему микрореактора максимизирует освещенность и в то же время обеспечивает эффективное охлаждение, что уменьшает побочные тепловые продукты. [10]
В случае фотохимических реакций свет обеспечивает энергию активации . Проще говоря, свет — это один из механизмов обеспечения энергии активации, необходимой для многих реакций. Если используется лазерный свет, можно избирательно возбудить молекулу, чтобы создать желаемое электронное и колебательное состояние. [11] Точно так же выбросы в конкретном штате могут выборочно контролироваться, обеспечивая измерение численности населения этого штата. Если химическая система находится под низким давлением, это позволяет ученым наблюдать распределение продуктов химической реакции по энергии до того, как различия в энергии будут размыты и усреднены в результате повторных столкновений.
Поглощение фотона света молекулой-реагентом может также позволить протекать реакции не только за счет доведения молекулы до необходимой энергии активации, но также за счет изменения симметрии электронной конфигурации молекулы, открывая путь реакции, недоступный иначе, как описывается правилами отбора Вудворда-Гоффмана . Реакция циклоприсоединения [2+2] является одним из примеров перициклической реакции , которую можно анализировать с использованием этих правил или связанной с ней теории пограничных молекулярных орбиталей .
Некоторые фотохимические реакции протекают на несколько порядков быстрее термических; Часто наблюдаются реакции со скоростью 10–9 секунд и связанные с ними процессы со скоростью 10–15 секунд .
Фотон может быть поглощен непосредственно реагентом или фотосенсибилизатором , который поглощает фотон и передает энергию реагенту. Противоположный процесс называется тушением , когда фотовозбужденное состояние дезактивируется химическим реагентом.
Большинство фотохимических превращений происходят посредством серии простых стадий, известных как первичные фотохимические процессы. Одним из распространенных примеров этих процессов является перенос протона в возбужденном состоянии.
Примерами фотохимических органических реакций являются электроциклические реакции , радикальные реакции , фотоизомеризация и реакции Норриша . [20] [21]
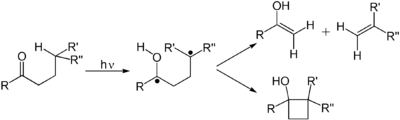
Алкены претерпевают множество важных реакций, которые протекают через индуцированный фотонами переход от π к π*. В первом электронном возбужденном состоянии алкена отсутствует π-связь, поэтому вращение вокруг связи C–C происходит быстро, и молекула участвует в реакциях, не наблюдаемых термически. Эти реакции включают цис-транс-изомеризацию, циклоприсоединение к другому (основному состоянию) алкену с образованием производных циклобутана . Цис-транс-изомеризация (поли)алкена участвует в сетчатке глаза , компоненте зрительного аппарата . Димеризация алкенов связана с фотоповреждением ДНК , когда димеры тимина наблюдаются при освещении ДНК УФ-излучением. Такие димеры мешают транскрипции . Благотворное воздействие солнечного света связано с фотохимически индуцированной реакцией ретроциклизации (дециклизации) эргостерина с образованием витамина D. В реакции ДеМайо алкен реагирует с 1,3-дикетоном, реагирующим через его енол с образованием 1,5-дикетона. -дикетон. Еще одной распространенной фотохимической реакцией является перегруппировка ди-π-метана Говарда Циммермана .
В промышленном применении ежегодно путем газофазной фотохимической реакции толуола с хлором получают около 100 000 тонн бензилхлорида . [22] Свет поглощается молекулой хлора, о низкой энергии этого перехода свидетельствует желтоватый цвет газа. Фотон индуцирует гомолиз связи Cl-Cl, и образующийся радикал хлора превращает толуол в бензильный радикал:
Меркаптаны можно получить фотохимическим присоединением сероводорода (H 2 S) к альфа- олефинам .
Фотореактивными являются также координационные комплексы и металлоорганические соединения . Эти реакции могут повлечь за собой цис-транс-изомеризацию. Чаще всего фотореакции приводят к диссоциации лигандов, поскольку фотон переводит электрон на металле на орбиталь, которая является разрыхляющей по отношению к лигандам. Таким образом, карбонилы металлов , устойчивые к термическому замещению, подвергаются декарбонилированию при облучении УФ-светом. УФ-облучение раствора гексакарбонила молибдена в ТГФ дает комплекс ТГФ, который полезен в синтетическом отношении:
В аналогичной реакции фотолиз пентакарбонила железа дает нонакарбонил дижелеза (см. Рисунок):
Некоторые фотореактивные координационные комплексы могут подвергаться окислительно-восстановительным процессам посредством переноса одного электрона. Этот перенос электрона может происходить внутри внутренней или внешней координационной сферы металла. [23]
Вот несколько различных типов фотохимических реакций:
Хотя отбеливание практикуется уже давно, первая фотохимическая реакция была описана Троммсдорфом в 1834 году. [24] Он заметил, что кристаллы соединения α-сантонин под воздействием солнечного света желтели и лопались. В исследовании 2007 года реакция была описана как последовательность трех стадий, происходящих внутри монокристалла. [25]
Первый этап представляет собой реакцию перегруппировки с образованием циклопентадиенонового интермедиата 2 , второй — димеризацию по реакции Дильса–Альдера ( 3 ) и третий — внутримолекулярное [2+2] циклоприсоединение ( 4 ). Эффект взрыва объясняется большим изменением объема кристалла при димеризации.
Организацию этих конференций осуществляет Международный фонд фотохимии. [26]