
Биокатализ – это использование живых (биологических) систем или их частей для ускорения ( катализирования ) химических реакций. В биокаталитических процессах природные катализаторы, такие как ферменты , выполняют химические превращения органических соединений . Для этой задачи используются как ферменты, которые были более или менее изолированы , так и ферменты, все еще находящиеся внутри живых клеток . [1] [2] [3] Современная биотехнология, направленная на эволюцию , сделала возможным производство модифицированных или неприродных ферментов. Это позволило разработать ферменты, которые могут катализировать новые преобразования малых молекул, которые могут быть трудными или невозможными с использованием классической синтетической органической химии. Использование природных или модифицированных ферментов для осуществления органического синтеза называется химиоферментативным синтезом ; Реакции, осуществляемые ферментом, относят к химиоферментативным реакциям .
Биокатализ лежит в основе некоторых из старейших химических превращений, известных человечеству, поскольку пивоварение предшествует письменной истории. Самым древним записям о пивоварении около 6000 лет, и они относятся к шумерам .
Использование ферментов и целых клеток на протяжении веков было важно для многих отраслей промышленности. Наиболее очевидным применением является производство продуктов питания и напитков, где производство вина, пива, сыра и т. д. зависит от воздействия микроорганизмов .
Более ста лет назад биокатализ использовался для химических превращений неприродных искусственных органических соединений , а за последние 30 лет наблюдался значительный рост применения биокатализа для производства тонких химикатов , особенно для фармацевтической промышленности . [4]
Поскольку биокатализ имеет дело с ферментами и микроорганизмами, его исторически классифицируют отдельно от «гомогенного катализа» и «гетерогенного катализа». Однако с механистической точки зрения биокатализ — это просто частный случай гетерогенного катализа. [5]
- Ферменты экологически безопасны и полностью разлагаются в окружающей среде.
-Большинство ферментов обычно функционируют в мягких или биологических условиях, что сводит к минимуму проблемы нежелательных побочных реакций, таких как разложение, изомеризация , рацемизация и перегруппировка , которые часто мешают традиционной методологии.
-Ферменты, выбранные для химиоферментативного синтеза, можно иммобилизовать на твердой подложке. Эти иммобилизованные ферменты демонстрируют улучшенную стабильность и возможность повторного использования.
-Благодаря развитию белковой инженерии , в частности сайт-направленного мутагенеза и направленной эволюции, ферменты могут быть модифицированы, чтобы обеспечить необычную реактивность. Модификации также могут обеспечить более широкий диапазон субстратов, повысить скорость реакции или оборачиваемость катализатора.
- Ферменты проявляют чрезвычайную избирательность по отношению к своим субстратам. Обычно ферменты проявляют три основных типа селективности:
Эти причины, и особенно последняя, являются основными причинами интереса химиков-синтетиков к биокатализу. Этот интерес, в свою очередь, обусловлен главным образом необходимостью синтеза энантиочистых соединений в качестве хиральных строительных блоков для фармацевтических препаратов и агрохимикатов .
Использование биокатализа для получения энантиочистых соединений можно разделить на два разных метода:
При кинетическом разрешении рацемической смеси присутствие хирального объекта (фермента) превращает один из стереоизомеров реагента в его продукт с большей скоростью реакции , чем для другого стереоизомера реагента. Стереохимическая смесь теперь превратилась в смесь двух разных соединений, что позволяет разделить их обычными методами.
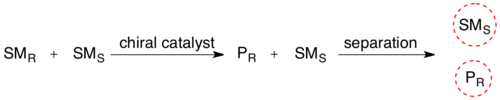
Биокаталитическое кинетическое разделение широко используется при очистке рацемических смесей синтетических аминокислот. Многие популярные пути синтеза аминокислот, такие как синтез Стрекера , приводят к получению смеси энантиомеров R и S. Эту смесь можно очистить путем (I) ацилирования амина с использованием ангидрида и затем (II) селективного деацилирования только L-энантиомера с использованием ацилазы из почек свиньи. [6] Эти ферменты обычно чрезвычайно селективны в отношении одного энантиомера, что приводит к очень большим различиям в скорости, что позволяет осуществлять селективное деацилирование. [7] Наконец, эти два продукта теперь можно разделить с помощью классических методов, таких как хроматография .

Максимальный выход при таком кинетическом разрешении составляет 50%, поскольку выход более 50% означает, что часть неправильного изомера также прореагировала, что дает меньший энантиомерный избыток . Поэтому такие реакции должны быть прекращены до достижения равновесия. Если возможно осуществить такое разделение в условиях, когда два субстрата-энантиомера непрерывно рацемизуются, теоретически весь субстрат может быть превращен в энантиочистый продукт. Это называется динамическим разрешением .
При биокаталитическом асимметричном синтезе нехиральная единица становится хиральной таким образом, что различные возможные стереоизомеры образуются в разных количествах. Хиральность привносится в субстрат под действием фермента, который является хиральным. Дрожжи являются биокатализатором энантиоселективного восстановления кетонов .
Окисление Байера -Виллигера является еще одним примером биокаталитической реакции. В одном исследовании было обнаружено , что специально созданный мутант Candida antarctica является эффективным катализатором присоединения по Михаэлю акролеина к ацетилацетону при 20 ° C в отсутствие дополнительного растворителя. [8]
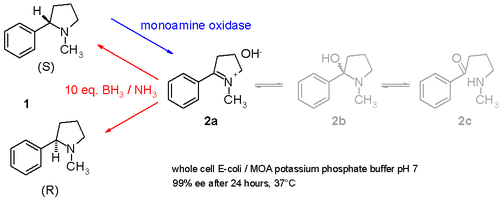
Другое исследование демонстрирует, как рацемический никотин (смесь S- и R-энантиомеров 1 на схеме 3 ) может быть дерацемизирован с помощью однореакторной процедуры с использованием моноаминоксидазы, выделенной из Aspergillus niger , которая способна окислять только аминный S-энантиомер до имина. 2 и с участием восстанавливающей пары аммиак - боран , которая может восстановить имин 2 обратно до амина 1 . [9] Таким образом, S-энантиомер будет постоянно потребляться ферментом, в то время как R-энантиомер накапливается. Возможно даже стереоинвертировать чистый S в чистый R.
Недавно фотоокислительно-восстановительный катализ был применен к биокатализу, что позволило осуществить уникальные, ранее недоступные преобразования. Фотоокислительно-восстановительная химия использует свет для генерации промежуточных продуктов свободных радикалов . [10] Эти радикальные промежуточные соединения являются ахиральными, поэтому рацемические смеси продуктов получаются без внешнего хирального окружения. Ферменты могут обеспечить эту хиральную среду внутри активного центра и стабилизировать определенную конформацию, способствуя образованию одного энантиочистого продукта. [11] Реакции биокатализа с использованием фоторедокса делятся на две категории:
Некоторые распространенные кофакторы переноса атома водорода ( HAT ) ( НАДФН и флавин ) могут действовать как реагенты переноса одиночного электрона ( SET ). [11] [12] [13] Хотя эти виды способны к HAT без облучения, их окислительно-восстановительный потенциал увеличивается почти на 2,0 В при облучении видимым светом. [14] В сочетании с соответствующими ферментами (обычно енредуктазами ). Это явление использовалось химиками для разработки методологий энантиоселективного восстановления. Например, лактамы среднего размера могут быть синтезированы в хиральном окружении ен-редуктазы посредством восстановительной, предпочтительной по Болдуину , радикальной циклизации , завершаемой энантиоселективной HAT из НАДФН. [15]
Вторая категория фотоокислительно-восстановительных реакций позволяет проводить биокаталитические реакции с использованием внешнего фотокатализатора (ПК). Можно использовать многие типы ПК с большим диапазоном окислительно-восстановительных потенциалов, что обеспечивает большую возможность настройки реактивной реакции по сравнению с использованием кофактора. Бенгальский розовый и внешний ПК использовались в тандеме с оксидоредуктазой для энантиоселективного деацилирования альфа-ацилкетонов среднего размера . [16]
Использование внешнего ПК имеет некоторые недостатки. Например, внешние ПК обычно усложняют разработку реакции, поскольку ПК могут реагировать как со связанным, так и с несвязанным субстратом. Если реакция происходит между несвязанным субстратом и ПК, энантиоселективность теряется и могут возникнуть другие побочные реакции.
Биоферменты также являются биокатализаторами. Их готовят путем ферментации органических отходов, неочищенного пальмового сахара и воды в соотношении 3:1:10 в течение трех месяцев. Он увеличивает популяцию почвенных микробов, ускоряет компостирование и разложение и поэтому входит в состав катализаторов. Он лечит почву. Это одно из лучших органических жидких удобрений. Его разбавляют водой.
{{cite book}}: CS1 maint: несколько имен: список авторов ( ссылка ) CS1 maint: числовые имена: список авторов ( ссылка )