Эукариотическая трансляция — это биологический процесс, посредством которого информационная РНК транслируется в белки у эукариот . Он состоит из четырех фаз: инициации, удлинения, завершения и повторения.

Инициация трансляции — это процесс, посредством которого рибосома и связанные с ней факторы связываются с мРНК и собираются в стартовом кодоне. Этот процесс определяется либо как кэп-зависимый, при котором рибосома первоначально связывается с 5'-кэпом, а затем перемещается к стоп-кодону, либо как кэп-независимый, когда рибосома изначально не связывается с 5'-кэпом.
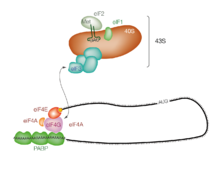
Инициация трансляции обычно включает взаимодействие определенных ключевых белков, факторов инициации , со специальной меткой, связанной с 5'-концом молекулы мРНК, 5'-кэпом , а также с 5'-UTR . Эти белки связывают малую (40S) субъединицу рибосомы и удерживают мРНК на месте. [1]
eIF3 связан с субъединицей рибосомы 40S и играет роль в предотвращении преждевременного связывания большой субъединицы рибосомы (60S). eIF3 также взаимодействует с комплексом eIF4F , который состоит из трех других факторов инициации: eIF4A , eIF4E и eIF4G . eIF4G представляет собой каркасный белок, который напрямую связывается как с eIF3, так и с двумя другими компонентами. eIF4E представляет собой белок, связывающий кэп. Связывание кэпа с помощью eIF4E часто считают стадией, лимитирующей скорость кэп-зависимой инициации, а концентрация eIF4E является регуляторным звеном контроля трансляции. Некоторые вирусы расщепляют часть eIF4G, которая связывает eIF4E, тем самым предотвращая кэп-зависимую трансляцию с целью перехватить механизм хозяина в пользу вирусных (кэп-независимых) сообщений. eIF4A представляет собой АТФ-зависимую РНК-геликазу, которая помогает рибосоме, расщепляя определенные вторичные структуры, образующиеся вдоль транскрипта мРНК. [2] Поли (А)-связывающий белок (PABP) также связывается с комплексом eIF4F через eIF4G и связывает поли-А-хвост большинства молекул мРНК эукариот. Этот белок участвует в циркуляризации мРНК во время трансляции. [3]
Этот преинициативный комплекс 43S (43S PIC), сопровождаемый белковыми факторами, движется вдоль цепи мРНК к ее 3'-концу в процессе, известном как «сканирование», чтобы достичь стартового кодона (обычно AUG). У эукариот и архей аминокислота , кодируемая стартовым кодоном, — метионин . Met-заряженная инициаторная тРНК (Met-tRNA i Met ) доставляется в P-сайт малой рибосомальной субъединицы с помощью эукариотического фактора инициации 2 (eIF2) . Он гидролизует GTP и сигнализирует о диссоциации нескольких факторов из малой субъединицы рибосомы, что в конечном итоге приводит к ассоциации большой субъединицы (или субъединицы 60S ). Затем полная рибосома ( 80S ) начинает элонгацию трансляции.
На регуляцию синтеза белка частично влияет фосфорилирование eIF2 (через α-субъединицу), который входит в состав тройного комплекса eIF2-GTP-Met-tRNA i Met (eIF2-TC). Когда большое количество eIF2 фосфорилируется, синтез белка ингибируется. Это происходит при аминокислотном голодании или после вирусной инфекции. Однако небольшая часть этого фактора инициации фосфорилируется естественным путем. Другим регулятором является 4EBP , который связывается с фактором инициации eIF4E и ингибирует его взаимодействие с eIF4G , тем самым предотвращая кэп-зависимую инициацию. Чтобы противостоять эффектам 4EBP, факторы роста фосфорилируют 4EBP, снижая его сродство к eIF4E и обеспечивая синтез белка. [ нужна цитата ]
Хотя синтез белка глобально регулируется путем модуляции экспрессии ключевых факторов инициации, а также количества рибосом, отдельные мРНК могут иметь разные скорости трансляции из-за присутствия элементов регуляторной последовательности. Было показано, что это важно в различных условиях, включая дрожжевой мейоз и реакцию этилена у растений. Кроме того, недавние исследования на дрожжах и людях предполагают, что эволюционное расхождение в цис-регуляторных последовательностях может влиять на регуляцию трансляции. [4] Кроме того, РНК- хеликазы , такие как DHX29 и Ded1/DDX3, могут участвовать в процессе инициации трансляции, особенно для мРНК со структурированными 5'UTR. [5]
Наиболее изученный пример кэп-независимой инициации трансляции у эукариот использует внутренний сайт входа в рибосому (IRES). В отличие от кэп-зависимой трансляции, кэп-независимая трансляция не требует 5'-кэпа для инициации сканирования от 5'-конца мРНК до стартового кодона. Рибосома может локализоваться в стартовом сайте посредством прямого связывания, факторов инициации и/или ITAF (транс-действующих факторов IRES), минуя необходимость сканирования всей 5'-UTR . Этот метод трансляции важен в условиях, требующих трансляции специфических мРНК во время клеточного стресса, когда общая трансляция снижается. Примеры включают факторы, реагирующие на апоптоз и реакции, вызванные стрессом. [6]
Элонгация зависит от факторов элонгации эукариот . В конце этапа инициации мРНК располагается так, что следующий кодон может быть транслирован во время стадии элонгации синтеза белка. Инициаторная тРНК занимает участок Р в рибосоме , а участок А готов принять аминоацил-тРНК. Во время удлинения цепи каждая дополнительная аминокислота добавляется к образующейся полипептидной цепи в трехэтапном микроцикле. Этапы этого микроцикла: (1) размещение правильной аминоацил-тРНК в участке A рибосомы, которая переносится в этот участок с помощью eEF1, (2) образование пептидной связи и (3) сдвиг мРНК на один кодон. относительно рибосомы с помощью eEF2. В отличие от бактерий, у которых инициация трансляции происходит сразу после синтеза 5'-конца мРНК, у эукариот такая тесная связь между транскрипцией и трансляцией невозможна, поскольку транскрипция и трансляция осуществляются в отдельных компартментах клетки ( ядре и цитоплазма ). Предшественники мРНК эукариот должны быть процессированы в ядре (например, кэпирование, полиаденилирование , сплайсинг) в рибосомах, прежде чем они будут экспортированы в цитоплазму для трансляции. На трансляцию также может влиять рибосомальная пауза , которая может вызвать эндонуклеолитическую атаку тРНК, процесс, называемый no-go распадом мРНК. Рибосомальная пауза также способствует котрансляционному сворачиванию образующегося полипептида на рибосоме и задерживает трансляцию белка, пока он кодирует тРНК. Это может вызвать сдвиг рамки рибосомы. [7]
Прекращение элонгации зависит от эукариотических факторов высвобождения . Этот процесс аналогичен процессу бактериальной терминации , но в отличие от бактериальной терминации существует универсальный фактор высвобождения eRF1, который распознает все три стоп-кодона. По окончании рибосома разбирается и высвобождается законченный полипептид. eRF3 представляет собой рибосомозависимую ГТФазу, которая помогает eRF1 высвобождать готовый полипептид. Геном человека кодирует несколько генов, стоп-кодон мРНК которых на удивление ненадежен: в этих генах терминация трансляции неэффективна из-за наличия особых оснований РНК вблизи стоп-кодона. Утечка терминации в этих генах приводит к трансляционному считыванию до 10% стоп-кодонов этих генов. Некоторые из этих генов кодируют функциональные белковые домены в своем расширении, что позволяет создавать новые изоформы белков . Этот процесс получил название «функционально-трансляционное прочтение». [8]
Трансляция является одним из ключевых потребителей энергии в клетках, поэтому она строго регулируется. Развились многочисленные механизмы, которые контролируют и регулируют трансляцию как у эукариот , так и у прокариот . Регуляция трансляции может влиять на глобальную скорость синтеза белка, которая тесно связана с метаболическим и пролиферативным состоянием клетки. Чтобы глубже разобраться в этом сложном процессе, ученые обычно используют метод, известный как профилирование рибосом. [9] Этот метод позволяет исследователям сделать снимок транслатома, показывая, какие части мРНК транслируются рибосомами в белки в данный момент времени. Профилирование рибосом дает ценную информацию о динамике трансляции, раскрывая сложное взаимодействие между последовательностью генов, структурой мРНК и регуляцией трансляции. В развитие этой концепции более поздней разработкой является профилирование рибосом отдельных клеток — метод, который позволяет нам изучать процесс трансляции с разрешением отдельных клеток. [10] Профилирование рибосом отдельных клеток потенциально может пролить свет на гетерогенную природу клеток, что приведет к более детальному пониманию того, как регуляция трансляции может влиять на поведение клеток, метаболическое состояние и реакцию на различные стимулы или условия.
В некоторых клетках некоторые аминокислоты могут истощаться, что влияет на эффективность трансляции. Например, активированные Т-клетки секретируют интерферон-γ , который вызывает внутриклеточную нехватку триптофана за счет активации фермента индоламин-2,3-диоксигеназы 1 (IDO1). Удивительно, но, несмотря на истощение триптофана , синтез белка в рамке считывания продолжается через кодоны триптофана . Это достигается за счет включения фенилаланина вместо триптофана. Полученные пептиды называются «заместителями» W>F. Такие заменители W>F широко распространены при некоторых типах рака и связаны с повышенной экспрессией IDO1. Функционально заместители W>F могут ухудшать активность белка . [11]
{{cite journal}}: CS1 maint: несколько имен: список авторов ( ссылка )