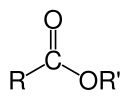
В химии сложный эфир — это соединение , полученное из кислоты (органической или неорганической), в котором атом водорода (H) по крайней мере одной кислой гидроксильной группы ( -OH ) этой кислоты заменен органильной группой ( -R ). Аналоги, полученные из кислорода , замененного другими халькогенами, также относятся к категории сложных эфиров. [1] По мнению некоторых авторов, органильные производные кислого водорода других кислот также являются сложными эфирами (например, амидами ), но не по данным ИЮПАК . [1]
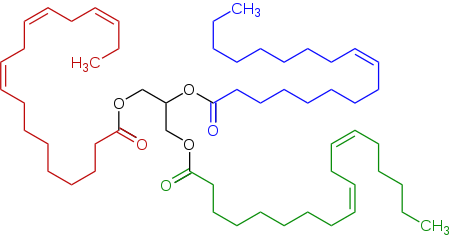
Глицериды представляют собой эфиры жирных кислот и глицерина ; они важны в биологии, поскольку являются одним из основных классов липидов и составляют основную часть животных жиров и растительных масел . Лактоны представляют собой сложные эфиры циклических карбоновых кислот; встречающиеся в природе лактоны представляют собой в основном 5- и 6-членные кольцевые лактоны. Лактоны придают аромат фруктам, маслу, сыру, овощам , например сельдерею , и другим продуктам.
Сложные эфиры могут образовываться из оксокислот (например, эфиры уксусной кислоты , угольной кислоты , серной кислоты , фосфорной кислоты , азотной кислоты , ксантиновой кислоты ), а также из кислот, не содержащих кислорода (например, эфиров тиоциановой кислоты и тритиоугольной кислоты ). Примером образования сложного эфира является реакция замещения между карбоновой кислотой ( R-C(=O)-OH ) и спиртом ( R'-OH ), образующая сложный эфир ( R-C(=O)-O-R). ' ), где R означает любую группу (обычно водородную или органильную), а R ' означает органильную группу.
Органиловые эфиры карбоновых кислот обычно имеют приятный запах; те, что имеют низкую молекулярную массу, обычно используются в качестве ароматизаторов и содержатся в эфирных маслах и феромонах . Они действуют как высококачественные растворители для широкого спектра пластмасс , пластификаторов , смол и лаков [2] и являются одним из крупнейших классов синтетических смазочных материалов на коммерческом рынке. [3] Полиэфиры являются важными пластиками, мономеры которых связаны сложноэфирными фрагментами . Эфиры фосфорной кислоты составляют основу молекул ДНК . Эфиры азотной кислоты , например нитроглицерин , известны своими взрывчатыми свойствами.
Существуют соединения, в которых кислый водород кислот, упомянутых в этой статье, заменен не органилом, а какой-либо другой группой. По мнению некоторых авторов, эти соединения также являются сложными эфирами, особенно когда первый атом углерода органильной группы, заменяющий кислый водород, заменен другим атомом из 14-й группы элементов ( Si , Ge , Sn , Pb ); например, по их мнению, триметилстаннилацетат (или ацетат триметилолова) CH 3 COOSn(CH 3 ) 3 представляет собой триметилстанниловый эфир уксусной кислоты , а дилаурат дибутилолова (CH 3 (CH 2 ) 10 COO) 2 Sn((CH 2 ) 3 CH 3 ) 2 представляет собой дибутилстанниленовый эфир лауриновой кислоты , а катализатор Филлипса CrO 2 (OSi(OCH 3 ) 3 ) 2 представляет собой триметоксисилиловый эфир хромовой кислоты ( H 2 CrO 4 ). [4] [5]
Слово « эфир» было придумано в 1848 году немецким химиком Леопольдом Гмелином [6], вероятно , как сокращение немецкого Essigäther , « уксусный эфир ».
Названия сложных эфиров, образующихся из спирта и кислоты, происходят от исходного спирта и исходной кислоты, причем последняя может быть органической или неорганической. Сложные эфиры, полученные из простейших карбоновых кислот, обычно называют в соответствии с более традиционными, так называемыми « тривиальными названиями », например, формиат, ацетат, пропионат и бутират, в отличие от номенклатуры ИЮПАК метаноат, этаноат, пропаноат и бутаноат. С другой стороны, сложные эфиры, полученные из более сложных карбоновых кислот, чаще называют систематическим названием IUPAC, основанным на названии кислоты, за которым следует суффикс -оат . Например, сложный эфир гексилоктаноата, также известный под тривиальным названием гексилкаприлат , имеет формулу CH 3 (CH 2 ) 6 CO 2 (CH 2 ) 5 CH 3 .

Химические формулы органических эфиров, образующихся из карбоновых кислот и спиртов, обычно имеют вид RCO 2 R' или RCOOR', где R и R' — органильные части карбоновой кислоты и спирта соответственно, а R может представлять собой водород в Сложные эфиры муравьиной кислоты . Например, бутилацетат (систематически бутилэтаноат), полученный из бутанола и уксусной кислоты (систематически этаноловая кислота), будет обозначаться CH 3 CO 2 (CH 2 ) 3 CH 3 . Альтернативные представления являются общими, включая BuOAc и CH 3 COO(CH 2 ) 3 CH 3 .
Циклические сложные эфиры называются лактонами независимо от того, являются ли они производными органической или неорганической кислоты. Одним из примеров органического лактона является γ-валеролактон .
Необычным классом сложных эфиров являются ортоэфиры . Одними из них являются эфиры ортокарбоновых кислот. Эти сложные эфиры имеют формулу RC(OR') 3 , где R означает любую группу (органическую или неорганическую), а R ' означает органильную группу. Например, триэтилортомуравьиная кислота ( HC(OCH 2 CH 3 ) 3 ) получается, согласно его названию (но не его синтезу), в результате этерификации ортомуравьиной кислоты ( HC(OH) 3 ) этанолом .
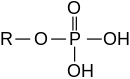
Эфиры также могут быть получены из неорганических кислот.
Неорганические кислоты, существующие в виде таутомеров, образуют два или более типов сложных эфиров.
Некоторые неорганические кислоты, которые нестабильны или неуловимы, образуют стабильные сложные эфиры.
В принципе, часть алкоксидов металлов и металлоидов , которых известны многие сотни, можно отнести к сложным эфирам соответствующих кислот (например, триэтоксид алюминия ( Al(OCH 2 CH 3 ) 3 ) можно отнести к сложному эфиру алюминиевой кислоты. который представляет собой гидроксид алюминия , тетраэтилортосиликат ( Si(OCH 2 CH 3 ) 4 ) можно классифицировать как сложный эфир ортокремниевой кислоты , а этоксид титана ( Ti(OCH 2 CH 3 ) 4 ) можно классифицировать как сложный эфир ортотитановой кислоты . .
Сложные эфиры, полученные из карбоновых кислот и спиртов , содержат карбонильную группу C=O, которая представляет собой двухвалентную группу при атоме C , что приводит к образованию углов C–C–O и O–C–O 120°. В отличие от амидов , эфиры карбоновых кислот представляют собой структурно гибкие функциональные группы, поскольку вращение вокруг связей C–O–C имеет низкий барьер. Их гибкость и малая полярность проявляются в их физических свойствах; они имеют тенденцию быть менее жесткими (более низкая температура плавления) и более летучими (более низкая температура кипения), чем соответствующие амиды . [7] P K a альфа-водородов в эфирах карбоновых кислот составляет около 25 (альфа-водород представляет собой водород, связанный с углеродом, соседним с карбонильной группой (C=O) сложных эфиров карбоновых кислот). [8]
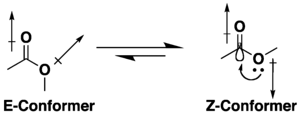
Многие эфиры карбоновых кислот обладают потенциалом конформационной изомерии , но они имеют тенденцию принимать S - цис (или Z ) конформацию, а не альтернативу S - транс (или E ) из-за комбинации эффектов гиперконъюгации и дипольной минимизации . На предпочтение Z- конформации влияет природа заместителей и растворителя, если он присутствует. [9] [10] Лактоны с маленькими кольцами ограничены конформацией s -транс (т.е. E ) из-за их циклической структуры.
Сложные эфиры, полученные из карбоновых кислот и спиртов, более полярны, чем простые эфиры , но менее полярны, чем спирты. Они участвуют в водородных связях как акцепторы водородных связей, но не могут выступать в качестве доноров водородных связей, в отличие от своих исходных спиртов. Эта способность участвовать в образовании водородных связей придает некоторую растворимость в воде. Из-за отсутствия способности донора водородных связей сложные эфиры не самоассоциируются. Следовательно, сложные эфиры более летучи, чем карбоновые кислоты с аналогичной молекулярной массой. [7]
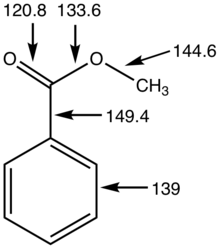
Сложные эфиры обычно идентифицируются с помощью газовой хроматографии, учитывая их летучесть. ИК-спектры сложных эфиров имеют интенсивную резкую полосу в диапазоне 1730–1750 см -1 , принадлежащую ν C=O . Этот пик меняется в зависимости от функциональных групп, присоединенных к карбонилу. Например, бензольное кольцо или двойная связь в сочетании с карбонилом снизят волновое число примерно на 30 см -1 .
Эфиры широко распространены в природе и широко используются в промышленности. В природе жиры , как правило, представляют собой триэфиры, полученные из глицерина и жирных кислот . [12] Эфиры отвечают за аромат многих фруктов, включая яблоки , дурианы , груши , бананы , ананасы и клубнику . [13] Ежегодно в промышленности производится несколько миллиардов килограммов полиэфиров , важными продуктами являются полиэтилентерефталат , сложные эфиры акрилата и ацетат целлюлозы . [14]
Этерификация — это общее название химической реакции , в которой два реагента (обычно спирт и кислота) образуют в качестве продукта реакции сложный эфир . Эфиры широко распространены в органической химии и биологических материалах и часто имеют приятный характерный фруктовый запах. Это приводит к их широкому использованию в парфюмерной и вкусовой промышленности. Эфирные связи также встречаются во многих полимерах .
Классическим синтезом является этерификация Фишера , которая включает обработку карбоновой кислоты спиртом в присутствии дегидратирующего агента:
Константа равновесия для таких реакций составляет около 5 для типичных эфиров, например этилацетата. [15] Реакция протекает медленно в отсутствие катализатора. Серная кислота является типичным катализатором этой реакции. Также используются многие другие кислоты, такие как полимерные сульфоновые кислоты . Поскольку этерификация весьма обратима, выход сложного эфира можно улучшить, используя принцип Ле Шателье :
Известны реагенты, вызывающие дегидратацию смесей спиртов и карбоновых кислот. Одним из примеров является этерификация Стеглиха , которая представляет собой метод образования сложных эфиров в мягких условиях. Этот метод популярен в синтезе пептидов , где субстраты чувствительны к суровым условиям, таким как высокая температура. DCC ( дициклогексилкарбодиимид ) используется для активации карбоновой кислоты для дальнейшей реакции. В качестве катализатора переноса ацила используется 4-диметиламинопиридин (ДМАП) . [16]
Другим методом дегидратации смесей спиртов и карбоновых кислот является реакция Мицунобу :
Карбоновые кислоты можно этерифицировать диазометаном :
Используя этот диазометан, смеси карбоновых кислот можно преобразовать в их метиловые эфиры с близкими к количественным выходам, например, для анализа с помощью газовой хроматографии . Этот метод полезен в специализированных операциях по органическому синтезу, но считается слишком опасным и дорогим для крупномасштабного применения.
Карбоновые кислоты этерифицируются обработкой эпоксидами с образованием β-гидроксиэфиров:
Эта реакция используется при производстве винилэфирной смолы из акриловой кислоты .
Спирты реагируют с ацилхлоридами и ангидридами кислот с образованием сложных эфиров:
Реакции необратимы, что упрощает исследование . Поскольку ацилхлориды и ангидриды кислот также реагируют с водой, предпочтительными являются безводные условия. Аналогичные ацилирования аминов с образованием амидов менее чувствительны, поскольку амины являются более сильными нуклеофилами и реагируют быстрее, чем вода. Этот метод используется только для процедур лабораторного масштаба, поскольку он дорог.
Тетрафторборат триметилоксония можно использовать для этерификации карбоновых кислот в условиях, когда кислотно-катализируемые реакции невозможны: [17]
Хотя соли карбоксилатов (часто образующиеся in situ ) редко используются для этерификации, они реагируют с электрофильными алкилирующими агентами , такими как алкилгалогениды , с образованием сложных эфиров. [14] [18] Наличие анионов может ингибировать эту реакцию, что, соответственно, выгодно при использовании катализаторов межфазного переноса или таких высокополярных апротонных растворителей , как ДМФ . Дополнительная йодистая соль может посредством реакции Финкельштейна катализировать реакцию упорного алкилгалогенида. Альтернативно, соли координирующего металла, такого как серебро, могут улучшить скорость реакции за счет облегчения удаления галогенидов.
Широко практикуется переэтерификация , заключающаяся в превращении одного сложного эфира в другой:
Как и гидролиз, переэтерификация катализируется кислотами и основаниями. Реакция широко используется для разложения триглицеридов , например, при производстве эфиров жирных кислот и спиртов. Поли(этилентерефталат) получают переэтерификацией диметилтерефталата и этиленгликоля: [14]
Подвидом переэтерификации является алкоголиз дикетена . Эта реакция дает 2-кетоэфиры. [14]
Алкены подвергаются « гидроэтерификации » в присутствии металлических карбонильных катализаторов. Эфиры пропановой кислоты производятся в промышленных масштабах следующим методом:
Одним из показательных примеров является получение метилпропионата .
Карбонилирование метанола дает метилформиат , который является основным коммерческим источником муравьиной кислоты . Реакция катализируется метоксидом натрия :
При гидроэтерификации алкены и алкины встраиваются в связь OH карбоновых кислот. Винилацетат получают в промышленности добавлением уксусной кислоты к ацетилену в присутствии катализаторов из ацетата цинка : [19] В настоящее время в качестве катализатора используется ацетат цинка :
Винилацетат также можно получить катализируемой палладием реакцией этилена, уксусной кислоты и кислорода :
Кремневольфрамовая кислота используется для производства этилацетата путем алкилирования уксусной кислоты этиленом:
Реакция Тищенко включает диспропорционирование альдегида в присутствии безводного основания с образованием сложного эфира . Катализаторами являются алкоксиды алюминия или алкоксиды натрия. Бензальдегид реагирует с бензилоксидом натрия (полученным из натрия и бензилового спирта ) с образованием бензилбензоата . [20] Метод применяется при производстве этилацетата из ацетальдегида . [14]
Эфиры реагируют с нуклеофилами по карбонильному углероду. Карбонил слабо электрофилен, но подвергается атаке сильных нуклеофилов (аминов, алкоксидов, источников гидридов, литийорганических соединений и др.). Связи C–H, прилегающие к карбонилу, слабокислые, но подвергаются депротонированию сильными основаниями. Именно этот процесс обычно инициирует реакции конденсации. Карбонильный кислород в сложных эфирах является слабоосновным, в меньшей степени, чем карбонильный кислород в амидах из-за резонансного донорства электронной пары от азота в амидах, но образует аддукты .
Этерификация является обратимой реакцией. Сложные эфиры подвергаются гидролизу в кислых и основных условиях. В кислых условиях реакция является обратной реакцией этерификации Фишера . В основных условиях гидроксид действует как нуклеофил, а алкоксид — уходящая группа. Эта реакция, омыление , лежит в основе изготовления мыла.
Алкоксидная группа также может быть замещена более сильными нуклеофилами, такими как аммиак или первичные или вторичные амины , с образованием амидов : (реакция аммонолиза)
Эта реакция обычно необратима. Вместо аминов можно использовать гидразины и гидроксиламин. Эфиры могут быть преобразованы в изоцианаты через промежуточные гидроксамовые кислоты в перегруппировке Лоссена .
Источники углеродных нуклеофилов, например реактивы Гриньяра и литийорганические соединения, легко присоединяются к карбонилу.
По сравнению с кетонами и альдегидами сложные эфиры относительно устойчивы к восстановлению . Введение каталитического гидрирования в начале 20 века стало прорывом; эфиры жирных кислот гидрируются до жирных спиртов .
Типичным катализатором является хромит меди . До развития каталитического гидрирования сложные эфиры восстанавливались в больших масштабах с использованием восстановления Буво-Блана . В этом методе, который в значительной степени устарел, используется натрий в присутствии источников протонов.
Специально для тонкого химического синтеза алюмогидрид лития используется для восстановления сложных эфиров до двух первичных спиртов. Соответствующий реагент боргидрид натрия в этой реакции протекает медленно. ДИБАГ восстанавливает сложные эфиры до альдегидов. [24]
Прямое восстановление с получением соответствующего эфира затруднено, поскольку промежуточный полуацеталь имеет тенденцию разлагаться с образованием спирта и альдегида (который быстро восстанавливается с образованием второго спирта). Реакцию можно провести, используя триэтилсилан с различными кислотами Льюиса. [25] [26]
Что касается альдегидов , атомы водорода на атоме углерода, примыкающем («α к») к карбоксильной группе в сложных эфирах, достаточно кислые, чтобы подвергаться депротонированию, что, в свою очередь, приводит к множеству полезных реакций. Для депротонирования требуются относительно сильные основания, такие как алкоксиды . Депротонирование дает нуклеофильный енолят , который может далее реагировать, например, с конденсацией Кляйзена и ее внутримолекулярным эквивалентом, конденсацией Дикмана . Это преобразование используется в синтезе эфира малоновой кислоты , где диэфир малоновой кислоты реагирует с электрофилом (например, алкилгалогенидом ) и впоследствии декарбоксилируется. Другой вариант - алкилирование Фратера-Зеебаха .
Как класс, сложные эфиры служат защитными группами для карбоновых кислот . Защита карбоновой кислоты полезна при синтезе пептидов, чтобы предотвратить самореакции бифункциональных аминокислот . Метиловые и этиловые эфиры обычно доступны для многих аминокислот; т - бутиловый эфир имеет тенденцию быть более дорогим. Однако трет -бутиловые эфиры особенно полезны, поскольку в сильнокислых условиях трет -бутиловые эфиры подвергаются элиминированию с образованием карбоновой кислоты и изобутилена , что упрощает обработку.
Эфиры реагируют с сильными окисляющими кислотами , что может вызвать бурную реакцию, достаточно экзотермическую , чтобы воспламенить эфиры и продукты реакции. Тепло также выделяется при взаимодействии сложных эфиров с растворами щелочей . Очень легковоспламеняющийся газообразный водород образуется при смешивании сложных эфиров с щелочными металлами и ионными гидридами . [28]
Многие сложные эфиры имеют характерный фруктовый запах, и многие из них встречаются в природе в эфирных маслах растений. Это также привело к их широкому использованию в искусственных ароматизаторах и ароматизаторах, имитирующих эти запахи.
Перевод:б. Эстер или sauerstoffsäure Aetherarten.
Жанр «Эфиры тройки».
Viele Mineralische und Organische Sauerstoffsäuren treten mit einer Alkohol-Art unter Ausscheidung von Wasser zu neutralen flüchtigen ätherischen Verbindungen zusammen, welche man als gepaarte Verbindungen von Alkohol und Säuren-Wasser oder, nach der Radicaltheorie, als Salze betrachten kann, в welchen eine Säure mit Einem Эфир verbunden ist.
б. Сложный эфир или эфиры оксикислот.
Эфиры третьего типа.
Многие минеральные и органические кислоты, содержащие кислород, при отщеплении воды соединяются со спиртом с образованием нейтральных летучих эфирных соединений, которые можно рассматривать как сопряженные соединения спирта и кислоты с водой или, согласно теории радикалов, как соли. в котором кислота связана с эфиром.