Антитромбин (АТ) — небольшой гликопротеин , который инактивирует несколько ферментов системы свертывания крови . Это белок из 464 аминокислот, вырабатываемый печенью . Он содержит три дисульфидные связи и в общей сложности четыре возможных участка гликозилирования . α-Антитромбин — доминирующая форма антитромбина, обнаруженная в плазме крови , и имеет олигосахарид, занимающий каждый из его четырех участков гликозилирования. Один участок гликозилирования остается постоянно незанятым в минорной форме антитромбина, β-антитромбине. [5] Его активность многократно увеличивается антикоагулянтным препаратом гепарином , который усиливает связывание антитромбина с фактором IIa (тромбином) и фактором Xa . [6]
Антитромбин также называется антитромбином III (AT III). Обозначения от антитромбина I до антитромбина IV берут начало в ранних исследованиях, проведенных в 1950-х годах Сигерсом, Джонсоном и Феллом. [7]
Антитромбин I (AT I) относится к связыванию тромбина с фибрином после того, как тромбин активировал фибриноген в некаталитическом месте связывания тромбина. Антитромбин II (AT II) относится к кофактору в плазме, который вместе с гепарином препятствует взаимодействию тромбина и фибриногена . Антитромбин III (AT III) относится к веществу в плазме , которое инактивирует тромбин. Антитромбин IV (AT IV) относится к антитромбину, который активируется во время и вскоре после свертывания крови . [8] Только AT III и, возможно, AT I имеют медицинское значение. AT III обычно называют исключительно «антитромбином», и в этой статье обсуждается именно антитромбин III.

Период полураспада антитромбина в плазме крови составляет около 3 дней. [9] Нормальная концентрация антитромбина в плазме крови человека высока и составляет приблизительно 0,12 мг/мл, что эквивалентно молярной концентрации 2,3 мкМ. [10] Антитромбин был выделен из плазмы большого количества видов, помимо человека. [11] Как следует из секвенирования белков и кДНК , длина антитромбинов коровы, овцы, кролика и мыши составляет 433 аминокислоты, что на одну аминокислоту длиннее, чем у человеческого антитромбина. Предполагается, что дополнительная аминокислота находится в позиции аминокислоты 6. Антитромбины коровы, овцы, кролика, мыши и человека имеют от 84 до 89% идентичности аминокислотной последовательности. [12] Шесть аминокислот образуют три внутримолекулярные дисульфидные связи , Cys 8-Cys128, Cys21-Cys95 и Cys248-Cys430. Все они имеют четыре потенциальных сайта N-гликозилирования . Они встречаются в аминокислотах аспарагина (Asn) с номерами 96, 135, 155 и 192 у людей и в аналогичных аминокислотных номерах у других видов. Все эти сайты заняты ковалентно присоединенными боковыми цепями олигосахаридов в преобладающей форме человеческого антитромбина, α-антитромбине, что приводит к молекулярной массе этой формы антитромбина 58 200. [5] Потенциальный сайт гликозилирования в аспарагине 135 не занят в минорной форме (около 10%) антитромбина, β-антитромбине (см. Рисунок 1 ). [13]
Рекомбинантные антитромбины со свойствами, аналогичными свойствам нормального человеческого антитромбина, были получены с использованием инфицированных бакуловирусом клеток насекомых и клеточных линий млекопитающих, выращенных в клеточной культуре . [14] [15] [16] [17] Эти рекомбинантные антитромбины, как правило, имеют другие паттерны гликозилирования, чем нормальный антитромбин, и обычно используются в структурных исследованиях антитромбина. По этой причине многие из структур антитромбина, хранящихся в банке данных белков и представленных в этой статье, показывают различные паттерны гликозилирования.
Антитромбин начинает свое существование в своем нативном состоянии, которое имеет более высокую свободную энергию по сравнению с латентным состоянием, в которое он распадается в среднем через 3 дня. Латентное состояние имеет ту же форму, что и активированное состояние, то есть, когда оно ингибирует тромбин. Таким образом, это классический пример полезности кинетического и термодинамического контроля сворачивания белка.


Антитромбин представляет собой серпин (ингибитор сериновой протеазы) и поэтому по структуре схож с большинством других ингибиторов протеазы плазмы , таких как альфа-1-антихимотрипсин , альфа-2-антиплазмин и кофактор гепарина II .
Физиологические целевые протеазы антитромбина - это протеазы пути контактной активации (ранее известного как внутренний путь), а именно активированные формы фактора X (Xa), фактора IX (IXa), фактора XI (XIa), фактора XII (XIIa) и, в большей степени, фактора II (тромбина) (IIa), а также активированная форма фактора VII (VIIa) из пути тканевого фактора (ранее известного как внешний путь). [20] Ингибитор также инактивирует калликреин и плазмин [ требуется цитата ] , также участвующие в свертывании крови. Однако он инактивирует некоторые другие сериновые протеазы, которые не участвуют в свертывании, такие как трипсин и субъединица C1s фермента C1, участвующего в классическом пути комплемента . [12] [21]
Инактивация протеазы происходит в результате захвата протеазы в эквимолярном комплексе с антитромбином, в котором активный центр фермента протеазы недоступен для его обычного субстрата . [12] Образование комплекса антитромбин-протеаза включает взаимодействие между протеазой и специфической реактивной пептидной связью в антитромбине. В человеческом антитромбине эта связь находится между аргинином (arg) 393 и серином (ser) 394 (см. Рисунок 2 и Рисунок 3 ). [12]
Считается, что ферменты протеазы попадают в ловушку неактивных комплексов антитромбин-протеаза в результате их атаки на реактивную связь. Хотя атака на похожую связь в пределах нормального субстрата протеазы приводит к быстрому протеолитическому расщеплению субстрата, инициирование атаки на реактивную связь антитромбина заставляет антитромбин активироваться и захватывать фермент на промежуточной стадии протеолитического процесса. Со временем тромбин способен расщепить реактивную связь в пределах антитромбина, и неактивный комплекс антитромбин-тромбин будет диссоциировать, однако время, необходимое для этого, может быть больше 3 дней. [22] Однако связи P3-P4 и P1'-P2' могут быстро расщепляться нейтрофильной эластазой и бактериальным ферментом термолизином , соответственно, в результате чего неактивные антитромбины больше не способны ингибировать активность тромбина. [23]
Скорость ингибирования антитромбином активности протеазы значительно увеличивается за счет его дополнительного связывания с гепарином , как и его инактивация нейтрофильной эластазой . [23]
Антитромбин инактивирует свои физиологические целевые ферменты, тромбин, фактор Xa и фактор IXa с константами скорости 7–11 x 10 3 , 2,5 x 10 3 М −1 с −1 и 1 x 10 М −1 с −1 соответственно. [5] [24] Скорость инактивации антитромбина-тромбина увеличивается до 1,5–4 x 10 7 М −1 с −1 в присутствии гепарина, т. е. реакция ускоряется в 2000–4000 раз. [25] [26] [27] [28] Ингибирование фактора Xa ускоряется всего в 500–1000 раз в присутствии гепарина, а максимальная константа скорости в 10 раз ниже, чем у ингибирования тромбина. [25] [28] Скорость ингибирования антитромбина-фактора IXa увеличивается приблизительно в 1 миллион раз в присутствии гепарина и физиологических уровней кальция . [24]
AT-III связывается со специфической последовательностью сульфатирования пентасахарида, содержащейся в полимере гепарина
GlcNAc/NS(6S)-GlcA-GlcNS(3S,6S)-IdoA(2S)-GlcNS(6S)
При связывании с этой пентасахаридной последовательностью ингибирование активности протеазы усиливается гепарином в результате двух различных механизмов. [29] В одном механизме стимуляция гепарином фактора IXa и ингибирование Xa зависит от конформационного изменения в антитромбине, вовлекающего петлю реактивного сайта, и, таким образом, является аллостерическим . [30] В другом механизме стимуляция ингибирования тромбина зависит от образования тройного комплекса между AT-III, тромбином и гепарином. [30]

Усиление ингибирования факторов IXa и Xa требует минимальной последовательности пентасахарида гепарина. Конформационные изменения, которые происходят в антитромбине в ответ на связывание пентасахарида, хорошо документированы. [18] [31] [32]
При отсутствии гепарина аминокислоты P14 и P15 (см. Рисунок 3 ) из петли реактивного сайта встроены в основную часть белка (в частности, в верхнюю часть бета-слоя A). Эта особенность является общей с другими серпинами , такими как кофактор гепарина II , альфа-1-антихимотрипсин и MENT .
Конформационное изменение, наиболее значимое для ингибирования факторов IXa и Xa, включает аминокислоты P14 и P15 в N-концевой области петли реактивного сайта (обведено на рисунке 4, модель B ). Эта область была названа шарнирной областью. Конформационное изменение в шарнирной области в ответ на связывание гепарина приводит к вытеснению P14 и P15 из основной части белка, и было показано, что при предотвращении этого конформационного изменения не происходит повышенного ингибирования факторов IXa и Xa. [30] Считается, что повышенная гибкость, приданная петле реактивного сайта в результате конформационного изменения шарнирной области, является ключевым фактором, влияющим на повышенное ингибирование факторов IXa и Xa. Было подсчитано, что в отсутствие пентасахарида только одна из каждых 400 молекул антитромбина (0,25%) находится в активной конформации с вытесненными аминокислотами P14 и P15. [30]
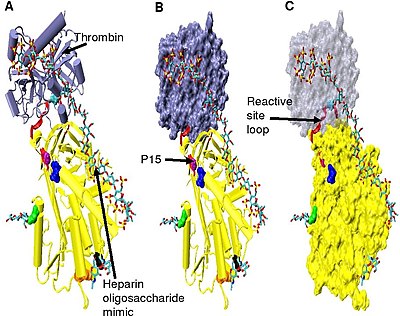
Повышенное ингибирование тромбина требует минимального пентасахарида гепарина плюс по крайней мере 13 дополнительных мономерных единиц. [33] Считается, что это связано с требованием, чтобы антитромбин и тромбин связывались с одной и той же цепью гепарина, смежной друг с другом. Это можно увидеть в серии моделей, показанных на рисунке 5 .
В структурах, показанных на рисунке 5, C-концевая часть (сторона P') петли реактивного сайта находится в расширенной конформации по сравнению с другими неактивированными или активированными гепарином структурами антитромбина. [34] Область P' антитромбина необычно длинная по сравнению с областью P' других серпинов и в неактивированных или активированных гепарином структурах антитромбина образует плотно связанный водородом β-поворот . Удлинение P' происходит посредством разрыва всех водородных связей, вовлеченных в β-поворот . [34]
Шарнирная область антитромбина в комплексе на рисунке 5 не может быть смоделирована из-за ее конформационной гибкости, и аминокислоты P9-P14 не видны в этой структуре. Эта конформационная гибкость указывает на то, что внутри комплекса может существовать равновесие между вставленной в петлю реактивного сайта P14 P15 конформацией антитромбина и выведенной из петли реактивного сайта P14 P15 конформацией. В поддержку этого, анализ позиционирования P15 Gly в комплексе на рисунке 5 (отмечено в модели B) показывает, что он вставлен в бета-слой A (см. модель C). [34]
α-Антитромбин и β-антитромбин различаются по своему сродству к гепарину. [35] Разница в константе диссоциации между ними составляет три раза для пентасахарида, показанного на рисунке 3 , и более чем в десять раз для полноразмерного гепарина, при этом β-антитромбин имеет более высокое сродство. [36] Считается, что более высокое сродство β-антитромбина обусловлено повышенной скоростью, с которой происходят последующие конформационные изменения внутри белка при первоначальном связывании гепарина. Для α-антитромбина дополнительное гликозилирование по Asn-135, как полагают, не мешает первоначальному связыванию гепарина, а скорее ингибирует любые возникающие конформационные изменения. [35]
Несмотря на то, что он присутствует только в 5–10% от уровня α-антитромбина, из-за его повышенного сродства к гепарину, считается, что β-антитромбин более важен, чем α-антитромбин, в контроле тромбогенных событий, возникающих в результате повреждения тканей. Действительно, ингибирование тромбина после повреждения аорты приписывалось исключительно β-антитромбину. [37]
Доказательства важной роли антитромбина в регуляции нормального свертывания крови демонстрируются корреляцией между унаследованным или приобретенным дефицитом антитромбина и повышенным риском развития тромботического заболевания у любого пораженного человека. [38] Дефицит антитромбина обычно выявляется, когда пациент страдает рецидивирующим венозным тромбозом и тромбоэмболией легочной артерии .
Приобретенный дефицит антитромбина возникает в результате трех совершенно разных механизмов. Первый механизм — повышенная экскреция, которая может возникнуть при почечной недостаточности, связанной с протеинурией нефротическим синдромом . Второй механизм возникает из-за снижения продукции, как это наблюдается при печеночной недостаточности или циррозе или незрелой печени вследствие преждевременных родов . Третий механизм возникает из-за ускоренного потребления, которое наиболее выражено как следствие тяжелой травмы , но также может наблюдаться в меньших масштабах в результате вмешательств, таких как крупная операция или сердечно-легочное шунтирование . [39]
Частота наследственного дефицита антитромбина оценивается в пределах от 1:2000 до 1:5000 в нормальной популяции, причем первая семья, страдающая наследственным дефицитом антитромбина, была описана в 1965 году. [40] [41] Впоследствии было предложено классифицировать наследственный дефицит антитромбина как тип I или тип II на основе функционального и иммунохимического анализа антитромбина. [42] Поддержание адекватного уровня активности антитромбина, который составляет не менее 70% от нормального функционального уровня, имеет важное значение для обеспечения эффективного ингибирования протеаз свертывания крови. [43] Обычно в результате дефицита антитромбина типа I или типа II функциональные уровни антитромбина снижаются до уровня ниже 50% от нормы. [44]
Дефицит антитромбина типа I характеризуется снижением как активности антитромбина, так и концентрации антитромбина в крови пораженных лиц. Дефицит типа I был первоначально далее разделен на две подгруппы, Ia и Ib, на основе сродства к гепарину. Антитромбин лиц подгруппы Ia показал нормальное сродство к гепарину, в то время как антитромбин лиц подгруппы Ib показал сниженное сродство к гепарину. [45] Последующий функциональный анализ группы случаев 1b показал, что у них не только сниженное сродство к гепарину, но и множественные или «плейотрофные» аномалии, влияющие на реактивный участок, участок связывания гепарина и концентрацию антитромбина в крови. В пересмотренной системе классификации, принятой Научным и стандартизационным комитетом Международного общества по тромбозу и гемостазу, случаи типа Ib теперь обозначаются как ЛЭ II типа, плейотрофный эффект. [46]
Большинство случаев дефицита I типа обусловлены точечными мутациями , делециями или незначительными вставками в гене антитромбина. Эти генетические мутации приводят к дефициту I типа посредством различных механизмов:
Дефицит антитромбина II типа характеризуется нормальными уровнями антитромбина, но сниженной активностью антитромбина в крови пораженных лиц. Первоначально было предложено, что дефицит II типа может быть далее разделен на три подгруппы (IIa, IIb и IIc) в зависимости от того, какая функциональная активность антитромбина снижена или сохранена. [45]
В пересмотренной системе классификации, вновь принятой Научным и стандартизационным комитетом Международного общества по тромбозу и гемостазу, дефицит антитромбина II типа по-прежнему подразделяется на три подгруппы: уже упомянутый тип II PE, а также тип II RS, где мутации влияют на реактивный сайт, и тип II HBS, где мутации влияют на сайт связывания антитромбина с гепарином. [46] Для целей базы данных мутаций антитромбина, составленной членами Подкомитета по ингибиторам свертывания плазмы Научного и стандартизационного комитета Международного общества по тромбозу и гемостазу, случаи типа IIa теперь классифицируются как тип II PE, случаи типа IIb как тип II RS и случаи типа IIc как тип II HBS. [49]
В настоящее время относительно легко охарактеризовать конкретную генетическую мутацию антитромбина. Однако до использования современных методов характеристики исследователи называли мутации по названию города, где проживал человек, страдающий от дефицита, т.е. мутация антитромбина была обозначена как топоним . [50] Современная мутационная характеристика с тех пор показала, что многие индивидуальные топонимы антитромбина на самом деле являются результатом одной и той же генетической мутации, например, антитромбин-Тояма эквивалентен антитромбин-Кумамото, -Амьен, -Тур, -Париж-1, -Париж-2, -Алжир, -Падуя-2 и -Барселона. [49]
Антитромбин используется в качестве терапевтического белка , который может быть очищен из плазмы человека [51] или получен рекомбинантным путем (например, Атрин, который производится из молока генетически модифицированных коз [52] [53] ).
Он одобрен FDA в качестве антикоагулянта для предотвращения образования тромбов до, во время или после операции или родов у пациентов с наследственным дефицитом антитромбина. [51] [53]
Он изучался при сепсисе для снижения диффузного внутрисосудистого свертывания и других последствий. Не было обнаружено, что он приносит какую-либо пользу тяжелобольным людям с сепсисом. [54]

Расщепление в реактивном сайте приводит к захвату тромбиновой протеазы с перемещением расщепленной петли реактивного сайта вместе со связанной протеазой, так что петля образует дополнительную шестую нить в середине бета-слоя А. Это перемещение петли реактивного сайта может быть также вызвано без расщепления, при этом результирующая кристаллографическая структура будет идентична структуре физиологически латентной конформации ингибитора активатора плазминогена-1 (PAI-1). [55] По этой причине конформация антитромбина, в которой петля реактивного сайта включена в нерасщепленном виде в основную часть белка, называется латентным антитромбином. В отличие от PAI-1 переход антитромбина из нормальной или нативной конформации в латентную конформацию необратим.
Нативный антитромбин может быть преобразован в латентный антитромбин (L-антитромбин) путем нагревания отдельно или в присутствии цитрата . [56] [57] Однако без экстремального нагревания и при температуре 37 °C (температура тела) 10% всего антитромбина, циркулирующего в крови, преобразуется в L-антитромбин в течение 24 часов. [58] [59] Структура L-антитромбина показана на рисунке 6 .
Трехмерная структура нативного антитромбина была впервые определена в 1994 году. [31] [32] Неожиданно белок кристаллизовался как гетеродимер, состоящий из одной молекулы нативного антитромбина и одной молекулы латентного антитромбина. Латентный антитромбин при образовании немедленно связывается с молекулой нативного антитромбина, образуя гетеродимер, и только когда концентрация латентного антитромбина превысит 50% от общего антитромбина, его можно будет обнаружить аналитически. [59] Латентная форма антитромбина не только неактивна против своих целевых протеаз коагуляции, но и ее димеризация с в остальном активной молекулой нативного антитромбина также приводит к инактивации нативных молекул. Физиологическое влияние потери активности антитромбина либо через латентное образование антитромбина, либо через последующее образование димера усугубляется предпочтением димеризации, происходящей между активированным гепарином β-антитромбином и латентным антитромбином, а не α-антитромбином. [59]
Также была выделена форма антитромбина, которая является промежуточным звеном в превращении нативной и латентной форм антитромбина, и она была названа прелатентным антитромбином . [60]
Ангиогенез — это физиологический процесс, включающий рост новых кровеносных сосудов из уже существующих. В нормальных физиологических условиях ангиогенез строго регулируется и контролируется балансом ангиогенных стимуляторов и ангиогенных ингибиторов . Рост опухоли зависит от ангиогенеза, и во время развития опухоли требуется устойчивая продукция ангиогенных стимулирующих факторов наряду с уменьшением количества ангиогенных ингибирующих факторов, вырабатываемых опухолевыми клетками. [61] Расщепленная и латентная форма антитромбина мощно ингибирует ангиогенез и рост опухоли в животных моделях. [62] Было показано, что прелатентная форма антитромбина ингибирует ангиогенез in vitro, но на сегодняшний день она не была протестирована в экспериментальных животных моделях.