

Цис - транс -изомерия , также известная как геометрическая изомерия , описывает определенные расположения атомов внутри молекул. Префиксы « цис » и « транс » происходят от латинского: «эта сторона» и «другая сторона» соответственно. [1] В контексте химии цис указывает на то, что функциональные группы (заместители) находятся на одной стороне некоторой плоскости, в то время как транс передает, что они находятся на противоположных (поперечных) сторонах. Цис - транс- изомеры являются стереоизомерами , то есть парами молекул, которые имеют одинаковую формулу, но чьи функциональные группы находятся в разных ориентациях в трехмерном пространстве. Цис- и транс -изомеры встречаются как в органических молекулах, так и в неорганических координационных комплексах. Цис- и транс -дескрипторы не используются для случаев конформационной изомерии , где две геометрические формы легко взаимопревращаются, таких как большинство структур с открытой цепью с одной связью; вместо этого используются термины « син » и « анти ».
Согласно ИЮПАК , «геометрическая изомерия» является устаревшим синонимом « цис - транс- изомерии». [2]
Цис-транс или геометрическая изомерия классифицируется как один из типов конфигурационной изомерии . [3]
Очень часто цис - транс -стереоизомеры содержат двойные связи или кольцевые структуры. В обоих случаях вращение связей ограничено или предотвращено. [4] Когда замещающие группы ориентированы в одном направлении, диастереомер называется цис , тогда как когда заместители ориентированы в противоположных направлениях, диастереомер называется транс . Примером небольшого углеводорода, демонстрирующего цис - транс -изомерию, является бут-2-ен . Другим примером является 1,2-дихлорциклогексан.
Цис- и транс- изомеры имеют различные физические свойства. Их различные формы влияют на дипольные моменты , температуру кипения и особенно плавления.
Эти различия могут быть очень небольшими, как в случае температуры кипения алкенов с прямой цепью, таких как пент-2-ен , которая составляет 37 °C в цис- изомере и 36 °C в транс- изомере. [5] Различия между цис- и транс -изомерами могут быть больше, если присутствуют полярные связи, как в 1,2-дихлорэтенах . Цис -изомер в этом случае имеет температуру кипения 60,3 °C, в то время как транс -изомер имеет температуру кипения 47,5 °C. [6] В цис -изомере два полярных дипольных момента связи C–Cl объединяются, образуя общий молекулярный диполь, так что возникают межмолекулярные диполь-дипольные силы (или силы Кисома), которые добавляются к силам дисперсии Лондона и повышают температуру кипения. С другой стороны, в транс- изомере этого не происходит, поскольку два момента связи C−Cl компенсируются, и молекула имеет нулевой дипольный момент (однако она имеет ненулевой квадрупольный момент ).
Различия в свойствах двух изомеров бутендиовой кислоты часто весьма различны.
Полярность является ключевым фактором в определении относительной температуры кипения, поскольку сильные межмолекулярные силы повышают температуру кипения. Таким же образом, симметрия является ключевым фактором в определении относительной температуры плавления, поскольку она обеспечивает лучшую упаковку в твердом состоянии, даже если это не изменяет полярность молекулы. Другим примером этого является связь между олеиновой кислотой и элаидиновой кислотой ; олеиновая кислота, цис- изомер, имеет температуру плавления 13,4 °C, что делает ее жидкостью при комнатной температуре, в то время как транс -изомер, элаидиновая кислота, имеет гораздо более высокую температуру плавления 43 °C из-за того, что более прямой транс -изомер способен упаковываться более плотно и является твердым при комнатной температуре.
Таким образом, транс -алкены, которые менее полярны и более симметричны, имеют более низкие температуры кипения и более высокие температуры плавления, а цис- алкены, которые, как правило, более полярны и менее симметричны, имеют более высокие температуры кипения и более низкие температуры плавления.
В случае геометрических изомеров, которые являются следствием двойных связей, и, в частности, когда оба заместителя одинаковы, обычно сохраняются некоторые общие тенденции. Эти тенденции можно объяснить тем фактом, что диполи заместителей в цис- изомере будут складываться, давая общий молекулярный диполь. В транс- изомере диполи заместителей будут нейтрализовываться [7] из-за того, что они находятся на противоположных сторонах молекулы. Транс- изомеры также имеют тенденцию иметь более низкую плотность, чем их цис- аналоги. [ необходима цитата ]
Как правило, транс- алкены имеют более высокие температуры плавления и более низкую растворимость в инертных растворителях, поскольку транс -алкены, в целом, более симметричны, чем цис -алкены. [8]
Вицинальные константы связи ( 3 J HH ), измеренные с помощью ЯМР-спектроскопии , больше для транс-изомеров (диапазон: 12–18 Гц; типично: 15 Гц), чем для цис- изомеров (диапазон: 0–12 Гц; типично: 8 Гц). [9]
Обычно для ациклических систем транс -изомеры более стабильны, чем цис -изомеры. Это различие объясняется неблагоприятным стерическим взаимодействием заместителей в цис -изомере. Поэтому транс- изомеры имеют менее экзотермическую теплоту сгорания , что указывает на более высокую термохимическую стабильность. [8] В наборе данных по аддитивности группы теплоты образования Бенсона цис -изомеры страдают от штрафа за стабильность в 1,10 ккал/моль. Существуют исключения из этого правила, такие как 1,2-дифторэтилен , 1,2-дифтордиазен (FN=NF) и несколько других галоген- и кислородзамещенных этиленов. В этих случаях цис -изомер более стабилен, чем транс -изомер. [10] Это явление называется цис-эффектом . [11]

В принципе, цис - транс- обозначение не следует использовать для алкенов с двумя или более различными заместителями. Вместо этого используется обозначение E - Z , основанное на приоритете заместителей с использованием правил приоритета Кана-Ингольда-Прелога (CIP) для абсолютной конфигурации. Стандартные обозначения IUPAC E и Z являются однозначными во всех случаях и, следовательно, особенно полезны для три- и тетразамещенных алкенов, чтобы избежать путаницы относительно того, какие группы идентифицируются как цис- или транс- по отношению друг к другу.
Z (от немецкого zusammen ) означает «вместе». E (от немецкого entgegen ) означает «противоположный» в смысле «противоположный». То есть Z имеет группы с более высоким приоритетом в цис-положении друг к другу, а E имеет группы с более высоким приоритетом в транс-положении друг к другу. Обозначается ли молекулярная конфигурация как E или Z , определяется правилами CIP; более высокие атомные номера имеют более высокий приоритет. Для каждого из двух атомов в двойной связи необходимо определить приоритет каждого заместителя. Если оба заместителя с более высоким приоритетом находятся на одной стороне , расположение будет Z ; если на противоположных сторонах, расположение будет E.
Поскольку системы цис – транс и E – Z сравнивают разные группы на алкене, не совсем верно, что Z соответствует цис , а E соответствует транс . Например, транс -2-хлорбут-2-ен (две метильные группы, C1 и C4, на остове бут-2-ена находятся в транс-положении друг к другу) представляет собой ( Z )-2-хлорбут-2-ен (хлор и C4 находятся вместе, поскольку C1 и C4 противоположны).
Волнистые одинарные связи являются стандартным способом представления неизвестной или неопределенной стереохимии или смеси изомеров (как в случае с тетраэдрическими стереоцентрами). Иногда использовалась перекрещенная двойная связь; она больше не считается приемлемым стилем для общего использования ИЮПАК , но все еще может потребоваться для компьютерного программного обеспечения. [12]
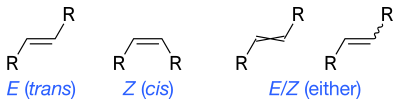
Цис - транс- изомерия может наблюдаться и в неорганических соединениях.
Диазены (и родственные им дифосфены ) также могут проявлять цис - транс -изомерию. Как и в случае с органическими соединениями, цис- изомер обычно более реакционноспособен из двух, являясь единственным изомером, который может восстанавливать алкены и алкины до алканов , но по другой причине: транс -изомер не может выстроить свои водороды подходящим образом для восстановления алкена, а цис -изомер, имеющий другую форму, может.
Координационные комплексы с октаэдрической или плоскоквадратной геометрией также могут проявлять цис-транс -изомерию.
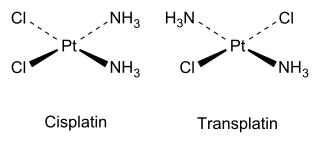
Например, существует два изомера квадратного плоского Pt(NH 3 ) 2 Cl 2 , как объяснил Альфред Вернер в 1893 году. Цис- изомер, полное название которого цис -диамминдихлорплатина(II), как было показано в 1969 году Барнеттом Розенбергом, обладает противоопухолевой активностью, и в настоящее время является химиотерапевтическим препаратом, известным под коротким названием цисплатин . Напротив, транс -изомер ( трансплатин ) не обладает полезной противораковой активностью. Каждый изомер может быть синтезирован с использованием транс-эффекта для контроля того, какой изомер производится.
Для октаэдрических комплексов формулы MX 4 Y 2 также существуют два изомера. (Здесь M — атом металла, а X и Y — два разных типа лигандов .) В цис- изомере два лиганда Y расположены рядом друг с другом под углом 90°, как это верно для двух атомов хлора, показанных зеленым в цис- [Co(NH 3 ) 4 Cl 2 ] + , слева. В транс- изомере, показанном справа, два атома Cl находятся по разные стороны от центрального атома Co.
Связанный тип изомерии в октаэдрических комплексах MX 3 Y 3 — это фасеточно-меридиональная (или fac – mer ) изомерия, в которой различное количество лигандов находится в цис- или транс-положении друг к другу. Металлокарбонильные соединения можно охарактеризовать как fac или mer с помощью инфракрасной спектроскопии .