5-Метилцитозин представляет собой метилированную форму цитозина основания ДНК ( C), которая регулирует транскрипцию генов и выполняет ряд других биологических функций. [1] Когда цитозин метилируется, ДНК сохраняет ту же последовательность, но экспрессия метилированных генов может быть изменена (изучение этого является частью области эпигенетики ). 5-Метилцитозин включен в состав нуклеозида 5-метилцитидина .
В 5-метилцитозине метильная группа присоединена к 5-му атому 6-атомного кольца, считая против часовой стрелки от NH-связанного азота в положении «шесть часов». Эта метильная группа отличает 5-метилцитозин от цитозина.
Пытаясь выделить бактериальный токсин , вызывающий туберкулез , В. Г. Руппель в 1898 году выделил из туберкулезной палочки новую нуклеиновую кислоту , названную туберкулиновой кислотой . [2] Нуклеиновая кислота оказалась необычной, поскольку она содержала помимо тимина , гуанина и цитозина , метилированный нуклеотид. В 1925 году Джонсон и Когхилл успешно обнаружили незначительное количество метилированного производного цитозина как продукта гидролиза туберкулиновой кислоты серной кислотой . [3] [4] Этот отчет подвергся резкой критике, поскольку их идентификация была основана исключительно на оптических свойствах кристаллического пикрата , а другим ученым не удалось воспроизвести тот же результат. [5] Но его существование было окончательно доказано в 1948 году, когда Хочкисс отделил нуклеиновые кислоты ДНК из тимуса теленка с помощью бумажной хроматографии , с помощью которой он обнаружил уникальный метилированный цитозин, совершенно отличный от обычных цитозина и урацила . [6] Спустя семь десятилетий выяснилось, что это также общая черта для разных молекул РНК , хотя точная роль неясна. [7]
Функция этого химического вещества значительно различается у разных видов: [8]
В то время как спонтанное дезаминирование цитозина образует урацил , который распознается и удаляется ферментами репарации ДНК, дезаминирование 5-метилцитозина образует тимин . Это преобразование основания ДНК из цитозина (C) в тимин (T) может привести к переходной мутации . [11] Кроме того, активное ферментативное дезаминирование цитозина или 5-метилцитозина с помощью цитозиндезаминаз семейства APOBEC может иметь благотворное влияние на различные клеточные процессы, а также на эволюцию организма. [12] С другой стороны, последствия дезаминирования 5-гидроксиметилцитозина остаются менее изученными.
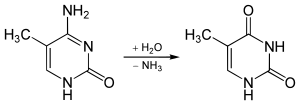
Группа NH 2 может быть удалена (дезаминирование) из 5-метилцитозина с образованием тимина с использованием таких реагентов, как азотистая кислота ; цитозин дезаминирует до урацила (U) в аналогичных условиях. [ нужна цитата ]
5-метилцитозин устойчив к дезаминированию при обработке бисульфитом , который дезаминирует остатки цитозина. Это свойство часто используется для анализа закономерностей метилирования цитозина ДНК с помощью бисульфитного секвенирования . [13]
Метки 5mC наносятся на геномную ДНК с помощью ДНК-метилтрансфераз (DNMT). У человека имеется 5 DNMT: DNMT1, DNMT2, DNMT3A, DNMT3B и DNMT3L, а в водорослях и грибах присутствуют еще 3 (DNMT4, DNMT5 и DNMT6). [14] DNMT1 содержит последовательность, нацеленную на фокусы репликации (RFTS) и домен CXXC, которые катализируют добавление меток 5mC. RFTS направляет DNMT1 к локусам репликации ДНК, чтобы помочь поддерживать 5mC на дочерних цепях во время репликации ДНК, тогда как CXXC содержит домен цинкового пальца для добавления метилирования к ДНК de novo . [15] Было обнаружено, что DNMT1 является преобладающей ДНК-метилтрансферазой во всех тканях человека. [16] В первую очередь, DNMT3A и DNMT3B отвечают за метилирование de novo , а DNMT1 сохраняет отметку 5mC после репликации. [1] DNMT могут взаимодействовать друг с другом, увеличивая способность к метилированию. Например, 2 DNMT3L может образовывать комплекс с 2 DNMT3A для улучшения взаимодействия с ДНК, способствуя метилированию. [17] Изменения в экспрессии DNMT приводят к аберрантному метилированию. Сверхэкспрессия приводит к усилению метилирования, тогда как нарушение работы фермента снижает уровень метилирования. [16]

Механизм присоединения следующий: сначала остаток цистеина в мотиве PCQ DNMT создает нуклеофильную атаку по углероду 6 на нуклеотид цитозина, который должен быть метилирован. Затем S-аденозилметионин отдает метильную группу углероду 5. Основание фермента DNMT депротонирует остаточный водород на углероде 5, восстанавливая двойную связь между атомами углерода 5 и 6 в кольце, образуя пару оснований 5-метилцитозин. [15]
После того как цитозин метилируется до 5mC, его можно вернуть в исходное состояние с помощью нескольких механизмов. Пассивное деметилирование ДНК путем разведения метку постепенно устраняет за счет репликации из-за отсутствия поддержки со стороны DNMT. При активном деметилировании ДНК серия окислений превращает ее в 5-гидроксиметилцитозин (5hmC), 5-формилцитозин (5fC) и 5-карбоксилцитозин (5caC), а последние два в конечном итоге вырезаются тимин-ДНК-гликозилазой (TDG), а затем путем эксцизионной репарации оснований (BER) для восстановления цитозина. [1] Нокаут TDG привел к двукратному увеличению 5fC без каких-либо статистически значимых изменений до уровней 5hmC, что указывает на то, что 5mC должен быть итеративно окислен как минимум дважды перед его полным деметилированием. [18] Окисление происходит посредством диоксигеназ семейства TET (Ten-eleven translocation) ( ферментов TET ), которые могут превращать 5mC, 5hmC и 5fC в их окисленные формы. Однако наибольшее предпочтение фермент имеет к 5mC, а начальная скорость реакции превращений 5hmC и 5fC с помощью ТЕТ2 в 4,9-7,6 раза медленнее. [19] ТЕТ требует Fe(II) в качестве кофактора, а также кислорода и α-кетоглутарата (α-KG) в качестве субстратов, причем последний субстрат образуется из изоцитрата с помощью фермента изоцитратдегидрогеназы (IDH). [20] Однако рак может производить 2-гидроксиглутарат (2HG), который конкурирует с α-KG, снижая активность ТЕТ и, в свою очередь, уменьшая превращение 5mC в 5hmC. [21]
При раке ДНК может стать как чрезмерно метилированной, называемой гиперметилированием , так и недостаточно метилированной, называемой гипометилированием. [22] Островки CpG, перекрывающие промоторы генов, метилируются de novo , что приводит к аберрантной инактивации генов, обычно связанных с ингибированием роста опухолей (пример гиперметилирования). [23] Сравнивая опухоль и нормальную ткань, первая имела повышенные уровни метилтрансфераз DNMT1, DNMT3A и, главным образом, DNMT3B, все из которых связаны с аномальными уровнями 5mC при раке. [16] Повторяющиеся последовательности в геноме, включая сателлитную ДНК, Alu и длинные вкрапления элементов (LINE), часто наблюдаются гипометилированными при раке, что приводит к экспрессии этих обычно молчащих генов, а уровни часто являются важными маркерами прогрессирования опухоли. [22] Была выдвинута гипотеза, что существует связь между гиперметилированием и гипометилированием; Повышенная активность ДНК-метилтрансфераз, которые вызывают аномальное метилирование 5mC de novo , может быть компенсирована удалением метилирования, типом эпигенетической репарации. Однако удаление метилирования неэффективно, что приводит к чрезмерному гипометилированию всего генома. Возможно и обратное; Чрезмерная экспрессия гипометилирования может быть подавлена за счет полногеномного гиперметилирования. [22] Отличительные способности рака, вероятно, приобретаются посредством эпигенетических изменений, которые изменяют 5mC как в раковых клетках, так и в окружающей опухоль-ассоциированной строме в микроокружении опухоли. [24] Сообщалось, что противораковый препарат Цисплатин вступает в реакцию с 5mC. [25]
«Эпигенетический возраст» относится к связи между хронологическим возрастом и уровнем метилирования ДНК в геноме. [26] Сочетание уровней метилирования ДНК в определенных наборах CpG, называемых «часовыми CpG», с алгоритмами, которые регрессируют типичные уровни коллективного метилирования всего генома в заданном хронологическом возрасте, позволяют прогнозировать эпигенетический возраст. В молодости (0–20 лет) изменения в метилировании ДНК происходят быстрее по мере развития и роста, а в старшем возрасте эти изменения начинают замедляться. Существует множество эпигенетических оценок возраста. Часы Хорвата измеряют набор из 353 CpG, состоящий из нескольких тканей, половина из которых положительно коррелирует с возрастом, а другая половина отрицательно, для оценки эпигенетического возраста. [27] Часы Ханнума используют образцы крови взрослых для расчета возраста на основе ортогональной основы 71 CpG. [28] Часы Левина, известные как DNAm PhenoAge, зависят от 513 CpG и превосходят другие средства оценки возраста в прогнозировании смертности и продолжительности жизни, но при этом демонстрируют смещение в отношении тканей, не относящихся к крови. [29] Имеются сообщения об оценщиках возраста с состоянием метилирования только одного CpG в гене ELOVL2. [30] Оценка возраста позволяет прогнозировать продолжительность жизни на основе ожиданий возрастных состояний, которым могут подвергаться люди, на основе их маркеров метилирования 5mC. [ нужна цитата ]