Углекислый газ представляет собой химическое соединение с химической формулой CO 2 . Он состоит из молекул , каждая из которых имеет один атом углерода , ковалентно связанный двойной связью с двумя атомами кислорода . Он находится в газообразном состоянии при комнатной температуре, и в качестве источника доступного углерода в углеродном цикле атмосферный CO 2 является основным источником углерода для жизни на Земле. В воздухе углекислый газ прозрачен для видимого света, но поглощает инфракрасное излучение , действуя как парниковый газ . Углекислый газ растворим в воде и содержится в грунтовых водах , озерах , ледяных шапках и морской воде . При растворении углекислого газа в воде образуется карбонат и преимущественно бикарбонат ( HCO−3), что вызывает закисление океана по мере увеличения уровня CO 2 в атмосфере . [9]
Это примесный газ в атмосфере Земли с концентрацией 421 частей на миллион (ppm) [примечание 1] , или около 0,04% (по состоянию на май 2022 года), по сравнению с доиндустриальным уровнем в 280 частей на миллион или около 0,025%. [11] [12] Сжигание ископаемого топлива является основной причиной увеличения концентрации CO 2 , а также основной причиной изменения климата . [13]
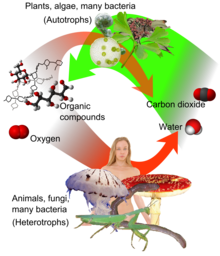
Его концентрация в доиндустриальной атмосфере Земли с конца докембрия регулировалась организмами и геологическими явлениями. Растения , водоросли и цианобактерии используют энергию солнечного света для синтеза углеводов из углекислого газа и воды в процессе, называемом фотосинтезом , в результате которого в качестве побочного продукта образуется кислород. [14] В свою очередь, кислород потребляется, а CO 2 выделяется в качестве отходов всеми аэробными организмами , когда они метаболизируют органические соединения для производства энергии путем дыхания . [15] CO 2 выделяется из органических материалов при их разложении или горении, например, при лесных пожарах. Поскольку растениям требуется CO 2 для фотосинтеза, а люди и животные зависят от растений как источника пищи, CO 2 необходим для выживания жизни на Земле.
Углекислый газ на 53% плотнее сухого воздуха, но долговечен и тщательно смешивается в атмосфере. Около половины избыточных выбросов CO 2 в атмосферу поглощается поглотителями углерода на суше и в океане . [16] Эти поглотители могут стать насыщенными и летучими, поскольку гниение и лесные пожары приводят к выбросу CO 2 обратно в атмосферу. [17] CO 2 в конечном итоге изолируется (хранится в течение длительного времени) в горных породах и органических отложениях, таких как уголь , нефть и природный газ . Связанный CO 2 выбрасывается в атмосферу при сжигании ископаемого топлива или естественным путем из-за вулканов , горячих источников , гейзеров , а также когда карбонатные породы растворяются в воде или реагируют с кислотами.
CO 2 является универсальным промышленным материалом, используемым, например, в качестве инертного газа в сварке и огнетушителях , в качестве сжимающего газа в пневматических пистолетах и нефтедобыче, а также в качестве сверхкритического жидкого растворителя при декофеинизации кофе и сверхкритической сушке . [18] Это побочный продукт ферментации сахара при производстве хлеба , пива и вина , и его добавляют в газированные напитки, такие как сельтерская вода и пиво, для придания шипучести. Он имеет резкий и кислый запах и создает во рту привкус газированной воды , но в обычно встречающихся концентрациях не имеет запаха. [1]
Симметрия молекулы углекислого газа в равновесной геометрии линейна и центросимметрична . Длина связи углерод -кислород в диоксиде углерода составляет 116,3 пм , что заметно короче , чем длина типичной одинарной связи C-O, составляющая примерно 140 пм, и короче, чем у большинства других функциональных групп с многократными связями C-O , таких как карбонилы . [19] Поскольку молекула центросимметрична, она не имеет электрического дипольного момента .

Как линейная трехатомная молекула, CO 2 имеет четыре моды колебаний , как показано на схеме. В симметричном и антисимметричном режимах растяжения атомы движутся вдоль оси молекулы. Существуют две изгибные моды, которые являются вырожденными , что означает, что они имеют одинаковую частоту и одинаковую энергию из-за симметрии молекулы. Когда молекула касается поверхности или другой молекулы, две моды изгиба могут различаться по частоте, поскольку взаимодействие этих двух мод различно. Некоторые из колебательных мод наблюдаются в инфракрасном (ИК) спектре : антисимметричная мода растяжения с волновым числом 2349 см -1 (длина волны 4,25 мкм) и вырожденная пара изгибных мод при 667 см -1 (длина волны 15 мкм). Симметричная мода растяжения не создает электрический диполь, поэтому не наблюдается в ИК-спектроскопии, но обнаруживается с помощью спектроскопии комбинационного рассеяния света при 1388 см -1 (длина волны 7,2 мкм). [20]
В газовой фазе молекулы углекислого газа испытывают значительные колебательные движения и не сохраняют фиксированной структуры. Однако в эксперименте по визуализации кулоновского взрыва можно получить мгновенное изображение молекулярной структуры. Подобный эксперимент [21] был проведен для углекислого газа. Результатом этого эксперимента и выводом теоретических расчетов [22] , основанных на ab initio поверхности потенциальной энергии молекулы, является то, что ни одна из молекул в газовой фазе никогда не бывает точно линейной. Этот противоречивый результат тривиально обусловлен тем фактом, что элемент объема движения ядра исчезает для линейных геометрий. [22] Это справедливо для всех молекул (кроме двухатомных!).
Углекислый газ растворим в воде, в которой обратимо образует H 2 CO 3 (угольную кислоту), которая является слабой кислотой , так как ее ионизация в воде неполная.
Константа гидратного равновесия угольной кислоты при 25 °C равна:
Следовательно, большая часть углекислого газа не превращается в угольную кислоту, а остается в виде молекул CO 2 , не влияя на pH.
Относительные концентрации CO 2 , H 2 CO 3 и депротонированных форм HCO−3( бикарбонат ) и CO2-3( карбонатные ) зависят от pH . Как показано на графике Бьеррума , в нейтральной или слабощелочной воде (рН > 6,5) преобладает бикарбонатная форма (>50%), становясь наиболее распространенной (>95%) при рН морской воды. В очень щелочной воде (рН > 10,4) преобладающей (>50%) формой является карбонатная. Океаны, будучи слабощелочными с типичным pH = 8,2–8,5, содержат около 120 мг бикарбоната на литр.
Будучи дипротонной , угольная кислота имеет две константы кислотной диссоциации , первая из которых соответствует диссоциации на ион бикарбоната (также называемый гидрокарбонатом) ( HCO−3):
Это истинная первая константа диссоциации кислоты, определяемая как
где знаменатель включает только ковалентно связанную H 2 CO 3 и не включает гидратированный CO 2 (водн.). Гораздо меньшее и часто цитируемое значение около 4,16 × 10 -7 представляет собой кажущееся значение, рассчитанное на (неверном) предположении, что весь растворенный CO 2 присутствует в виде угольной кислоты, так что
Поскольку большая часть растворенного CO 2 остается в виде молекул CO 2 , K a1 (кажущийся) имеет гораздо больший знаменатель и гораздо меньшее значение, чем истинный K a1 . [23]
Ион бикарбоната представляет собой амфотерную разновидность, которая может действовать как кислота или как основание, в зависимости от pH раствора. При высоком pH он значительно диссоциирует на карбонат- ион ( CO2-3):
В организмах производство углекислоты катализируется ферментом, известным как карбоангидраза .
CO 2 является сильным электрофилом, имеющим электрофильную реакционную способность, сравнимую с бензальдегидом или сильными α,β-ненасыщенными карбонильными соединениями . Однако в отличие от электрофилов с аналогичной реакционной способностью реакции нуклеофилов с CO 2 термодинамически менее выгодны и часто оказываются весьма обратимыми. [24] Обратимая реакция диоксида углерода с аминами с образованием карбаматов используется в скрубберах CO 2 и была предложена в качестве возможной отправной точки для улавливания и хранения углерода путем очистки газа амином . Только очень сильные нуклеофилы, такие как карбанионы , образующиеся в реактивах Гриньяра , и литийорганические соединения реагируют с CO 2 с образованием карбоксилатов :
В комплексах металлов с углекислым газом CO 2 служит лигандом , который может способствовать превращению CO 2 в другие химические вещества. [25]
Восстановление CO 2 до CO обычно представляет собой сложную и медленную реакцию:
Фотоавтотрофы (т.е. растения и цианобактерии ) используют энергию, содержащуюся в солнечном свете, для фотосинтеза простых сахаров из CO2 , поглощенного из воздуха и воды:
Окислительно -восстановительный потенциал для этой реакции вблизи pH 7 составляет около -0,53 В по сравнению со стандартным водородным электродом . Этот процесс катализирует никельсодержащий фермент дегидрогеназа монооксида углерода . [26]

Углекислый газ бесцветен. При низких концентрациях газ не имеет запаха; однако при достаточно высоких концентрациях он имеет резкий кислый запах. [1] При стандартной температуре и давлении плотность углекислого газа составляет около 1,98 кг/м 3 , что примерно в 1,53 раза выше плотности воздуха . [27]
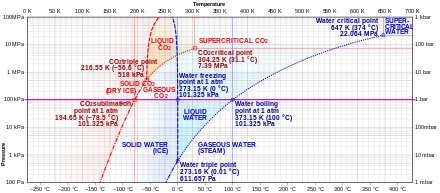
Углекислый газ не имеет жидкого состояния при давлениях ниже 0,51795(10) МПа [2] (5,11177(99) атм ). При давлении 1 атм (0,101325 МПа) газ осаждается непосредственно в твердое тело при температуре ниже 194,6855(30) К [2] (-78,4645(30) °С), а твердое тело сублимируется непосредственно в газ выше этой температуры. В твердом состоянии углекислый газ обычно называют сухим льдом .

Жидкий углекислый газ образуется только при давлениях выше 0,51795(10) МПа [2] (5,11177(99) атм); тройная точка углекислого газа — 216,592(3) К [2] (-56,558(3) °С) при 0,51795(10) МПа [2] (5,11177(99) атм) (см. фазовую диаграмму). Критическая точка — 304,128(15) К [2] (30,978(15) °С) при 7,3773(30) МПа [2] (72,808(30) атм). Другая форма твердого диоксида углерода, наблюдаемая при высоком давлении, представляет собой аморфное стеклоподобное твердое вещество. [28] Эта форма стекла, называемая карбонией , производится путем переохлаждения нагретого CO 2 при экстремальных давлениях (40–48 ГПа , или около 400 000 атмосфер) на алмазной наковальне . Это открытие подтвердило теорию о том, что углекислый газ может существовать в стеклянном состоянии, подобно другим членам своего элементарного семейства, таким как диоксид кремния (силикатное стекло) и диоксид германия . Однако, в отличие от кварцевого и германиевого стекла, карбониевое стекло не стабильно при нормальном давлении и превращается в газ при сбросе давления.
При температуре и давлении выше критической точки диоксид углерода ведет себя как сверхкритическая жидкость , известная как сверхкритический диоксид углерода .
Таблица теплофизических свойств насыщенной жидкой углекислоты: [29] [30]
Таблица теплофизических свойств углекислого газа (СО 2 ) при атмосферном давлении: [29] [30]
Углекислый газ является конечным продуктом клеточного дыхания в организмах, которые получают энергию путем расщепления сахаров, жиров и аминокислот кислородом в рамках своего метаболизма . Сюда входят все растения, водоросли и животные, а также аэробные грибы и бактерии. У позвоночных животных углекислый газ перемещается с кровью от тканей организма к коже (например, земноводным ) или жабрам (например, рыбам ), откуда он растворяется в воде, или к легким, откуда он выдыхается. Во время активного фотосинтеза растения могут поглощать из атмосферы больше углекислого газа, чем выделяют при дыхании.
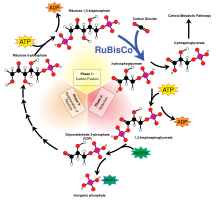
Фиксация углерода — это биохимический процесс, посредством которого углекислый газ из атмосферы включается растениями, водорослями и (цианобактериями) в богатые энергией органические молекулы, такие как глюкоза , создавая таким образом собственную пищу посредством фотосинтеза. Фотосинтез использует углекислый газ и воду для производства сахаров, из которых могут быть построены другие органические соединения , а кислород производится в качестве побочного продукта.
Рибулозо-1,5-бисфосфаткарбоксилаза оксигеназа , обычно сокращенно RuBisCO, представляет собой фермент , участвующий в первой основной стадии фиксации углерода, производстве двух молекул 3-фосфоглицерата из CO 2 и рибулозобисфосфата , как показано на диаграмме левый.
RuBisCO считается самым распространенным белком на Земле. [31]
Фототрофы используют продукты своего фотосинтеза как внутренние источники питания и как сырье для биосинтеза более сложных органических молекул, таких как полисахариды , нуклеиновые кислоты и белки. Они используются для собственного роста, а также в качестве основы пищевых цепей и сетей, питающих другие организмы, включая таких животных, как мы. Некоторые важные фототрофы, кокколитофоры, синтезируют твердые чешуйки карбоната кальция . [32] Всемирно значимым видом кокколитофоров является Emiliania huxleyi , чьи кальцитовые чешуйки сформировали основу многих осадочных пород , таких как известняк , где то, что раньше было атмосферным углеродом, может оставаться фиксированным в течение геологических временных масштабов.
Растения могут расти на 50% быстрее при концентрации CO 2 1000 ppm по сравнению с условиями окружающей среды, хотя это предполагает отсутствие изменений в климате и отсутствие ограничений на другие питательные вещества. [33] Повышенные уровни CO 2 вызывают увеличение роста, что отражается на урожайности сельскохозяйственных культур: пшеница, рис и соя демонстрируют увеличение урожайности на 12–14% при повышенном уровне CO 2 в экспериментах FACE. [34] [35]
Увеличение концентрации CO 2 в атмосфере приводит к уменьшению количества устьиц на растениях [36] , что приводит к снижению потребления воды и повышению эффективности водопользования . [37] Исследования с использованием FACE показали, что обогащение CO 2 приводит к снижению концентрации микроэлементов в сельскохозяйственных растениях. [38] Это может иметь побочные эффекты и на других частях экосистем , поскольку травоядным животным придется есть больше пищи, чтобы получить такое же количество белка. [39]
Концентрация вторичных метаболитов, таких как фенилпропаноиды и флавоноиды, также может изменяться у растений, подвергающихся воздействию высоких концентраций CO 2 . [40] [41]
Растения также выделяют CO 2 во время дыхания, поэтому большинство растений и водорослей, которые используют фотосинтез C3 , являются лишь чистыми поглотителями в течение дня. Хотя растущий лес будет поглощать много тонн CO 2 каждый год, зрелый лес будет производить столько же CO 2 в результате дыхания и разложения мертвых образцов (например, опавших ветвей), сколько используется в фотосинтезе растущих растений. [42] Вопреки давнему мнению, что они являются углеродно-нейтральными, зрелые леса могут продолжать накапливать углерод [43] и оставаться ценными поглотителями углерода , помогая поддерживать углеродный баланс атмосферы Земли. Кроме того, что имеет решающее значение для жизни на Земле, фотосинтез фитопланктона потребляет растворенный CO 2 в верхних слоях океана и тем самым способствует поглощению CO 2 из атмосферы. [44]

Содержание углекислого газа в свежем воздухе (в среднем между уровнем моря и уровнем 10 кПа, т. е. на высоте около 30 км (19 миль)) варьируется от 0,036% (360 частей на миллион) до 0,041% (412 частей на миллион), в зависимости от местоположения. [46]
CO 2 является удушающим газом и не классифицируется как токсичный или вредный в соответствии со стандартами Согласованной на глобальном уровне системы классификации и маркировки химических веществ Европейской экономической комиссии Организации Объединенных Наций с использованием Руководящих принципов ОЭСР по испытанию химических веществ . В концентрации до 1% (10 000 частей на миллион) у некоторых людей он вызывает сонливость и ощущение заложенности легких. [45] Концентрации от 7% до 10% (от 70 000 до 100 000 частей на миллион) могут вызвать удушье даже при наличии достаточного количества кислорода, что проявляется в виде головокружения, головной боли, нарушения зрения и слуха, а также потери сознания в течение от нескольких минут до часа. [47] Физиологические эффекты острого воздействия углекислого газа группируются под термином «гиперкапния» , разновидность асфиксии .
Поскольку он тяжелее воздуха, в местах, где газ просачивается из-под земли (из-за подповерхностной вулканической или геотермальной активности) в относительно высоких концентрациях, без рассеивающего воздействия ветра, он может собираться в защищенных/карманных местах ниже среднего уровня земли. уровне, в результате чего находящиеся там животные удушаются. Привлеченных к трупам падальщиков затем также убивают. Дети погибли таким же образом недалеко от города Гома в результате выбросов CO 2 из близлежащего вулкана Ньирагонго . [48] На языке суахили это явление называется мазуку .

У человека происходит адаптация к повышенным концентрациям CO 2 , включая изменение дыхания и выработку бикарбоната почками, чтобы сбалансировать эффекты закисления крови ( ацидоза ). Некоторые исследования показали, что 2,0-процентные вдыхаемые концентрации можно использовать для закрытых воздушных пространств (например, подводной лодки ), поскольку адаптация является физиологической и обратимой, поскольку ухудшение работоспособности или нормальной физической активности не происходит при таком уровне воздействия в течение пяти дней. [49] [50] Тем не менее, другие исследования показывают снижение когнитивных функций даже на гораздо более низких уровнях. [51] [52] Кроме того, при продолжающемся респираторном ацидозе адаптационные или компенсаторные механизмы не смогут обратить вспять это состояние.
Существует мало исследований последствий для здоровья длительного непрерывного воздействия CO 2 на людей и животных при уровнях ниже 1%. В США установлены пределы профессионального воздействия CO 2 на уровне 0,5% (5000 частей на миллион) в течение восьмичасового периода. [53] При такой концентрации CO 2 экипаж Международной космической станции испытывал головные боли, вялость, умственную медлительность, эмоциональное раздражение и нарушение сна. [54] Исследования на животных при концентрации CO 2 0,5% продемонстрировали кальцификацию почек и потерю костной массы после восьми недель воздействия. [55] Исследование людей, подвергавшихся воздействию в течение 2,5-часовых сеансов, продемонстрировало значительное негативное воздействие на когнитивные способности даже при таких низких концентрациях, как 0,1% (1000 ppm) CO 2 , вероятно, из-за вызванного CO 2 увеличения мозгового кровотока. [51] В другом исследовании наблюдалось снижение уровня базовой активности и использования информации при 1000 ppm по сравнению с 500 ppm. [52]
Однако обзор литературы показал, что надежная группа исследований феномена, вызывающего когнитивные нарушения углекислого газа, показывает лишь небольшое влияние на принятие решений на высоком уровне (для концентраций ниже 5000 частей на миллион). Большинство исследований были затруднены из-за неадекватного дизайна исследований, комфорта окружающей среды, неопределенности в дозах воздействия и различных используемых когнитивных оценок. [56] Аналогичным образом, исследование влияния концентрации CO 2 в мотоциклетных шлемах подверглось критике за сомнительную методологию, в которой не принимались во внимание самоотчеты мотоциклистов и проводились измерения с использованием манекенов. Кроме того, когда были достигнуты нормальные условия для мотоцикла (например, скорость на шоссе или в городе) или был поднят козырек, концентрация CO 2 снижалась до безопасного уровня (0,2%). [57] [58]

Плохая вентиляция является одной из основных причин чрезмерной концентрации CO 2 в закрытых помещениях, что приводит к ухудшению качества воздуха в помещениях . Дифференциал углекислого газа выше концентраций наружного воздуха в установившихся условиях (когда работа системы вентиляции достаточно продолжительна и концентрация CO 2 стабилизировалась) иногда используется для оценки интенсивности вентиляции на человека. [ нужна цитация ] Более высокие концентрации CO 2 связаны со здоровьем пассажиров, комфортом и ухудшением производительности. [62] [63] Скорость вентиляции по стандарту ASHRAE 62.1–2007 может привести к концентрации в помещении до 2100 частей на миллион выше, чем окружающие условия на открытом воздухе. Таким образом, если концентрация на открытом воздухе составляет 400 частей на миллион, концентрация в помещении может достигать 2500 частей на миллион при скорости вентиляции, соответствующей этому отраслевому консенсусному стандарту. Концентрации в плохо вентилируемых помещениях могут быть еще выше (диапазон 3000 или 4000 частей на миллион).
Шахтеры, которые особенно уязвимы к воздействию газа из-за недостаточной вентиляции, называют смеси углекислого газа и азота « черной сыростью », «удушающей сыростью» или «удушающей сыростью». До того, как были разработаны более эффективные технологии, шахтеры часто проверяли опасные уровни черной сырости и других газов в шахтах, принося с собой во время работы канарейку в клетке. Канарейка более чувствительна к удушливым газам, чем человек, и, теряя сознание, переставала петь и падала со своего насеста. Лампа Дэви также может обнаруживать высокие уровни черной влаги (которая опускается и собирается у пола), горя менее ярко, в то время как метан , еще один удушающий газ и риск взрыва, заставит лампу гореть более ярко.
В феврале 2020 года три человека умерли от удушья на вечеринке в Москве, когда в бассейн для охлаждения добавили сухой лед (замороженный CO2) . [64] Аналогичная авария произошла в 2018 году, когда женщина умерла от паров CO 2 , исходящих от большого количества сухого льда, который она перевозила в своей машине. [65]
Люди проводят все больше и больше времени в замкнутой атмосфере (около 80–90% времени в здании или транспортном средстве). По данным Французского агентства по продовольствию, окружающей среде, охране труда и технике безопасности (ANSES) и различных субъектов во Франции, уровень CO 2 в воздухе помещений зданий (связанный с пребыванием людей или животных и наличием установок для сжигания ), взвешенный по Обновление воздуха «обычно составляет от 350 до 2500 частей на миллион». [66]
В домах, школах, детских садах и офисах не существует систематической взаимосвязи между уровнями CO 2 и других загрязняющих веществ, а CO 2 в помещении статистически не является надежным показателем загрязнения, связанного с уличным дорожным (или воздушным и т. д.) движением. [67] CO 2 — параметр, который меняется быстрее всего (с гигрометрией и уровнем кислорода, когда люди или животные собираются в закрытом или плохо вентилируемом помещении). В бедных странах многие открытые очаги являются источниками CO 2 и выбросов CO непосредственно в жилую среду. [68]
Локальные концентрации углекислого газа могут достигать высоких значений вблизи сильных источников, особенно тех, которые изолированы окружающей местностью. В горячем источнике Боссолето недалеко от Раполано-Терме в Тоскане , Италия, расположенном в чашеобразной впадине диаметром около 100 м (330 футов), концентрация CO 2 за ночь поднимается выше 75%, что достаточно для уничтожения насекомых и мелких животных. После восхода солнца газ рассеивается за счет конвекции. [69] Высокие концентрации CO 2 , образующиеся в результате возмущения глубоководных вод озера, насыщенных CO 2 , как полагают, стали причиной 37 смертельных случаев на озере Монун , Камерун , в 1984 году и 1700 жертв на озере Ньос , Камерун, в 1986 году . [70]
Организм производит примерно 2,3 фунта (1,0 кг) углекислого газа в день на человека, [72] содержащего 0,63 фунта (290 г) углерода.У людей этот углекислый газ переносится через венозную систему и выдыхается через легкие, что приводит к снижению его концентрации в артериях . Содержание углекислого газа в крови часто выражается как парциальное давление , то есть давление, которое имел бы углекислый газ, если бы он один занимал этот объем. [73] Содержание углекислого газа в крови человека показано в соседней таблице.
CO 2 переносится кровью тремя различными путями. (Точные проценты варьируются в зависимости от артериальной и венозной крови).
Гемоглобин , основная молекула, переносящая кислород в эритроцитах , переносит как кислород, так и углекислый газ. Однако CO 2 , связанный с гемоглобином, не связывается с тем же сайтом, что и кислород. Вместо этого он соединяется с N-концевыми группами четырех цепей глобина. Однако из-за аллостерического воздействия на молекулу гемоглобина связывание CO 2 уменьшает количество связанного кислорода при данном парциальном давлении кислорода. Это известно как эффект Холдейна и играет важную роль в транспортировке углекислого газа из тканей в легкие. И наоборот, повышение парциального давления CO 2 или снижение pH вызовет выгрузку кислорода из гемоглобина, что известно как эффект Бора .
Углекислый газ является одним из медиаторов местной ауторегуляции кровоснабжения. Если его концентрация высока, капилляры расширяются, обеспечивая больший приток крови к этой ткани. [75]
Ионы бикарбоната имеют решающее значение для регулирования pH крови. Частота дыхания человека влияет на уровень CO 2 в крови. Слишком медленное или поверхностное дыхание вызывает респираторный ацидоз , а слишком быстрое дыхание приводит к гипервентиляции , которая может вызвать респираторный алкалоз . [76]
Хотя организму необходим кислород для метаболизма, низкий уровень кислорода обычно не стимулирует дыхание. Скорее, дыхание стимулируется более высоким уровнем углекислого газа. В результате вдыхание воздуха низкого давления или газовой смеси, вообще не содержащей кислорода (например, чистого азота), может привести к потере сознания, даже не испытывая недостатка воздуха . Особенно опасно это для летчиков-высотников-истребителей. Именно поэтому бортпроводники советуют пассажирам в случае потери давления в салоне сначала надеть кислородную маску на себя, прежде чем помогать другим; в противном случае человек рискует потерять сознание. [74]
Дыхательные центры стараются поддерживать артериальное давление СО 2 на уровне 40 мм рт. ст . При преднамеренной гипервентиляции содержание СО 2 в артериальной крови может быть снижено до 10–20 мм рт. ст. (содержание кислорода в крови изменяется незначительно), а двигательный импульс снижается. Вот почему после гипервентиляции можно задерживать дыхание дольше, чем без гипервентиляции. Это сопряжено с риском потери сознания до того, как потребность в дыхании станет непреодолимой, поэтому гипервентиляция особенно опасна перед фридайвингом. [77]

В атмосфере Земли углекислый газ является примесью газа , который играет неотъемлемую роль в парниковом эффекте , углеродном цикле , фотосинтезе и океаническом углеродном цикле . Это один из нескольких парниковых газов в атмосфере Земли. Текущая глобальная средняя концентрация CO 2 в атмосфере по состоянию на май 2022 года составляет 421 ppm (0,04%). [80] Это увеличение на 50% с начала промышленной революции по сравнению с 280 ppm в течение 10 000 лет до середины 18 века. [81] [80] [82] Увеличение связано с деятельностью человека . [83] Сжигание ископаемого топлива является основной причиной увеличения концентрации CO 2 , а также основной причиной изменения климата. [84] Другие крупные антропогенные источники включают производство цемента , вырубку лесов и сжигание биомассы .
Несмотря на то , что углекислый газ прозрачен для видимого света , он является парниковым газом, поглощающим и излучающим инфракрасное излучение на двух своих инфракрасно-активных колебательных частотах. CO 2 поглощает и излучает инфракрасное излучение с длинами волн 4,26 мкм (2,347 см -1 ) (асимметричный режим валентных колебаний ) и 14,99 мкм (667 см -1 ) (мода изгибных колебаний). Он играет значительную роль в влиянии на температуру поверхности Земли посредством парникового эффекта. [85] Световое излучение с поверхности Земли наиболее интенсивно в инфракрасной области между 200 и 2500 см -1 , [86] в отличие от светового излучения от гораздо более горячего Солнца, которое наиболее интенсивно в видимой области. Поглощение инфракрасного света на частотах колебаний атмосферного CO 2 удерживает энергию у поверхности, нагревая поверхность и нижние слои атмосферы. Меньше энергии достигает верхних слоев атмосферы, которые, следовательно, более холодные из-за этого поглощения. [87]
Увеличение концентрации в атмосфере CO 2 и других долгоживущих парниковых газов, таких как метан , закись азота и озон , увеличивает поглощение и излучение инфракрасного излучения атмосферой, вызывая наблюдаемое повышение средней глобальной температуры и закисление океана . Другим прямым эффектом является эффект внесения CO 2 . Эти изменения вызывают целый ряд косвенных последствий изменения климата для физической среды, экосистем и человеческого общества. Углекислый газ оказывает большее общее влияние на потепление, чем все остальные парниковые газы вместе взятые. [82] Его время жизни в атмосфере увеличивается с совокупным количеством извлеченного и сожженного ископаемого углерода из-за дисбаланса, который эта деятельность наложила на быстрый углеродный цикл Земли . [88] Это означает, что некоторая часть (по прогнозам 20–35%) ископаемого углерода, перенесенного до сих пор, будет сохраняться в атмосфере в виде повышенного уровня CO 2 в течение многих тысяч лет после того, как деятельность по переносу углерода начнет спадать. [89] [90] [91] Углеродный цикл — это биогеохимический цикл, в котором происходит обмен углеродом между океанами Земли , почвой, горными породами и биосферой . Растения и другие фотоавтотрофы используют солнечную энергию для производства углеводов из атмосферного углекислого газа и воды путем фотосинтеза . Почти все другие организмы зависят от углеводов, полученных в результате фотосинтеза, в качестве основного источника энергии и соединений углерода.
Современная концентрация CO 2 в атмосфере является самой высокой за 14 миллионов лет. [92] Концентрация CO 2 в атмосфере достигала 4000 частей на миллион в кембрийский период около 500 миллионов лет назад и всего лишь 180 частей на миллион во время четвертичного оледенения последних двух миллионов лет. [81] Реконструированные температурные записи за последние 420 миллионов лет показывают, что концентрации CO 2 в атмосфере достигли пика примерно на уровне 2000 ppm в девонский период (400 миллионов лет), а затем в триасовый период (220–200 миллионов лет) и в четыре раза превышали современные уровни в юрский период (201–145 миллионов лет). [93] [94]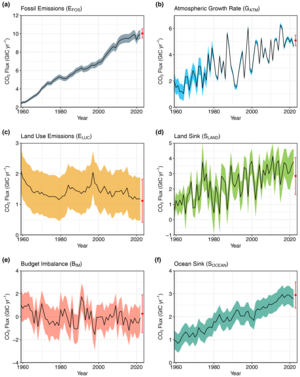
Углекислый газ растворяется в океане с образованием угольной кислоты ( H 2 CO 3 ), бикарбоната ( HCO−3) и карбонат ( CO2-3). В океанах растворено примерно в пятьдесят раз больше углекислого газа, чем в атмосфере. Океаны действуют как огромный поглотитель углерода и поглощают около трети CO 2 , выбрасываемого в результате деятельности человека. [96]
Закисление океана — это продолжающееся снижение pH земного океана . В период с 1950 по 2020 год средний pH поверхности океана упал примерно с 8,15 до 8,05. [97] Выбросы углекислого газа в результате деятельности человека являются основной причиной закисления океана: уровень углекислого газа (CO 2 ) в атмосфере превышает 410 частей на миллион (в 2020 году). CO 2 из атмосферы поглощается океанами. При этом образуется угольная кислота ( H2CO3 ), которая диссоциирует на ион бикарбоната ( HCO ) .−3) и ион водорода ( H + ). Наличие свободных ионов водорода ( H + ) снижает pH океана, повышая кислотность (это не значит, что морская вода еще кислая; она все еще щелочная , с pH выше 8). Морские кальцифицирующие организмы , такие как моллюски и кораллы , особенно уязвимы, поскольку они полагаются на карбонат кальция для построения раковин и скелетов. [98]
Изменение pH на 0,1 представляет собой увеличение концентрации ионов водорода в Мировом океане на 26% (шкала pH логарифмическая, поэтому изменение на единицу в единицах pH эквивалентно десятикратному изменению концентрации ионов водорода). Уровень pH морской поверхности и насыщенность карбонатами варьируются в зависимости от глубины и местоположения океана. Воды более холодных и более высоких широт способны поглощать больше CO 2 . Это может привести к повышению кислотности, снижению pH и уровня насыщения карбонатами в этих областях. Другие факторы, которые влияют на обмен CO 2 между атмосферой и океаном и, следовательно, на местное закисление океана, включают: океанские течения и зоны апвеллинга , близость к крупным континентальным рекам, покрытие морским льдом и обмен атмосферы азотом и серой в результате сжигания ископаемого топлива и сельского хозяйства . [99] [100] [101]
Изменения в химии океана могут иметь обширные прямые и косвенные последствия для организмов и их среды обитания. Одно из наиболее важных последствий повышения кислотности океана связано с образованием раковин из карбоната кальция ( CaCO 3 ). [98] Этот процесс называется кальцификацией и важен для биологии и выживания широкого спектра морских организмов. Кальцификация включает осаждение растворенных ионов в твердые структуры CaCO 3 , структуры для многих морских организмов, таких как кокколитофоры , фораминиферы , ракообразные , моллюски и т. д. После того, как они сформированы, эти структуры CaCO 3 уязвимы для растворения , если окружающая морская вода не содержит насыщающие концентрации карбонат-ионов ( CO2-3).
Очень небольшая часть дополнительного углекислого газа, добавляемого в океан, остается в виде растворенного углекислого газа. Большая часть диссоциирует на дополнительные ионы бикарбоната и свободных ионов водорода. Увеличение водорода больше, чем увеличение бикарбоната, [102] создавая дисбаланс реакции:
Чтобы поддерживать химическое равновесие, некоторые ионы карбоната, уже находящиеся в океане, соединяются с некоторыми ионами водорода, образуя новый бикарбонат. Таким образом, концентрация карбонат-ионов в океане снижается, удаляя важный строительный блок для морских организмов, позволяющий строить раковины или кальцинировать:
Углекислый газ также попадает в океаны через гидротермальные жерла. Гидротермальное жерло Шампани , обнаруженное на северо-западе вулкана Эйфуку в Марианской впадине , производит почти чистый жидкий углекислый газ. Это одно из двух известных мест в мире по состоянию на 2004 год, другое находится в Окинавском желобе . [103] Об обнаружении подводного озера жидкого углекислого газа в Окинавском желобе сообщалось в 2006 году. [104]
Углекислый газ является побочным продуктом ферментации сахара при пивоварении , виски и других алкогольных напитках , а также при производстве биоэтанола . Дрожжи метаболизируют сахар с образованием CO 2 и этанола , также известного как спирт, следующим образом:
Все аэробные организмы производят CO 2 при окислении углеводов , жирных кислот и белков . Большое количество задействованных реакций чрезвычайно сложны и их нелегко описать. См. ( клеточное дыхание , анаэробное дыхание и фотосинтез ). Уравнение дыхания глюкозы и других моносахаридов :
Анаэробные организмы разлагают органический материал, образуя метан и углекислый газ вместе со следами других соединений. [105] Независимо от типа органического материала, образование газов следует четко определенной кинетической схеме . Углекислый газ составляет около 40–45% газа, образующегося при разложении на свалках (так называемый « свалочный газ »). Большую часть оставшихся 50–55% составляет метан. [106]
Углекислый газ можно получить перегонкой из воздуха, но метод малоэффективен. В промышленности диоксид углерода представляет собой преимущественно непереработанный отход, производимый несколькими методами, которые можно применять на практике в различных масштабах. [107]
При сжигании всех видов топлива на основе углерода , таких как метан ( природный газ ), нефтяные дистилляты ( бензин , дизельное топливо , керосин , пропан ), уголь, древесина и обычные органические вещества, образуется углекислый газ и, за исключением чистого углерода, вода. . Например, химическая реакция между метаном и кислородом :
Железо восстанавливают из его оксидов коксом в доменной печи с получением чугуна и углекислого газа: [108]
Углекислый газ является побочным продуктом промышленного производства водорода путем паровой конверсии и реакции конверсии водяного газа при производстве аммиака . Эти процессы начинаются с реакции воды и природного газа (в основном метана). [109] Это основной источник пищевого диоксида углерода, который используется при газировании пива и безалкогольных напитков , а также используется для оглушения животных, таких как домашняя птица . Летом 2018 года в Европе возник дефицит углекислого газа для этих целей из-за временной остановки на техническое обслуживание нескольких заводов по производству аммиака. [110]
Его получают путем термического разложения известняка CaCO 3 путем нагревания ( прокаливания ) при температуре около 850 °C (1560 °F) при производстве негашеной извести ( оксид кальция , CaO), соединения, которое имеет множество промышленных применений:
Кислоты высвобождают CO 2 из большинства карбонатов металлов. Следовательно, его можно получить непосредственно из природных источников углекислого газа , где он образуется путем воздействия подкисленной воды на известняк или доломит . Реакция между соляной кислотой и карбонатом кальция (известняком или мелом) показана ниже:
Угольная кислота ( H 2 CO 3 ) затем разлагается на воду и CO 2 :
Такие реакции сопровождаются вспениванием или пузырьками, или тем и другим, по мере выделения газа. Они широко используются в промышленности, поскольку их можно использовать для нейтрализации потоков отработанной кислоты.
Углекислый газ используется в пищевой, нефтяной и химической промышленности. [107] Это соединение имеет разнообразное коммерческое применение, но одно из наиболее важных его применений в качестве химического вещества — производство газированных напитков; он придает блеск газированным напиткам, таким как газированная вода, пиво и игристое вино.
В химической промышленности углекислый газ в основном используется в качестве ингредиента при производстве карбамида , меньшая часть используется для производства метанола и ряда других продуктов. [111] Некоторые производные карбоновых кислот, такие как салицилат натрия, получают с использованием CO 2 по реакции Кольбе-Шмитта . [112]
Помимо традиционных процессов использования CO 2 в химическом производстве, на исследовательском уровне исследуются также электрохимические методы. В частности, использование возобновляемых источников энергии для производства топлива из CO 2 (например, метанола) является привлекательным, поскольку это может привести к получению топлива, которое можно было бы легко транспортировать и использовать в рамках традиционных технологий сжигания, но при этом не иметь чистых выбросов CO 2 . [113]
Растениям необходим углекислый газ для проведения фотосинтеза. Атмосфера теплиц может (если они большие по размеру, должна) быть обогащена дополнительным CO 2 для поддержания и увеличения скорости роста растений. [114] [115] При очень высоких концентрациях (в 100 раз превышающих атмосферную концентрацию или выше) углекислый газ может быть токсичным для животных, поэтому повышение концентрации до 10 000 частей на миллион (1%) или выше на несколько часов уничтожит таких вредителей, как белокрылка и паутинный клещ в теплице. [116]

Углекислый газ — пищевая добавка , используемая в пищевой промышленности в качестве вытеснителя и регулятора кислотности. Он одобрен для использования в ЕС [117] ( номер E290), США [118] , Австралии и Новой Зеландии [119] ( номер INS 290).
Конфета под названием Pop Rocks находится под давлением углекислого газа [120] под давлением около 4000 кПа (40 бар ; 580 фунтов на квадратный дюйм ). При попадании в рот он растворяется (как и другие леденцы) и выпускает пузырьки газа со слышимым хлопком.
Разрыхлители заставляют тесто подниматься, выделяя углекислый газ. [121] Пекарские дрожжи производят углекислый газ в результате ферментации сахаров в тесте, в то время как химические закваски, такие как разрыхлитель и пищевая сода, выделяют углекислый газ при нагревании или воздействии кислот .
Углекислый газ используется для производства газированных безалкогольных напитков и газированной воды . Традиционно газирование пива и игристого вина осуществлялось путем естественного брожения, но многие производители газируют эти напитки углекислым газом, извлеченным в процессе брожения. В случае пива в бутылках и бочонках наиболее распространенным методом является карбонизация переработанным диоксидом углерода. За исключением британского настоящего эля , разливное пиво обычно переносят из бочонков в холодном помещении или подвале в разливные краны на баре с использованием углекислого газа под давлением, иногда смешанного с азотом.
Вкус газированной воды (и связанные с ней вкусовые ощущения от других газированных напитков) — это результат растворенного углекислого газа, а не лопающихся пузырьков газа. Карбоангидраза 4 превращается в угольную кислоту , что приводит к кислому вкусу, а растворенный углекислый газ вызывает соматосенсорную реакцию. [122]

Углекислый газ в форме сухого льда часто используется на этапе холодного вымачивания в виноделии для быстрого охлаждения гроздей винограда после сбора и предотвращения самопроизвольного брожения дикими дрожжами . Основное преимущество использования сухого льда перед водяным льдом заключается в том, что он охлаждает виноград без добавления дополнительной воды, которая могла бы снизить концентрацию сахара в виноградном сусле и, следовательно, концентрацию алкоголя в готовом вине. Углекислый газ также используется для создания гипоксической среды для углекислой мацерации — процесса, используемого при производстве вина Божоле .
Углекислый газ иногда используется для пополнения винных бутылок или других емкостей для хранения, таких как бочки, чтобы предотвратить окисление, но проблема заключается в том, что он может растворяться в вине, делая ранее неподвижное вино слегка шипучим. По этой причине профессиональные виноделы предпочитают для этого процесса другие газы, такие как азот или аргон .
Углекислый газ часто используют для «оглушения» животных перед убоем. [123] Термин «ошеломляющий» может быть неправильным, поскольку животные не теряют сознание сразу и могут страдать от дистресса. [124] [125]
Углекислый газ является одним из наиболее часто используемых сжатых газов в пневматических (газовых) системах портативных инструментов, работающих под давлением. Углекислый газ также используется в качестве атмосферы при сварке , хотя в сварочной дуге он вступает в реакцию с окислением большинства металлов. Использование в автомобильной промышленности широко распространено, несмотря на убедительные доказательства того, что сварные швы, выполненные в углекислом газе, более хрупкие , чем сварные швы, выполненные в более инертной атмосфере. [ нужна ссылка ] При сварке MIG использование CO 2 иногда называют сваркой MAG, для металлического активного газа, поскольку CO 2 может реагировать при таких высоких температурах. Он имеет тенденцию создавать более горячую лужу, чем действительно инертная атмосфера, улучшая характеристики потока. Хотя, возможно, это связано с атмосферными реакциями, происходящими на месте лужи. Обычно это противоположно желаемому эффекту при сварке, поскольку имеет тенденцию к охрупчиванию места сварки, но может не быть проблемой для обычной сварки мягкой стали, где предельная пластичность не является серьезной проблемой.
Углекислый газ используется во многих потребительских товарах, для которых требуется газ под давлением, потому что он недорогой и негорючий, а также потому, что он претерпевает фазовый переход из газа в жидкость при комнатной температуре и достижимом давлении примерно 60 бар (870 фунтов на квадратный дюйм ; 59 атм ), что позволяет в данном контейнере помещается гораздо больше углекислого газа, чем в противном случае. Спасательные жилеты часто содержат баллоны с углекислым газом под давлением для быстрого надувания. Алюминиевые капсулы с CO 2 также продаются в качестве запаса сжатого газа для пневматического оружия , пейнтбольных маркеров/ружей, накачивания велосипедных шин и для приготовления газированной воды . Высокие концентрации углекислого газа также можно использовать для уничтожения вредителей. Жидкий углекислый газ применяется при сверхкритической сушке некоторых пищевых продуктов и технологических материалов, при подготовке препаратов для сканирующей электронной микроскопии [126] и при декофеинизации кофейных зерен .

Углекислый газ можно использовать для тушения пламени, заполняя газом окружающую среду вокруг пламени. Он сам по себе не реагирует на тушение пламени, а лишает пламя кислорода, вытесняя его. Некоторые огнетушители , особенно предназначенные для пожаров, связанных с электричеством , содержат жидкий углекислый газ под давлением. Углекислотные огнетушители хорошо работают при небольших возгораниях легковоспламеняющихся жидкостей и электрооборудования, но не при пожарах обычных горючих веществ, поскольку они не охлаждают существенно горящие вещества, а при рассеивании углекислого газа могут загореться при воздействии кислорода воздуха . В основном их используют в серверных комнатах. [127]
Углекислый газ также широко используется в качестве средства пожаротушения в стационарных системах противопожарной защиты для локального применения при определенных опасностях и полного затопления защищаемого помещения. [128] Стандарты Международной морской организации признают углекислотные системы для противопожарной защиты судовых трюмов и машинных отделений. Системы противопожарной защиты на основе углекислого газа были связаны с несколькими смертельными случаями, поскольку в достаточно высоких концентрациях он может вызвать удушье. Обзор систем CO 2 выявил 51 инцидент в период с 1975 года по дату отчета (2000 год), в результате которого 72 человека погибли и 145 получили ранения. [129]
Жидкий углекислый газ является хорошим растворителем многих липофильных органических соединений и используется для удаления кофеина из кофе . [18] Углекислый газ привлек внимание в фармацевтической и других химических отраслях промышленности как менее токсичная альтернатива более традиционным растворителям, таким как хлорорганические соединения . По этой причине его также используют некоторые химчистки . Его используют при приготовлении некоторых аэрогелей из-за свойств сверхкритического диоксида углерода.
В медицине к кислороду добавляют до 5% углекислого газа (концентрация в 130 раз больше атмосферного) для стимуляции дыхания после апноэ и для стабилизации баланса О 2 /СО 2 в крови.
Углекислый газ может смешиваться с 50% кислорода, образуя вдыхаемый газ; он известен как карбоген и имеет множество медицинских и исследовательских целей.
Другое медицинское применение — мофетте , сухие курорты, в которых в терапевтических целях используется углекислый газ из поствулканических выбросов.
Сверхкритический CO 2 используется в качестве рабочего тела в двигателе с силовым циклом Аллама .
Углекислый газ используется при повышении нефтеотдачи , когда его закачивают в добывающие нефтяные скважины или рядом с ними, обычно в сверхкритических условиях, когда он становится смешиваемым с нефтью. Этот подход может увеличить первоначальную нефтеотдачу за счет снижения остаточной нефтенасыщенности на 7–23% в дополнение к первичной добыче . [130] Он действует одновременно как повышающий давление агент и при растворении в подземной сырой нефти значительно снижает ее вязкость и изменяет химический состав поверхности, позволяя нефти быстрее течь через пласт к добывающей скважине. [131] На зрелых нефтяных месторождениях для подачи углекислого газа к точкам закачки используются обширные сети трубопроводов.
При улучшенной добыче метана из угольных пластов углекислый газ будет закачиваться в угольный пласт для вытеснения метана, в отличие от нынешних методов, которые в основном основаны на удалении воды (для снижения давления), чтобы заставить угольный пласт высвободить захваченный метан. [132]
Было предложено подавать CO 2 от выработки электроэнергии в пруды, чтобы стимулировать рост водорослей , которые затем можно было бы превратить в биодизельное топливо. [133] Штамм цианобактерии Synechococcus elongatus был генетически сконструирован для производства топлива изобутиральдегида и изобутанола из CO 2 с помощью фотосинтеза. [134]
Исследователи разработали процесс, называемый электролизом, используя ферменты, выделенные из бактерий, для запуска химических реакций, которые превращают CO 2 в топливо. [135] [136] [137]
Жидкий и твердый диоксид углерода являются важными хладагентами , особенно в пищевой промышленности, где они используются при транспортировке и хранении мороженого и других замороженных продуктов. Твердый диоксид углерода называется «сухим льдом» и используется для небольших грузов, где холодильное оборудование нецелесообразно. Твердый углекислый газ всегда имеет температуру ниже -78,5 ° C (-109,3 ° F) при обычном атмосферном давлении, независимо от температуры воздуха.
Жидкий диоксид углерода (отраслевая номенклатура R744 или R-744) использовался в качестве хладагента до использования [ нужна ссылка ] дихлордифторметана ( R12, соединение хлорфторуглерода (CFC)). CO 2 может переживать возрождение, поскольку один из основных заменителей ХФУ, 1,1,1,2-тетрафторэтан ( R134a , соединение гидрофторуглерода (ГФУ)) способствует изменению климата больше, чем CO 2 . Физические свойства CO 2 очень благоприятны для целей охлаждения, охлаждения и нагрева, поскольку он имеет высокую объемную холодопроизводительность. Из-за необходимости работать при давлении до 130 бар (1900 фунтов на квадратный дюйм; 13 000 кПа) для систем CO 2 требуются высокомеханически стойкие резервуары и компоненты, которые уже разработаны для массового производства во многих секторах. В автомобильных кондиционерах более чем в 90% всех условий движения на широтах выше 50° CO 2 (R744) работает более эффективно, чем системы, использующие ГФУ (например, R134a). Его экологические преимущества ( ПГП , равный 1, не разрушает озоновый слой, нетоксичен, невоспламеняем) могут сделать его будущей рабочей жидкостью для замены нынешних ГФУ в автомобилях, супермаркетах и водонагревателях с тепловыми насосами, среди прочего. Компания Coca-Cola внедрила охладители напитков на основе CO 2 , а армия США заинтересована в технологии охлаждения и отопления с использованием CO 2 . [138] [139]

Углекислый газ является лазерной средой в углекислотном лазере , который является одним из самых ранних типов лазеров.
Углекислый газ можно использовать в качестве средства контроля pH в бассейнах [140] путем постоянного добавления газа в воду, предотвращая тем самым повышение pH. Среди преимуществ этого — отсутствие работы с (более опасными) кислотами. Точно так же он также используется для содержания рифовых аквариумов , где он обычно используется в кальциевых реакторах для временного снижения pH воды, пропускаемой через карбонат кальция , чтобы позволить карбонату кальция более свободно растворяться в воде, где он используется некоторыми кораллами для построения своего скелета.
Используется в качестве основного теплоносителя в британском усовершенствованном реакторе с газовым охлаждением для атомной энергетики.
Индукция углекислым газом обычно используется для эвтаназии лабораторных исследовательских животных. Методы введения CO 2 включают помещение животных непосредственно в закрытую, предварительно заполненную камеру, содержащую CO 2 , или воздействие постепенно увеличивающейся концентрации CO 2 . В рекомендациях Американской ветеринарной медицинской ассоциации от 2020 года по индукции углекислым газом говорится, что скорость перемещения 30–70% объема камеры или клетки в минуту является оптимальной для гуманной эвтаназии мелких грызунов. [141] : 5, 31 Процентное содержание CO 2 варьируется для разных видов, исходя из установленных оптимальных процентных значений для минимизации страданий. [141] : 22
Углекислый газ также используется в некоторых связанных методах очистки и подготовки поверхности .

Углекислый газ был первым газом, который был описан как дискретное вещество. Примерно в 1640 году [142] фламандский химик Ян Баптист ван Гельмонт заметил, что когда он сжигал древесный уголь в закрытом сосуде, масса образующегося пепла была значительно меньше массы исходного древесного угля. Его интерпретация заключалась в том, что остальная часть древесного угля превратилась в невидимую субстанцию, которую он назвал «газом» (от греческого «хаос») или «диким духом» ( Spiritus sylvestris ). [143]
Свойства углекислого газа были дополнительно изучены в 1750-х годах шотландским врачом Джозефом Блэком . Он обнаружил, что известняк ( карбонат кальция ) можно нагревать или обрабатывать кислотами , чтобы получить газ, который он назвал «неподвижным воздухом». Он заметил, что фиксированный воздух был плотнее воздуха и не поддерживал ни пламя, ни животную жизнь. Блэк также обнаружил, что при барботировании известковой воды (насыщенного водного раствора гидроксида кальция ) происходит осаждение карбоната кальция. Он использовал это явление, чтобы проиллюстрировать, что углекислый газ образуется в результате дыхания животных и микробной ферментации. В 1772 году английский химик Джозеф Пристли опубликовал статью под названием « Пропитка воды фиксированным воздухом», в которой он описал процесс капания серной кислоты (или купоросного масла , как его знал Пристли) на мел с целью получения углекислого газа и принудительного вытеснения газа. раствориться путем перемешивания миски с водой, находящейся в контакте с газом. [144]
Углекислый газ был впервые сжижен (при повышенном давлении) в 1823 году Хамфри Дэви и Майклом Фарадеем . [145] Самое раннее описание твердого углекислого газа ( сухого льда ) было дано французским изобретателем Адриеном-Жаном-Пьером Тилорье , который в 1835 году открыл герметичный контейнер с жидким углекислым газом и обнаружил, что охлаждение происходит за счет быстрого испарения. жидкости образовался «снег» твердого CO 2 . [146] [147]
Углекислый газ в сочетании с азотом издревле был известен как Blackdamp , каменная или дроссельная влага. [148] Наряду с другими типами влаги он встречался при добыче полезных ископаемых и проходке скважин. Медленное окисление угля и биологические процессы заменили кислород, создав удушающую смесь азота и углекислого газа. [149]
(Рубиско) — наиболее распространенный фермент на этой планете, на его долю приходится 30–50% общего растворимого белка в хлоропластах.
{{cite report}}: CS1 maint: неподходящий URL ( ссылка ){{cite report}}: CS1 maint: неподходящий URL ( ссылка )Жертвы были связаны с влиятельной личностью в Instagram Екатериной Диденко.
Рисунок 1f
{{cite book}}: |website=игнорируется ( помощь )