Деметилирование – это химический процесс, приводящий к удалению метильной группы (СН 3 ) из молекулы. [1] [2] Распространенным способом деметилирования является замена метильной группы атомом водорода, что приводит к чистой потере одного атома углерода и двух атомов водорода.
Аналогом деметилирования является метилирование .
В биохимических системах процесс деметилирования катализируется деметилазами . Эти ферменты окисляют N-метильные группы, которые встречаются в гистонах и некоторых формах ДНК:
Одним из таких семейств окислительных ферментов является цитохром P450 . [3] Альфа-кетоглутарат-зависимые гидроксилазы активны в деметилировании ДНК, действуя по аналогичному пути. В этих реакциях используется слабая связь CH , примыкающая к аминам .
.jpg/440px-Conversion_of_5-methylcytosine_to_5-hydroxymetnylcytosine_by_TET_enzyme_plus_alpha-ketoglutarate_&_Fe(II).jpg)
В частности, 5-метилцитозины в ДНК могут быть деметилированы ферментами ТЕТ , как показано на рисунке. Ферменты ТЕТ представляют собой диоксигеназы из семейства альфа-кетоглутарат-зависимых гидроксилаз . Фермент ТЕТ представляет собой альфа-кетоглутарат (α-KG)-зависимую диоксигеназу, которая катализирует реакцию окисления путем включения одного атома кислорода из молекулярного кислорода (O 2 ) в его субстрат , 5-метилцитозин в ДНК (5mC), с образованием продукта. 5-гидроксиметилцитозин в ДНК. Это преобразование сопровождается окислением ко -субстрата α-KG до сукцината и диоксида углерода (см. Рисунок).
Первый этап включает связывание α-KG и 5-метилцитозина с активным центром фермента ТЕТ . Каждый из ферментов ТЕТ содержит основной каталитический домен с двухцепочечной укладкой β-спирали, которая содержит важные металлсвязывающие остатки, обнаруженные в семействе Fe(II)/α-KG-зависимых оксигеназ . [4] α-KG координируется как бидентатный лиганд (соединенный в двух точках) с Fe(II) (см. рисунок), тогда как 5mC удерживается нековалентной силой в непосредственной близости. Активный центр ТЕТ содержит высококонсервативный триадный мотив, в котором каталитически необходимый Fe(II) удерживается двумя остатками гистидина и одним остатком аспарагиновой кислоты (см. рисунок). Триада связывается с одной стороной Fe-центра, оставляя три лабильных сайта, доступных для связывания α-KG и O 2 (см. рисунок). Затем ТЕТ преобразует 5-метилцитозин в 5-гидроксиметилцитозин, а α-кетоглутарат превращается в сукцинат и CO 2 .
Деметилирование некоторых стеринов является этапом биосинтеза тестостерона и холестерина . Метильные группы теряются в виде формиата . [5] Во время эмбриогенеза у мышей около 20 миллионов 5-метилцитозинов деметилируются в течение шести часов сразу после оплодотворения яйцеклетки сперматозоидом с образованием зиготы. [ нужна цитата ]
Деметилирование часто относится к расщеплению простых эфиров , особенно ариловых эфиров, хотя есть и некоторые исключения, такие как N -деметилирование аминов (например, имипрамин до дезипрамина ).
Арилметиловые эфиры широко распространены в лигнине и многих производных соединениях. [6] Деметилирование этих материалов было предметом больших усилий. Реакция обычно требует суровых условий или агрессивных реагентов. Например, метиловый эфир ванилина можно удалить нагреванием сильного основания при температуре около 250 °C (482 °F). [7] Более сильные нуклеофилы , такие как диорганофосфиды (LiPPh 2 ), также расщепляют ариловые эфиры в более мягких условиях. [8] Другие сильные нуклеофилы, которые использовались, включают тиолатные соли, такие как EtSNa. [9]
Также можно использовать кислые условия. Исторически арилметиловые эфиры, включая природные продукты, такие как кодеин ( O -метилморфин), деметилировались путем нагревания вещества в расплавленном гидрохлориде пиридина (температура плавления 144 °C (291 °F)) при температуре от 180 до 220 °C (от 356 до 356 °F). 428 °F), иногда с избытком хлористого водорода , в процессе, известном как расщепление эфира Цейзеля-Прея . [10] [11] Количественный анализ ароматических метиловых эфиров может быть выполнен аргентометрическим определением образующегося хлорида N -метилпиридиния . [12] Механизм этой реакции начинается с переноса протона от иона пиридиния к арилметиловому эфиру, крайне неблагоприятной стадии ( K < 10 -11 ), которая объясняет необходимость суровых условий, учитывая гораздо более слабую кислотность пиридиния ( p K а = 5,2) по сравнению с протонированным арилметиловым эфиром (ион арилметилоксония, p K a = –6,7 для арил = Ph [13] ). За этим следует S N 2 атака иона арилметилоксония по метильной группе ионом пиридина или хлорида (в зависимости от субстрата) с образованием свободного фенола и, в конечном итоге, хлорида N -метилпиридиния либо непосредственно, либо путем последующего переноса метила от метилхлорид в пиридин. [12]

Другой классический (но, опять же, жесткий) метод удаления метильной группы арилметилового эфира — нагревание эфира до кипения с обратным холодильником в растворе бромистого водорода или йодистого водорода в уксусной кислоте (температура кипения 118 °С (244 °С). F)) или концентрированную бромистоводородную или иодистоводородную кислоту . [14] Расщепление эфиров бромистоводородной или иодистоводородной кислотой происходит по очень похожему механизму, при котором высококислотные HBr или HI служат для протонирования эфира с последующим замещением бромидом или йодидом , которые оба являются отличными нуклеофилами. В несколько более мягких условиях используется циклогексилиодид (CyI, 10,0 экв.) в N , N -диметилформамиде для образования небольшого количества йодистого водорода in situ . [15]
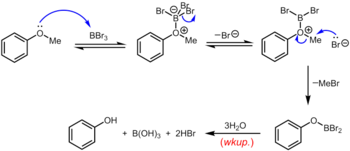
Трибромид бора , который можно использовать при комнатной температуре или ниже, является более специализированным реагентом для деметилирования арилметиловых эфиров. Механизм деалкилирования эфира протекает через начальное обратимое образование кислотно-основного аддукта Льюиса между сильнокислотным Льюисом BBr 3 и основным эфиром Льюиса. Этот аддукт Льюиса может обратимо диссоциировать с образованием катиона дибромборил оксония и Br – . Разрыв эфирной связи происходит в результате последующей нуклеофильной атаки Br на оксониевые соединения с образованием арилоксидибромборана и бромистого метила. По завершении реакции фенол высвобождается вместе с борной кислотой (H 3 BO 3 ) и бромистоводородной кислотой (водн. HBr) при гидролизе производного дибромборана при водной обработке . [16]
Ароматические метиловые эфиры, особенно с соседней карбонильной группой, можно региоселективно деметилировать с использованием эфирата йодида магния . [17] Примером этого является синтез природного продукта Кальфостина А , [18] , как показано ниже.

Метиловые эфиры также подвержены деметилированию, которое обычно достигается путем омыления . Широко распространены узкоспециализированные деметилирования, такие как декарбоксилирование Крапчо :
Смесь анетола , КОН и спирта нагревали в автоклаве. Хотя продуктом этой реакции был ожидаемый анол , Чарльз Доддс также обнаружил в маточных растворах высокореактивный продукт димеризации, называемый дианолом .
N -деметилирование 3°-аминов осуществляется по реакции фон Брауна , в которой в качестве реагента используется BrCN с образованием соответствующих нор- производных. Был разработан современный вариант реакции фон Брауна, в котором BrCN был заменен этилхлорформиатом . Применением этой реакции является получение Паксила из ареколина , как и синтез GSK-372,475 , например.
{{cite book}}: CS1 maint: отсутствует местоположение издателя ( ссылка )