
Онковирус или онкогенный вирус — это вирус, который может вызвать рак . [4] Этот термин возник в результате исследований остро трансформирующих ретровирусов в 1950–60-х годах, [5] когда термин «онкорнавирусы» использовался для обозначения их РНК- вирусного происхождения. [6] После удаления букв «РНК» оно теперь относится к любому вирусу с геномом ДНК или РНК, вызывающему рак, и является синонимом « вируса опухоли » или «вируса рака». Подавляющее большинство вирусов человека и животных не вызывают рак, вероятно, из-за длительной совместной эволюции вируса и его хозяина. Онковирусы сыграли важную роль не только в эпидемиологии , но и в исследованиях механизмов контроля клеточного цикла , таких как белок ретинобластомы .
По оценкам Международного агентства по исследованию рака Всемирной организации здравоохранения , в 2002 году инфекция стала причиной 17,8% случаев рака у человека, причем 11,9% были вызваны одним из семи вирусов. [7] Исследование 2658 образцов 38 различных типов рака, проведенное в 2020 году, показало, что 16% из них были связаны с вирусом. [8] Эти виды рака можно легко предотвратить с помощью вакцинации (например, вакцины против папилломавируса ), диагностики с помощью простых анализов крови и лечения менее токсичными противовирусными препаратами.
Как правило, опухолевые вирусы практически не вызывают заболеваний после заражения у своих хозяев или не вызывают никаких неопластических заболеваний, таких как острый гепатит в случае вируса гепатита В или мононуклеоз в случае вируса Эпштейна-Барр . У меньшинства людей (или животных) после заражения развивается рак. Это усложнило попытки определить, вызывает ли данный вирус рак. Известные постулаты Коха — конструкции XIX века, разработанные Робертом Кохом для установления вероятности того, что Bacillus anthracis вызовет заболевание сибирской язвой , неприменимы к вирусным заболеваниям. Во-первых, это связано с тем, что вирусы невозможно действительно выделить в чистой культуре — даже строгие методы изоляции не могут исключить необнаруженные контаминирующие вирусы с аналогичными характеристиками плотности, и вирусы необходимо выращивать на клетках. Во-вторых, для большинства опухолевых вирусов нормой является бессимптомное заражение и носительство вируса, что нарушает третий принцип Коха. Релман и Фредерикс описали трудности применения постулатов Коха к раку, индуцированному вирусами. [9] Наконец, ограничение хозяина для вирусов человека делает неэтичным экспериментальную передачу вируса, подозреваемого в раке. Другие меры, такие как критерии А.Б. Хилла [10] , более актуальны для вирусологии рака, но также имеют некоторые ограничения в определении причинно-следственной связи.
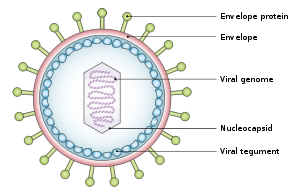
Опухолевые вирусы бывают различных форм: вирусы с ДНК- геномом , такие как аденовирусы , и вирусы с РНК-геномом, такие как вирус гепатита С (ВГС), могут вызывать рак, равно как и ретровирусы, имеющие как ДНК, так и РНК-геномы ( Человеческие вирусы). Т-лимфотропный вирус и вирус гепатита В , который обычно реплицируется как вирус со смешанной двойной и одноцепочечной ДНК, но также имеет ретровирусный компонент репликации). Во многих случаях опухолевые вирусы не вызывают рак у своих нативных хозяев, а только у тупиковых видов. Например, аденовирусы не вызывают рак у людей, а вызывают простуду, конъюнктивит и другие острые заболевания. Они становятся канцерогенными только при заражении определенными видами грызунов, такими как сирийские хомяки. Некоторые вирусы являются онкогенными, когда они заражают клетку и сохраняются в виде кольцевых эписом или плазмид, реплицирующихся отдельно от ДНК клетки-хозяина ( вирус Эпштейна-Барра и герпесвирус, ассоциированный с саркомой Капоши ). Другие вирусы, такие как полиомавирусы и папилломавирусы, являются канцерогенными только тогда, когда они интегрируются в геном клетки-хозяина в результате биологической катастрофы. [ нужна цитата ]

Прямой механизм онкогенного вируса [11] предполагает либо внедрение дополнительных вирусных онкогенных генов в клетку-хозяина, либо усиление уже существующих онкогенных генов ( протоонкогенов ) в геноме. Например, было показано, что vFLIP и vCyclin косвенно вмешиваются в сигнальный путь TGF-β, индуцируя онкогенный кластер mir17-92 хозяина. [12]
Косвенная вирусная онкогенность включает хроническое неспецифическое воспаление, возникающее на протяжении десятилетий после заражения, как в случае рака печени, вызванного ВГС. Эти два механизма различаются по своей биологии и эпидемиологии: вирусы прямой опухоли должны иметь по крайней мере одну копию вируса в каждой опухолевой клетке, экспрессирующую по крайней мере один белок или РНК, вызывающий превращение клетки в раковую. Поскольку в этих опухолях экспрессируются чужеродные вирусные антигены , люди с ослабленным иммунитетом, такие как больные СПИДом или пациенты, перенесшие трансплантацию, подвергаются более высокому риску развития этих типов рака. [ нужна цитата ]
Вирусы хронических непрямых опухолей, с другой стороны, могут быть потеряны (по крайней мере теоретически) из зрелой опухоли, накопившей достаточно мутаций и условий роста (гиперплазии) в результате хронического воспаления вирусной инфекции. В этом последнем случае спорно, но, по крайней мере, теоретически возможно, что вирус непрямой опухоли может подвергнуться «наезду и бегству», и поэтому вирус будет потерян из клинически диагностированной опухоли. С практической точки зрения, это редкое явление, если оно действительно происходит. [ нужна цитата ]

ДНК-онковирусы обычно повреждают два семейства белков-супрессоров опухолей: опухолевые белки p53 и белки ретинобластомы (Rb). Вирусам эволюционно выгодно инактивировать р53, поскольку р53 может вызвать остановку клеточного цикла или апоптоз в инфицированных клетках, когда вирус пытается реплицировать свою ДНК. [13] Точно так же белки Rb регулируют многие важные функции клеток, включая, помимо прочего, решающую контрольную точку клеточного цикла, что делает их мишенью для вирусов, пытающихся нарушить регулярную функцию клеток. [14]
Хотя было обнаружено несколько ДНК-онковирусов, три из них тщательно изучены. Аденовирусы могут вызывать опухоли у грызунов, но не вызывают рак у людей; однако их использовали в качестве средств доставки в генной терапии таких заболеваний, как муковисцидоз и рак. [15] Обезьяний вирус 40 (SV40), полиомавирус , может вызывать опухоли у грызунов, но не является онкогенным для человека. [16] Это явление стало одним из главных противоречий онкогенеза в 20-м веке, поскольку, по оценкам, 100 миллионов человек случайно подверглись воздействию SV40 через вакцины против полиомиелита. [16] Было показано, что вирус папилломы человека-16 (ВПЧ-16) приводит к раку шейки матки и другим видам рака, включая рак головы и шеи . [17] Эти три вируса имеют параллельные механизмы действия, образуя архетип ДНК-онковирусов. Все три ДНК-онковируса способны интегрировать свою ДНК в клетку-хозяина и использовать ее для ее транскрипции и трансформации клеток, минуя контрольную точку G1/S клеточного цикла. [ нужна цитата ]
ДНК-онковирусы трансформируют инфицированные клетки, интегрируя свою ДНК в геном клетки-хозяина. [18] Считается, что ДНК встраивается во время транскрипции или репликации, когда две отожженные цепи разделяются. [18] Это событие относительно редкое и, как правило, непредсказуемое; кажется, не существует детерминированного предсказателя места интеграции. [18] После интеграции клеточный цикл хозяина теряет регуляцию со стороны Rb и p53, и клетка начинает клонировать с образованием опухоли. [19]
Rb и p53 регулируют переход между фазой G1 и S , останавливая клеточный цикл перед репликацией ДНК до тех пор, пока не будут завершены соответствующие входные сигналы контрольных точек, такие как восстановление повреждений ДНК. [20] p53 регулирует ген p21, который продуцирует белок, который связывается с комплексом Cyclin D-Cdk4/6. [21] Это предотвращает фосфорилирование Rb и предотвращает переход клетки в S-фазу. [21] У млекопитающих, когда Rb активен (нефосфорилирован), он ингибирует семейство транскрипционных факторов E2F , регулирующих комплекс Cyclin E - Cdk2 , который ингибирует Rb, образуя петлю положительной обратной связи, удерживая клетку в G1 до момента ввода пересекает порог. [20] Чтобы преждевременно перевести клетку в S-фазу, вирусы должны инактивировать р53, который играет центральную роль в контрольной точке G1/S, а также Rb, который, хотя и находится ниже нее, обычно остается активным за счет положительной обратной связи. петля. [ нужна цитата ]
Вирусы используют различные методы инактивации р53. Белок E1B аденовируса ( 55K) предотвращает регуляцию генов р53 путем связывания с участком р53, который связывается с геномом. [13] Аналогом SV40 является большой Т-антиген (LT); LT также связывается с несколькими другими клеточными белками, такими как p107 и p130 , по тем же остаткам. [22] LT связывается со связывающим доменом p53 на ДНК (а не на белке), снова не позволяя p53 соответствующим образом регулировать гены. [13] Вместо этого ВПЧ разрушает р53: белок Е6 ВПЧ связывается с клеточным белком, называемым белком, ассоциированным с Е6 (E6-AP, также известным как UBE3A ), образуя комплекс, который вызывает быстрое и специфическое убиквитинирование р53. [23]
Rb инактивируется (тем самым обеспечивая беспрепятственное развитие перехода G1/S) различными, но аналогичными вирусными онкобелками. Ранняя область 1А аденовируса ( Е1А) представляет собой онкопротеин, который связывается с Rb и может стимулировать транскрипцию и трансформировать клетки. [13] SV40 использует тот же белок для инактивации Rb, LT, для инактивации p53. [21] ВПЧ содержит белок E7, который может связываться с Rb практически таким же образом. [24] Rb может быть инактивирован путем фосфорилирования или путем связывания с вирусным онкобелком или путем мутаций — мутации, которые предотвращают связывание онкопротеина, также связаны с раком. [22]
ДНК-онковирусы обычно вызывают рак, инактивируя р53 и Rb, тем самым обеспечивая нерегулируемое деление клеток и создавая опухоли. Может существовать множество различных механизмов, которые развивались отдельно; Помимо описанных выше, например, вирус папилломы человека инактивирует р53, изолируя его в цитоплазме. [13]
SV40 хорошо изучен и не вызывает рака у людей, но недавно обнаруженный аналог, называемый полиомавирусом клеток Меркеля , связан с карциномой клеток Меркеля , формой рака кожи. [25] Считается, что особенность связывания Rb у обоих вирусов одинакова. [25]
В 1960-х годах считалось, что процесс репликации РНК-вируса подобен процессу репликации других одноцепочечных РНК. Репликация одноцепочечной РНК включает РНК-зависимый синтез РНК, а это означает, что ферменты, кодирующие вирус, будут частично создавать двухцепочечную РНК. Было показано, что это мнение неверно, поскольку в ретровирусной клетке не обнаружено двухцепочечной РНК. В 1964 году Говард Темин предложил гипотезу провируса, но вскоре после этого была открыта обратная транскрипция в геноме ретровируса.
Все ретровирусы имеют три основных кодирующих домена; кляп , пол и окр . В gag- области вируса поддерживается синтез внутренних белков вириона, составляющих белки матрикса, капсида и нуклеокапсида. В pol хранится информация для ферментов обратной транскрипции и интеграции. В env он происходит с поверхности и трансмембранно для белка вирусной оболочки. Существует четвертый кодирующий домен, который меньше по размеру, но существует во всех ретровирусах. Pol — это домен, который кодирует протеазу вириона.
Ретровирус начинает свое путешествие в клетку-хозяина, прикрепляя поверхностный гликопротеин к рецептору плазматической мембраны клетки. Попав внутрь клетки, ретровирус проходит обратную транскрипцию в цитоплазме и генерирует двухцепочечную ДНК-копию генома РНК. Обратная транскрипция также производит идентичные структуры, известные как длинные концевые повторы (LTR). Длинные концевые повторы находятся на концах цепей ДНК и регулируют экспрессию вирусных генов. Затем вирусная ДНК транслоцируется в ядро, где одна цепь ретровирусного генома встраивается в хромосомную ДНК с помощью вирионной интегразы. На этом этапе ретровирус называется провирусом. Попав в хромосомную ДНК, провирус транскрибируется клеточной РНК-полимеразой II. Транскрипция приводит к сплайсингу и полноразмерным мРНК, а также полноразмерной РНК потомства вириона. Белок вириона и дочерняя РНК собираются в цитоплазме и покидают клетку, тогда как другие копии отправляют транслированные вирусные сообщения в цитоплазму.

Не все онковирусы являются ДНК-вирусами . Также были ассоциированы некоторые РНК-вирусы , такие как вирус гепатита С , а также некоторые ретровирусы, например, Т-лимфотропный вирус человека (HTLV-1) и вирус саркомы Рауса (RSV).
Приблизительный процент новых случаев рака, вызванных этим вирусом, во всем мире в 2002 г. [7] NA указывает на отсутствие данных. Связь других вирусов с раком человека постоянно исследуется.

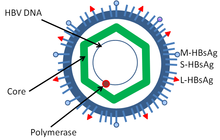
Основными вирусами, вызывающими рак человека, являются вирус папилломы человека , вирусы гепатита В и гепатита С , вирус Эпштейна-Барра , Т-лимфотропный вирус человека , герпесвирус, ассоциированный с саркомой Капоши (KSHV), и полиомавирус клеток Меркеля . Экспериментальные и эпидемиологические данные указывают на причинную роль вирусов, и они, по-видимому, являются вторым по важности фактором риска развития рака у людей, уступая только курению. [41] Тип вирусно-индуцированных опухолей можно разделить на два: остро трансформирующиеся и медленно трансформирующиеся . В вирусах с острой трансформацией вирусные частицы несут ген, который кодирует сверхактивный онкоген, называемый вирусным онкогеном (v-onc), и инфицированная клетка трансформируется, как только экспрессируется v-onc. Напротив, у медленно трансформирующихся вирусов геном вируса встраивается, тем более что вставка вирусного генома является обязательной частью ретровирусов , рядом с протоонкогеном в геноме хозяина. Вирусный промотор или другие элементы регуляции транскрипции, в свою очередь, вызывают сверхэкспрессию этого протоонкогена, что, в свою очередь, вызывает неконтролируемую клеточную пролиферацию. Поскольку вставка вирусного генома неспецифична для протоонкогенов и вероятность вставки рядом с этим протоонкогеном невелика, медленно трансформирующиеся вирусы имеют очень длительную латентную латентность опухоли по сравнению с остро трансформирующими вирусами, которые уже несут вирусный онкоген. [ нужна цитата ]
Вирусы гепатита, включая гепатит В и гепатит С , могут вызывать хроническую вирусную инфекцию, которая приводит к раку печени у 0,47% пациентов с гепатитом В в год (особенно в Азии, в меньшей степени в Северной Америке) и у 1,4% носителей гепатита С. в год. Цирроз печени, будь то вследствие хронического вирусного гепатита или алкоголизма, связан с развитием рака печени, а сочетание цирроза и вирусного гепатита представляет самый высокий риск развития рака печени. Во всем мире рак печени является одним из наиболее распространенных и самых смертоносных видов рака из-за огромного бремени передачи вирусного гепатита и других заболеваний. [ нужна цитата ]
Благодаря достижениям в области исследований рака были созданы вакцины, предназначенные для предотвращения рака. Вакцина против гепатита B является первой вакциной, созданной для предотвращения рака ( гепатоцеллюлярной карциномы ) путем предотвращения заражения вызывающим его вирусом. В 2006 году Управление по санитарному надзору за качеством пищевых продуктов и медикаментов США одобрило вакцину против вируса папилломы человека под названием Гардасил . Вакцина защищает от четырех типов ВПЧ, которые вместе вызывают 70% случаев рака шейки матки и 90% остроконечных кондилом. В марте 2007 года Консультативный комитет по практике иммунизации (ACIP) Центров по контролю и профилактике заболеваний США (CDC) официально рекомендовал вакцинацию женщинам в возрасте 11–12 лет и указал, что женщины в возрасте от 9 до 26 лет также являются кандидатами на иммунизацию. [ нужна цитата ]
История открытия вируса рака переплетается с историей исследований рака и историей вирусологии . Самым старым сохранившимся документом о раке человека является Вавилонский кодекс Хаммурапи (датированный примерно 1754 г. до н.э.), но научная онкология могла возникнуть только в 19 веке, когда опухоли изучались на микроскопическом уровне с помощью составного микроскопа и ахроматических линз . Микробиология XIX века накопила доказательства участия бактерий, дрожжей , грибов и простейших в развитии рака. В 1926 году Нобелевская премия была присуждена за подтверждение того, что червь-нематода может провоцировать рак желудка у крыс. Но то, что рак может иметь инфекционное происхождение, было признано гораздо позже, поскольку вирус был впервые обнаружен Дмитрием Ивановским и Мартинусом Бейеринком в конце XIX века. [42]

Теория о том, что рак может быть вызван вирусом, возникла с экспериментов Олуфа Банга и Вильгельма Эллермана в 1908 году в Копенгагенском университете . Банг и Эллерман продемонстрировали, что вирус птичьего саркомного лейкоза может передаваться между цыплятами после бесклеточной фильтрации и впоследствии вызывать лейкоз. [43] [44] Впоследствии это было подтверждено Пейтоном Роусом для солидных опухолей у кур в 1910–1911 годах . [45] [46] Раус из Университета Рокфеллера расширил эксперименты Банга и Эллермана, чтобы показать бесклеточную передачу саркомы солидной опухоли цыплятам (теперь известную как саркома Рауса ). Причины, по которым куры так восприимчивы к такой передаче, могут заключаться в необычных характеристиках стабильности или нестабильности, связанных с эндогенными ретровирусами . [46] [47] Шарлотта Френд подтвердила выводы Банга и Эллермана о жидкой опухоли у мышей. [48] В 1933 году Ричард Шоп и Эдвард Уэстон Херст показали, что бородавки диких кроликов содержат вирус папилломы Шопе . [42] В 1936 году Джон Джозеф Биттнер идентифицировал вирус опухоли молочной железы у мышей , «экстрахромосомный фактор» (то есть вирус), который мог передаваться между лабораторными линиями мышей при грудном вскармливании. [49]
К началу 1950-х годов было известно, что вирусы могут удалять и включать гены и генетический материал в клетки. Было высказано предположение, что такие типы вирусов могут вызывать рак путем внедрения в геном новых генов. Генетический анализ мышей, инфицированных вирусом Френд, подтвердил, что интеграция ретровирусов может нарушать гены-супрессоры опухолей, вызывая рак. [50] Впоследствии были обнаружены вирусные онкогены , которые вызывают рак. [ нужна ссылка ] Людвик Гросс идентифицировал первый вирус мышиного лейкоза ( вирус мышиного лейкоза ) в 1951 году [42] и в 1953 году сообщил о компоненте экстракта мышиного лейкоза , способном вызывать солидные опухоли у мышей. [51] Это соединение впоследствии было идентифицировано как вирус Сарой Стюарт и Бернис Эдди в Национальном институте рака , в честь которых оно когда-то было названо «SE-полиомой». [52] [53] [54] В 1957 году Шарлотта Френд обнаружила вирус Френд , штамм вируса мышиного лейкоза, способный вызывать рак у иммунокомпетентных мышей. [48] Хотя ее выводы вызвали значительную негативную реакцию, в конечном итоге они были приняты в этой области и закрепили достоверность вирусного онкогенеза. [55]
В 1961 году Эдди открыл обезьяний вакуолирующий вирус 40 ( SV40 ). Лаборатория Merck также подтвердила существование вируса макаки-резус, контаминирующего клетки, используемые для изготовления полиовакцин Солка и Сэбина . Несколько лет спустя было показано, что он вызывает рак у сирийских хомяков , что вызвало обеспокоенность по поводу возможных последствий для здоровья человека. Научный консенсус теперь полностью согласен с тем, что это вряд ли вызовет рак у человека. [56] [57]
В 1964 году Энтони Эпштейн , Берт Ачонг и Ивонн Барр идентифицировали первый человеческий онковирус из клеток лимфомы Беркитта . Этот вирус герпеса формально известен как вирус герпеса человека 4, но чаще его называют вирусом Эпштейна-Барра или ВЭБ. [58] В середине 1960-х годов Барух Блумберг впервые физически изолировал и охарактеризовал гепатит B , работая в Национальном институте здравоохранения (NIH), а затем в Онкологическом центре Фокса Чейза . [59] Хотя этот агент был явной причиной гепатита и мог способствовать развитию гепатоцеллюлярной карциномы рака печени , эта связь не была твердо установлена до тех пор, пока в 1980-х годах не были проведены эпидемиологические исследования Р. Палмером Бизли и другими. [60]
В 1980 году первый человеческий ретровирус, Т-лимфотропный вирус человека 1 (HTLV-I), был обнаружен Бернардом Поесом и Робертом Галло в Национальном институте здравоохранения [61] [62] и независимо Мицуаки Ёсида и его коллегами в Японии. [63] Но не было точно установлено, способствует ли HTLV-I лейкемии. В 1981 году Йорио Хинума и его коллеги из Киотского университета сообщили о визуализации ретровирусных частиц, продуцируемых линией лейкозных клеток, полученной от пациентов с Т-клеточным лейкозом/лимфомой взрослых . Этим вирусом оказался HTLV-1, и исследования установили причинную роль вируса HTLV-1 в развитии АТЛ. [42]

Между 1984 и 1986 годами Харальд цур Хаузен и Лутц Гиссманн обнаружили ВПЧ16 и ВПЧ18. Вместе эти папилломавирусные вирусы (ВПЧ) ответственны примерно за 70% папилломавирусных инфекций человека , вызывающих рак шейки матки . За открытие того, что ВПЧ вызывает рак у человека, в 2008 году была присуждена Нобелевская премия. [64] В 1987 году вирус гепатита С (ВГС) был обнаружен путем анализа библиотеки кДНК, полученной из больных тканей, на наличие чужеродных антигенов, распознаваемых сывороткой пациентов. Эту работу выполнили Майкл Хоутон из биотехнологической компании Chiron и Дэниел У. Брэдли из Центров по контролю и профилактике заболеваний (CDC). [65] Впоследствии было показано, что ВГС является основным виновником гепатоцеллюлярной карциномы (рака печени) во всем мире. [42]
В 1994 году Патрик С. Мур и Юань Чанг из Колумбийского университета , работая вместе с Этель Сезарман, [66] [67] выделили герпесвирус, ассоциированный с саркомой Капоши (KSHV или HHV8), используя анализ репрезентативных различий . Этот поиск был вызван работой Валери Бераль и ее коллег, которые на основании эпидемии саркомы Капоши среди пациентов со СПИДом сделали вывод, что этот рак должен быть вызван другим инфекционным агентом, помимо ВИЧ, и что это, вероятно, был второй вирус. [68] Последующие исследования показали, что KSHV является «агентом СК» и отвечает за эпидемиологическую картину СК и связанных с ним видов рака. [69]
В 2008 году Юань Чанг и Патрик С. Мур разработали новый метод идентификации раковых вирусов, основанный на компьютерном вычитании последовательностей человека из транскриптома опухоли , названный вычитанием цифрового транскриптома (DTS). [70] DTS использовался для выделения фрагментов ДНК полиомавируса клеток Меркеля из карциномы клеток Меркеля, и в настоящее время считается, что этот вирус вызывает 70–80% этих видов рака. [25]
Вирусы, известные как онкогенные РНК-вирусы или онкорнавирусы, были описаны у самых разных видов позвоночных [...] было очень мало, если вообще были, полностью убедительных примеров выделения онкорнавирусов человека.
{{cite book}}: |work=игнорируется ( помощь )