Вирус Эпштейна -Барра ( ВЭБ ), формально называемый гаммагерпесвирусом человека 4 , является одним из девяти известных типов вируса герпеса человека семейства герпеса и одним из наиболее распространенных вирусов у человека. ВЭБ представляет собой вирус с двухцепочечной ДНК . [2] Вирус Эпштейна-Барр (ВЭБ) является первым выявленным онкогенным вирусом , вызывающим стойкую инфекцию у человека. ВЭБ вызывает инфекционный мононуклеоз , а также тесно связан со многими злокачественными заболеваниями. Различные составы вакцин прошли испытания на разных животных или на людях. Однако ни один из них не смог предотвратить заражение ВЭБ, и на сегодняшний день ни одна вакцина не одобрена. [3]
Вирус вызывает инфекционный мононуклеоз («моно» или «железистая лихорадка»). Он также связан с различными доброкачественными, предраковыми и злокачественными лимфопролиферативными заболеваниями, связанными с вирусом Эпштейна-Барра, такими как лимфома Беркитта , гемофагоцитарный лимфогистиоцитоз [4] и лимфома Ходжкина ; нелимфоидные злокачественные новообразования, такие как рак желудка и карцинома носоглотки ; и состояния, связанные с вирусом иммунодефицита человека , такие как волосатая лейкоплакия и лимфомы центральной нервной системы . [5] [6] Вирус также связан с детскими расстройствами, такими как синдром Алисы в стране чудес [7] и острой мозжечковой атаксией [8] и, по некоторым данным, с более высоким риском развития некоторых аутоиммунных заболеваний , [9] особенно дерматомиозита , системная красная волчанка , ревматоидный артрит и синдром Шегрена . [10] [11] Считается, что около 200 000 случаев рака во всем мире в год связаны с ВЭБ. [12] [13] В 2022 году крупное исследование (10 миллионов человек за 20 лет) показало, что ВЭБ является основной причиной рассеянного склероза , при этом недавняя инфекция ВЭБ вызвала 32-кратное увеличение риска развития рассеянного склероза. [14] [15] [16] [17] [18]
Заражение ВЭБ происходит при пероральном переносе слюны [19] и генитальных выделений. Большинство людей заражаются ВЭБ и приобретают адаптивный иммунитет . В США около половины всех пятилетних детей и около 90% взрослых имеют признаки предшествующего заражения. [20] Младенцы становятся восприимчивыми к ВЭБ, как только исчезает защита материнских антител . У многих детей, инфицированных ВЭБ, симптомы не проявляются или симптомы неотличимы от других легких и кратковременных заболеваний детского возраста. [21] Когда инфекция возникает в подростковом или молодом возрасте, она вызывает инфекционный мононуклеоз в 35–50% случаев. [22]
ВЭБ инфицирует В-клетки иммунной системы и эпителиальные клетки . Как только первоначальная литическая инфекция EBV взята под контроль, латентный период EBV сохраняется в В-клетках памяти человека на всю оставшуюся жизнь. [19] [23] [24]
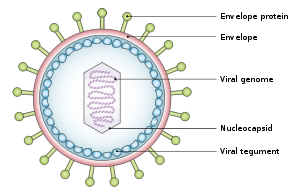
Вирус имеет диаметр около 122–180 нм и состоит из двойной спирали дезоксирибонуклеиновой кислоты (ДНК), которая содержит около 172 000 пар оснований , кодирующих 85 генов . [19] ДНК окружена белковым нуклеокапсидом , который окружен тегументом, состоящим из белка, который, в свою очередь, окружен оболочкой , содержащей как липиды , так и поверхностные проекции гликопротеинов , которые необходимы для заражения клетки-хозяина. [25] В июле 2020 года группа исследователей сообщила о первой полной атомной модели нуклеокапсида вируса. Эта «первая полная атомная модель [включает] икосаэдрический капсид, комплекс тегумента, связанный с капсидом (CATC), и додекамерный портал — аппарат транслокации вирусного генома». [26] [27]
Термин вирусный тропизм относится к типам клеток, которые инфицирует ВЭБ. ВЭБ может инфицировать различные типы клеток, включая В-клетки и эпителиальные клетки . [28]
Вирусные трехкомпонентные гликопротеиновые комплексы gHgL gp42 опосредуют слияние мембран В-клеток; хотя двухкомпонентные комплексы gHgL опосредуют слияние мембран эпителиальных клеток. ВЭБ, образующийся в В-клетках, имеет небольшое количество комплексов gHgLgp42, поскольку эти трехкомпонентные комплексы взаимодействуют с молекулами человеческого лейкоцитарного антигена класса II , присутствующими в В-клетках эндоплазматического ретикулума, и разрушаются. Напротив, EBV из эпителиальных клеток богат трехкомпонентными комплексами, поскольку эти клетки обычно не содержат молекул HLA класса II . Как следствие, ВЭБ, полученный из В-клеток, более инфекционен для эпителиальных клеток, а ВЭБ, полученный из эпителиальных клеток, более инфекционен для В-клеток. Вирусы, у которых отсутствует часть gp42, способны связываться с В-клетками человека, но не способны инфицировать. [29]

ВЭБ может инфицировать как В-клетки, так и эпителиальные клетки. Механизмы проникновения в эти две клетки различны.
Чтобы проникнуть в В-клетки, вирусный гликопротеин gp350 связывается с клеточным рецептором CD21 (также известным как CR2). [30] Затем вирусный гликопротеин gp42 взаимодействует с клеточными молекулами MHC класса II . Это вызывает слияние вирусной оболочки с клеточной мембраной, позволяя ВЭБ проникнуть в В-клетку. [25] CD35 человека, также известный как рецептор комплемента 1 (CR1), является дополнительным фактором прикрепления gp350/220 и может обеспечивать путь проникновения EBV в CD21-негативные клетки, включая незрелые B-клетки. Инфекция EBV снижает экспрессию CD35. [31]
Для проникновения в эпителиальные клетки вирусный белок BMRF-2 взаимодействует с клеточными интегринами β1 . Затем вирусный белок gH/gL взаимодействует с клеточными интегринами αvβ6/αvβ8. Это вызывает слияние вирусной оболочки с мембраной эпителиальной клетки, позволяя ВЭБ проникнуть в эпителиальную клетку. [25] В отличие от проникновения B-клеток, проникновению эпителиальных клеток фактически препятствует вирусный гликопротеин gp42. [30]
Как только EBV проникает в клетку, вирусный капсид растворяется, и вирусный геном транспортируется в ядро клетки . [ нужна цитата ]
Литический цикл , или продуктивная инфекция, приводит к образованию инфекционных вирионов . ВЭБ может подвергаться литической репликации как в В-клетках, так и в эпителиальных клетках. В В-клетках литическая репликация обычно происходит только после реактивации из латентного периода. В эпителиальных клетках литическая репликация часто следует непосредственно за проникновением вируса. [25]
Для того чтобы произошла литическая репликация, вирусный геном должен быть линейным. Латентный геном ВЭБ имеет кольцевую форму, поэтому он должен линеаризоваться в процессе литической реактивации. Во время литической репликации вирусная ДНК-полимераза отвечает за копирование вирусного генома. Это контрастирует с латентным периодом, при котором ДНК-полимераза клетки-хозяина копирует вирусный геном. [25]
Продукты литического гена производятся в три последовательных этапа: немедленный-ранний, ранний и поздний. [25] Продукты немедленных и ранних литических генов действуют как трансактиваторы , усиливая экспрессию более поздних литических генов. Продукты немедленно-раннего литического гена включают BZLF1 (также известный как Zta, EB1, связанный с его геном-продуктом ZEBRA ) и BRLF1 (связанный с его геном-продуктом Rta ). [25] Ранние литические генные продукты выполняют гораздо больше функций, таких как репликация, метаболизм и блокада обработки антигена . Ранние литические генные продукты включают BNLF2. [25] Наконец, поздние литические генные продукты, как правило, представляют собой белки со структурной ролью, такие как VCA , который образует вирусный капсид . Другие продукты позднего литического гена, такие как BCRF1, помогают ВЭБ уклоняться от иммунной системы. [25]
ЭГКГ , полифенол, содержащийся в зеленом чае , в исследовании показал, что он ингибирует спонтанную литическую инфекцию EBV на уровне ДНК, транскрипции генов и белка в зависимости от времени и дозы ; экспрессия литических генов EBV Zta, Rta и раннего антигенного комплекса EA-D (индуцированная Rta ), однако высокостабильный ген EBNA-1, обнаруженный на всех стадиях инфекции EBV, не затрагивается. [32] Специфические ингибиторы (путей) позволяют предположить, что путь Ras/MEK/MAPK способствует литической инфекции EBV через путь BZLF1 и PI3-K через BRLF1, причем последний полностью устраняет способность аденовирусного вектора BRLF1 индуцировать литическую форму ВЭБ-инфекция. [32] Кроме того, активация некоторых генов, но не других, изучается, чтобы определить, как вызвать иммунное разрушение латентно инфицированных В-клеток с помощью ТРА или бутирата натрия . [32]
В отличие от литической репликации, латентный период не приводит к образованию вирионов. [25] Вместо этого кольцевая ДНК генома EBV находится в ядре клетки в виде эписомы и копируется клеточной ДНК-полимеразой . [25] Он сохраняется в В-клетках памяти человека . [19] [24] Эпигенетические изменения, такие как метилирование ДНК и компоненты клеточного хроматина , подавляют большинство вирусных генов в латентно инфицированных клетках. [33] Экспрессируется только часть генов ВЭБ , которые поддерживают латентное состояние вируса. [33] [19] [34] Латентный ВЭБ экспрессирует свои гены по одному из трех паттернов, известных как латентные программы. ВЭБ может латентно персистировать внутри В-клеток и эпителиальных клеток , но в этих двух типах клеток возможны разные латентные программы. [ нужна цитата ]
EBV может иметь одну из трех программ задержки: Latency I, Latency II или Latency III. Каждая латентная программа приводит к выработке ограниченного, отдельного набора вирусных белков и вирусных РНК . [35] [36]
Кроме того, постулируется программа, в которой отключается вся экспрессия вирусных белков (латентность 0). [37]
Внутри В-клеток возможны все три латентные программы. [19] Латентный период EBV внутри B-клеток обычно прогрессирует от латентного периода III до латентного периода II, а затем до латентного периода I. Каждая стадия латентного периода уникальным образом влияет на поведение B-клеток. [19] При инфицировании покоящейся наивной В-клетки ВЭБ переходит в латентный период III. Набор белков и РНК, вырабатываемых в латентном периоде III, превращает В-клетку в пролиферирующий бласт (также известный как активация В-клеток). [19] [25] Позже вирус ограничивает экспрессию своих генов и переходит в латентный период II. Более ограниченный набор белков и РНК, вырабатываемых в латентном периоде II, побуждает В-клетку дифференцироваться в В-клетку памяти . [19] [25] Наконец, EBV еще больше ограничивает экспрессию генов и переходит в латентную фазу I. Экспрессия EBNA-1 позволяет геному EBV реплицироваться при делении B-клеток памяти. [19] [25]
Внутри эпителиальных клеток возможна только латентность II. [38]
При первичной инфекции ВЭБ реплицируется в эпителиальных клетках ротоглотки и создает латентную стадию III, II и I инфекции в В-лимфоцитах. Латентная инфекция В-лимфоцитов ВЭБ необходима для персистенции вируса, последующей репликации в эпителиальных клетках и выхода инфекционного вируса в слюну. Латентные инфекции III и II ВЭБ В-лимфоцитов, латентная инфекция II эпителиальных клеток полости рта и латентная инфекция II NK- или Т-клеток могут привести к злокачественным новообразованиям, характеризующимся однородным присутствием генома EBV и экспрессией генов. [39]
Латентный EBV в B-клетках может быть реактивирован для переключения на литическую репликацию. Известно, что это происходит in vivo , но что именно вызывает это, точно неизвестно. In vitro латентный EBV в B-клетках может быть реактивирован путем стимуляции рецептора B-клеток, поэтому вполне вероятно, что реактивация in vivo происходит после того, как латентно инфицированные B-клетки отвечают на несвязанные инфекции. [25]
Когда EBV инфицирует B-клетки in vitro , в конечном итоге возникают линии лимфобластоидных клеток, способные к неопределенному росту. Ростовая трансформация этих клеточных линий является следствием экспрессии вирусного белка. [40]
EBNA-2, EBNA-3C и LMP-1 необходимы для трансформации, тогда как EBNA-LP и EBER — нет. [41]
Считается, что после естественного заражения EBV вирус выполняет некоторые или все свои программы экспрессии генов, создавая стойкую инфекцию. Учитывая первоначальное отсутствие иммунитета хозяина , литический цикл производит большое количество вирионов для заражения других (предположительно) B-лимфоцитов внутри хозяина.
Латентные программы перепрограммируют и разрушают инфицированные В-лимфоциты, заставляя их пролиферировать и доставлять инфицированные клетки в места, где предположительно сохраняется вирус. В конце концов, когда иммунитет хозяина развивается, вирус сохраняется, отключая большую часть (или, возможно, все) своих генов, и лишь изредка реактивируется и производит вирионы-потомки. В конечном итоге достигается баланс между периодической реактивацией вируса и иммунным надзором хозяина, удаляющим клетки, которые активируют экспрессию вирусных генов. Манипулирование эпигенетикой человеческого организма с помощью EBV может изменить геном клетки, оставив онкогенные фенотипы. [42] В результате модификация EBV увеличивает вероятность развития рака, связанного с EBV. [43] Раковые заболевания, связанные с ВЭБ, уникальны тем, что они часто вызывают эпигенетические изменения, но с меньшей вероятностью мутируют. [44]
Местом персистенции ВЭБ может быть костный мозг . EBV-положительные пациенты, которым был заменен костный мозг костного мозга от EBV-отрицательного донора, после трансплантации оказываются EBV-отрицательными . [45]
Все ядерные белки EBV производятся путем альтернативного сплайсинга транскрипта, начинающегося с промоторов Cp или Wp на левом конце генома ( в общепринятой номенклатуре). Гены упорядочены в геноме EBNA-LP/EBNA-2/EBNA-3A/EBNA-3B/EBNA-3C/EBNA-1 .
Инициирующий кодон кодирующей области EBNA-LP создается путем альтернативного сплайсинга транскрипта ядерного белка. В отсутствие этого инициирующего кодона EBNA-2/EBNA-3A/EBNA-3B/EBNA-3C/EBNA-1 будут экспрессироваться в зависимости от того, какой из этих генов альтернативно сплайсирован в транскрипт.
ВЭБ можно разделить на два основных типа: ВЭБ типа 1 и ВЭБ типа 2. Эти два подтипа имеют разные гены EBNA-3 . В результате эти два подтипа различаются по своим преобразующим способностям и способности к реактивации. Тип 1 преобладает на большей части мира, но оба типа одинаково распространены в Африке . Отличить ВЭБ типа 1 от ВЭБ типа 2 можно, разрезав вирусный геном с помощью фермента рестрикции и сравнив полученные закономерности переваривания с помощью гель-электрофореза . [25]
Малые РНК, кодируемые вирусом Эпштейна-Барр (EBER), на сегодняшний день являются наиболее распространенными продуктами EBV, транскрибируемыми в клетках, инфицированных EBV. Их обычно используют в качестве мишеней для обнаружения ВЭБ в гистологических тканях. [46]
ВЭБ вызывает инфекционный мононуклеоз. [50] Дети, инфицированные ВЭБ, имеют мало симптомов или могут протекать бессимптомно, но когда заражение происходит в подростковом или взрослом возрасте, оно может вызвать усталость , лихорадку , воспаление горла , увеличение лимфатических узлов на шее, увеличение селезенки , опухание печени или сыпь. . [20] Постинфекционный синдром хронической усталости также связан с инфекцией ВЭБ. [51] [52]
ВЭБ также вовлечен в ряд других заболеваний, включая лимфому Беркитта , [53] гемофагоцитарный лимфогистиоцитоз , [54] лимфому Ходжкина , [55] рак желудка , [12] [56] рак носоглотки , [57] рассеянный склероз , [15] [16] [58] [17] и лимфоматоидный гранулематоз . [59]
В частности, было показано, что B-клетки, инфицированные EBV, обитают в очагах поражения головного мозга пациентов с рассеянным склерозом [17] , а исследование 2022 года, посвященное историческим образцам крови 10 миллионов солдат, показало, что «люди, которые не были инфицированы вирусом Эпштейна-Барра, практически никогда не заболевайте рассеянным склерозом. Только после заражения вирусом Эпштейна-Барра риск рассеянного склероза возрастает более чем в 30 раз", и только ВЭБ из многих инфекций имел столь четкую связь с заболеванием. [60]
Дополнительные заболевания, связанные с ВЭБ, включают синдром Джанотти-Крости , мультиформную эритему , острые генитальные язвы и волосатую лейкоплакию полости рта . [61] Вирусная инфекция также связана и часто способствует развитию широкого спектра незлокачественных лимфопролиферативных заболеваний , таких как тяжелые аллергические реакции гиперчувствительности на укусы комаров , [62] слизисто-кожные язвы, положительные на вирус Эпштейна-Барра , и Hydroa vacciniforme , а также злокачественные лимфопролиферативные заболевания, такие как вирус-положительная лимфома Беркитта Эпштейна-Барра , [63] вирус-положительная лимфома Ходжкина Эпштейна-Барра , [64] и первичная выпотная лимфома . [65]
Вирус Эпштейна-Барр вовлечен в нарушения, связанные с агрегацией альфа-синуклеина (например , болезнь Паркинсона , деменция с тельцами Леви и множественная системная атрофия ). [66]
Было обнаружено, что EBNA1 может вызывать хромосомные разрывы в 11-й хромосоме , особенно в области 11q23 между геном FAM55D и FAM55B, к которой EBNA-1, по-видимому, имеет высокое сродство из-за его ДНК-связывающего домена, проявляющего интерес к специфический палиндромный повтор в этом участке генома. [67] Хотя причина и точный механизм этого неизвестны, побочный продукт приводит к ошибкам и нарушению хромосомной структуры, поскольку клетки, происходящие из линии испорченного генома, подвергаются митозу . Поскольку гены в этой области вовлечены в лейкемию и являются домом для гена-супрессора опухоли , который модифицирован или отсутствует в экспрессии большинства опухолевых генов, была выдвинута гипотеза, что нарушение в этой области является основным виновником рака, что ВЭБ увеличивает вероятность из. Поломка также зависит от дозы: у человека с латентной инфекцией поломка будет меньше, чем у человека с новой или реактивированной инфекцией, поскольку уровни EBNA1 в ядре и ядрышке выше во время активной атаки организма из-за постоянной репликации и поглощения. переизбыток клеток в организме.
Вирус Эпштейна-Барра был назван в честь М.А. Эпштейна и Ивонн Барр , открывших вирус вместе с Бертом Ачонгом . [68] [69] В 1961 году Эпштейн, патолог и эксперт по электронной микроскопии , посетил лекцию Д. П. Беркитта , хирурга, практикующего в Уганде , на тему «Самый распространенный детский рак в тропической Африке — до сих пор нераспознанный синдром» , в которой Беркитт описал «эндемический вариант» (детская форма) заболевания, носящего теперь его имя . В 1963 году образец был отправлен из Уганды в больницу Миддлсекса для культивирования. Вирусные частицы были идентифицированы в культивируемых клетках, и результаты были опубликованы в журнале The Lancet в 1964 году Эпштейном, Ачонгом и Барром. [69] [70] Клеточные линии были отправлены Вернеру и Гертруде Хенле в Детскую больницу Филадельфии , которые разработали серологические маркеры. [71] В 1967 году у техника в их лаборатории развился мононуклеоз, и они смогли сравнить сохраненный образец сыворотки, показав, что выработались антитела к вирусу. [70] [72] [73] В 1968 году они обнаружили, что ВЭБ может непосредственно иммортализовать В-клетки после заражения, имитируя некоторые формы инфекций, связанных с ВЭБ, [71] и подтвердили связь между вирусом и инфекционным мононуклеозом. [74]
Будучи относительно сложным вирусом, ВЭБ еще не до конца изучен. Лаборатории по всему миру продолжают изучать вирус и разрабатывать новые способы лечения заболеваний, которые он вызывает. Одним из популярных способов изучения ВЭБ in vitro является использование искусственных бактериальных хромосом . [75] Вирус Эпштейна-Барра можно поддерживать и манипулировать в лаборатории в непрерывном латентном периоде (свойство, общее с герпесвирусом, ассоциированным с саркомой Капоши , еще одним из восьми вирусов герпеса человека). Хотя предполагается, что многие вирусы обладают этим свойством во время заражения своих естественных хозяев, не существует легко управляемой системы для изучения этой части жизненного цикла вируса. Геномные исследования EBV позволили изучить литическую реактивацию и регуляцию латентной вирусной эписомы. [76]
Несмотря на активные исследования, вакцина против вируса Эпштейна-Барра еще не доступна. Разработка эффективной вакцины могла бы предотвратить до 200 000 случаев рака во всем мире в год. [12] Отсутствие эффективных моделей на животных является препятствием для разработки профилактических и терапевтических вакцин против ВЭБ. [24]
Как и другие вирусы герпеса человека, вирус Эпштейна-Барра может позволить уничтожить его самостоятельно с помощью курса препарата валацикловир , но необходимы дальнейшие исследования, чтобы определить, действительно ли эрадикация достижима. [42] Противовирусные агенты действуют путем ингибирования репликации вирусной ДНК, но имеется мало доказательств того, что они эффективны против вируса Эпштейна-Барра. Более того, они дороги, рискуют вызвать устойчивость к противовирусным препаратам и (в 1–10% случаев) могут вызывать неприятные побочные эффекты . [43]