

В органической химии карбоксилат — это сопряженное основание карбоновой кислоты , RCOO − (или RCO−2). Это анион , ион с отрицательным зарядом .
Карбоксилатные соли — это соли , имеющие общую формулу M(RCOO) n , где M — металл, а n равно 1, 2,.... Карбоксилатные эфиры имеют общую формулу RCOOR′ (также пишется как RCO 2 R′ ), где R и R′ — органические группы.
Карбоксилатные ионы могут быть образованы депротонированием карбоновых кислот. Такие кислоты обычно имеют p K a менее 5, что означает, что они могут быть депротонированы многими основаниями, такими как гидроксид натрия или бикарбонат натрия . [1] : 271–2
Карбоновые кислоты легко диссоциируют на карбоксилат-анион и положительно заряженный ион водорода (протон), гораздо легче, чем спирты (на алкоксид -ион и протон), поскольку карбоксилат-ион стабилизируется резонансом . Отрицательный заряд, который остается после депротонирования карбоксильной группы, делокализован между двумя электроотрицательными атомами кислорода в резонансной структуре. Если группа R является электроноакцепторной группой (такой как –CF 3 ), основность карбоксилата будет еще больше ослаблена. [1] : 264–5
Эта делокализация электрона означает, что оба атома кислорода менее сильно отрицательно заряжены: положительный протон, следовательно, менее сильно притягивается обратно к карбоксилатной группе после того, как он ушел; следовательно, карбоксилатный ион более стабилен и менее основен в результате резонансной стабилизации отрицательного заряда. Напротив, ион алкоксида , однажды образованный, будет иметь сильный отрицательный заряд, локализованный на его одиночном атоме кислорода, который будет сильно притягивать любые близлежащие протоны (действительно, алкоксиды являются очень сильными основаниями). Из-за резонансной стабилизации карбоновые кислоты имеют гораздо более низкие значения p K a (и, следовательно, являются более сильными кислотами), чем спирты . Например, значение p K a уксусной кислоты составляет 4,8, в то время как этанол имеет ap K a 16. Следовательно, уксусная кислота является гораздо более сильной кислотой, чем этанол. Это, в свою очередь, означает, что для эквимолярных растворов карбоновой кислоты или спирта в воде карбоновая кислота будет иметь гораздо более низкий pH . [1] : 263–7
Соли карбоновых кислот с атомом водорода в альфа- положении рядом с карбоксилатной группой могут быть преобразованы в дианионы с сильными основаниями, такими как диизопропиламид лития . Они реагируют с алкилгалогенидами, давая производные: [1] : 474
Карбоксилатные ионы являются хорошими нуклеофилами . Они реагируют с алкилгалогенидами с образованием сложных эфиров . Следующая реакция показывает механизм реакции. [1] : 398–9
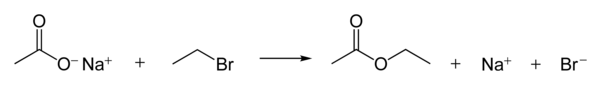
Нуклеофильность карбоксилат-ионов намного слабее, чем у гидроксид- и алкоксид -ионов, но сильнее, чем у галогенид- анионов (в полярном апротонном растворителе , хотя существуют и другие эффекты, такие как растворимость иона).
В отличие от восстановления сложного эфира, восстановление карбоксилата отличается из-за отсутствия уходящей группы и относительно богатого электронами атома углерода (из-за отрицательного заряда на атомах кислорода). При небольшом количестве кислоты реакция происходит с литийалюминийгидридом , изменяя LAH в кислоту Льюиса AlH 3 в процессе, преобразуя оксианион в 4 связи Al–O. [1] : 1212
Этот список предназначен для случаев, когда есть отдельная статья для аниона или его производных. Все другие органические кислоты должны быть найдены по их родительской карбоновой кислоте.