Опухоль надпочечника или образование надпочечника [ 2] — это любые доброкачественные или злокачественные новообразования надпочечников , некоторые из которых отличаются склонностью к избыточной выработке эндокринных гормонов . Рак надпочечников представляет собой наличие злокачественных опухолей надпочечников и включает нейробластому , адренокортикальную карциному и некоторые феохромоцитомы надпочечников . Большинство феохромоцитом надпочечников и все адренокортикальные аденомы являются доброкачественными опухолями, которые не метастазируют и не проникают в близлежащие ткани, но могут вызывать серьезные проблемы со здоровьем из-за нарушения баланса гормонов.
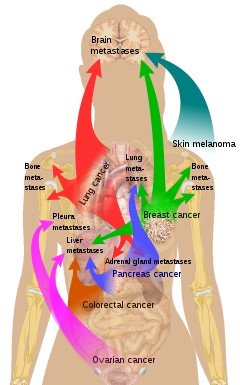
Метастазирование в один или оба надпочечника является наиболее распространенной формой злокачественного поражения надпочечников и второй по распространенности опухолью надпочечников после доброкачественных аденом. [4] Первичные опухоли в таких случаях чаще всего возникают из-за рака легких (39%), рака молочной железы (35%), злокачественной меланомы , рака желудочно-кишечного тракта , рака поджелудочной железы и рака почки . [4]
Кора надпочечников состоит из трех отдельных слоев эндокринных клеток, которые производят важные стероидные гормоны . К ним относятся глюкокортикоиды , которые имеют решающее значение для регулирования уровня сахара в крови и иммунной системы , а также реакции на физиологический стресс ; минералкортикоид альдостерон , который регулирует кровяное давление и функцию почек ; и некоторые половые гормоны . Как доброкачественные , так и злокачественные опухоли коры надпочечников могут продуцировать стероидные гормоны, что имеет важные клинические последствия. [ нужна цитата ]
Адренокортикальные аденомы представляют собой доброкачественные опухоли коры надпочечников, которые встречаются чрезвычайно часто (на аутопсии обнаруживаются у 1–10% лиц). Их не следует путать с адренокортикальными «узлами», которые не являются настоящими новообразованиями. Адренокортикальные аденомы редко встречаются у пациентов моложе 30 лет и встречаются с одинаковой частотой у обоих полов. [ нужна цитация ] Клиническое значение этих новообразований двоякое. Во-первых, в последние годы их все чаще выявляют как случайные находки из-за увеличения использования компьютерной томографии и магнитно-резонансной томографии в различных медицинских учреждениях. Это может привести к дорогостоящим дополнительным исследованиям и инвазивным процедурам, чтобы исключить небольшую вероятность ранней адренокортикальной карциномы . Во-вторых, меньшинство (около 15%) аденом коры надпочечников являются «функциональными», то есть они вырабатывают глюкокортикоиды , минералкортикоиды и/или половые стероиды , что приводит к эндокринным расстройствам, таким как синдром Кушинга , синдром Конна (гиперальдостеронизм), вирилизация женщин, или феминизация мужчин. Функциональные адренокортикальные аденомы поддаются хирургическому лечению. [ нужна цитата ]
Большинство адренокортикальных аденом имеют размер менее 2 см и массу менее 50 грамм. Однако размер и масса опухолей коры надпочечников больше не считаются надежным признаком доброкачественности или злокачественности. В целом адренокортикальные аденомы представляют собой инкапсулированные, хорошо очерченные, одиночные опухоли с твердой однородной поверхностью желтого цвета. Некроз и кровоизлияния встречаются редко. [ нужна цитата ]
Адренокортикальная карцинома (АКК) — редкий, высокоагрессивный рак клеток коры надпочечников, который может возникнуть у детей и взрослых. АКК могут быть «функциональными», продуцирующими стероидные гормоны и, как следствие, эндокринную дисфункцию, аналогичную той, которая наблюдается при многих аденомах коры надпочечников, но многие из них таковыми не являются. Из-за своего расположения глубоко в забрюшинном пространстве большинство адренокортикальных карцином не диагностируются до тех пор, пока они не достигнут достаточно больших размеров. Они часто проникают в крупные сосуды, такие как почечная вена и нижняя полая вена , а также метастазируют через лимфатические сосуды и кровь в легкие и другие органы. Наиболее эффективным лечением является хирургическое вмешательство , хотя для многих пациентов оно неосуществимо, а общий прогноз заболевания неблагоприятный. Химиотерапия , лучевая терапия и гормональная терапия также могут использоваться при лечении этого заболевания. [ нужна цитата ]
Мозговое вещество надпочечников анатомически расположено в центре каждого надпочечника и состоит из нейроэндокринных (хромаффинных) клеток, которые производят и выделяют адреналин (адреналин) в кровоток в ответ на активацию симпатической нервной системы . Нейробластома и феохромоцитома — две наиболее важные опухоли, возникающие из мозгового вещества надпочечников. Обе опухоли могут также возникать из вненадпочечниковых участков, в частности, в параганглиях симпатической цепи . [ нужна цитата ]
Нейробластома представляет собой агрессивный рак незрелых нейробластических клеток (предшественников нейронов ) и является одним из наиболее распространенных видов рака у детей со средним возрастом постановки диагноза два года. [5] Нейробластома надпочечника обычно проявляется быстро увеличивающимся образованием в брюшной полости. Хотя на момент постановки диагноза опухоль часто распространяется на отдаленные части тела, этот рак необычен тем, что во многих случаях он хорошо излечим, когда распространение ограничивается печенью , кожей и /или костным мозгом (стадия IVS). Родственные, но менее агрессивные опухоли, состоящие из более зрелых нервных клеток, включают ганглионейробластому и ганглионеврому . Нейробластные опухоли часто продуцируют повышенные уровни метаболитов гормона катехоламинов , таких как ванилилминдальная кислота (ВМА) и гомованилиновая кислота , и могут вызывать тяжелую водянистую диарею за счет продукции вазоактивного кишечного пептида . Лечение нейробластомы включает хирургическое вмешательство и лучевую терапию при локализованном заболевании, а также химиотерапию при метастатическом заболевании. [6]
Феохромоцитома — новообразование , состоящее из клеток, сходных с хромаффинными клетками зрелого мозгового слоя надпочечников. Феохромоцитомы встречаются у пациентов всех возрастов и могут быть спорадическими или связаны с наследственным раковым синдромом , таким как множественная эндокринная неоплазия (МЭН) типов IIA и IIB, нейрофиброматоз типа I или синдром фон Хиппеля-Линдау . Лишь 10% феохромоцитом надпочечников являются злокачественными , остальные — доброкачественными опухолями . Наиболее клинически важной особенностью феохромоцитом является их склонность к выработке большого количества гормонов катехоламинов адреналина ( адреналина) и норадреналина . Это может привести к потенциально опасному для жизни высокому кровяному давлению или сердечной аритмии , а также многочисленным симптомам, таким как головная боль , сердцебиение , приступы паники , потливость , потеря веса и тремор . Диагноз легче всего подтвердить путем измерения в моче метаболитов катехоламинов , таких как VMA и метанефрины . Большинство феохромоцитом первоначально лечат антиадренергическими препаратами для защиты от перегрузки катехоламинами, а после того, как пациент становится медицински стабильным, опухоль удаляют хирургическим путем. [7]
Инциденталома надпочечников — это опухоль надпочечников, обнаруженная случайно без клинических симптомов или подозрений. Это один из наиболее частых неожиданных результатов, выявляемых с помощью компьютерной томографии (КТ), магнитно-резонансной томографии (МРТ) или ультразвукового исследования. [8]
В этих случаях для выявления избытка кортизола часто используют тест на подавление дексаметазоном , а при избытке этих гормонов — метанефринов или катехоламинов . Опухоли размером менее 3 см обычно считаются доброкачественными и подлежат лечению только при наличии оснований для диагноза синдрома Кушинга или феохромоцитомы . [9] Радиоплотность дает ключ к оценке риска злокачественного новообразования, при этом опухоль с 10 единицами Хаунсфилда или менее на неусиленной КТ, вероятно, является аденомой, богатой липидами. [10] Гормональная оценка включает: [11]
При КТ доброкачественные аденомы обычно имеют низкую рентгенографическую плотность (из-за содержания жира) и быстрое вымывание контрастного вещества (50% или более контрастного вещества вымывается за 10 минут). Если гормональная оценка отрицательна и визуализация предполагает доброкачественный результат, следует рассмотреть возможность последующего наблюдения с визуализацией через 6, 12 и 24 месяца и повторять гормональную оценку ежегодно в течение 4 лет [11].
Хирургический
При карциноме надпочечников наиболее эффективным методом лечения является хирургическое вмешательство , хотя для многих пациентов оно неосуществимо, а общий прогноз заболевания неблагоприятный. Химиотерапия , лучевая терапия и гормональная терапия также могут использоваться при лечении этого заболевания.
В Кокрейновском систематическом обзоре 2018 года сравнивались два различных типа хирургического вмешательства: лапароскопическая ретроперотенальная адреналэктомия и лапороскопическая трансперитоенальная адренелэктомия при различных типах опухолей надпочечников. [12] Лапароскопическая ретроперотенальная адреналэктомия, по-видимому, снижает позднюю заболеваемость, время до приема жидкости или пищи, а также время до передвижения по сравнению с лапароскопической трансперитоенальной адреналэктомией. [12] Однако в этих результатах существовала неопределенность из-за низкого качества доказательств, а также неубедительных результатов о влиянии любой операции на смертность от всех причин, раннюю заболеваемость, социально-экономические последствия, продолжительность операции, операционную кровопотерю, переход на открытую операцию. операция. [12]
МикроРНК, циркулирующие в крови (миРНК), исследовались в последние годы на предмет их потенциального использования в качестве менее инвазивного биомаркера заболеваний надпочечников. На данный момент в девяти исследованиях изучалось появление циркулирующих микроРНК в крови пациентов с диагностированными опухолями коры надпочечников. [13] [14] МикроРНК могут попадать в кровоток тремя различными способами экскреции. [15] Повреждение клеток с пассивным высвобождением (некроз, воспаление), активной секрецией в виде внеклеточных везикул (ВВ) (микровезикулы, экзосомы и апоптотические тельца) или в ассоциации с липопротеинами высокой плотности (ЛПВП) и белками аргонавта (AGO). [16] [17] Большинство микроРНК, обнаруженных в крови, находятся в комплексах с AGO. [18] [19] Несмотря на многообещающие результаты, чувствительность потенциальных циркулирующих маркеров микроРНК для опухолей коры надпочечников, по-видимому, варьируется. Повышение чувствительности может быть достигнуто путем нацеливания только на микроРНК, ассоциированные с ЭВ, поскольку предполагается, что высвобождение микроРНК в ЭВ является контролируемым процессом. [20] Таким образом, EV-ассоциированные микроРНК могут действовать как более специфические маркеры злокачественных новообразований. [20] Однако, поскольку существовали значительные различия в результатах проведенных исследований, этому несоответствию могли способствовать методологические различия и небольшое количество пациентов. Это требует дальнейших исследований на более крупных когортах с едиными методологическими требованиями для выяснения применимости циркулирующих микроРНК в качестве биомаркеров прогноза и злокачественности у пациентов с диагнозом адренокортикальных опухолей. [13]
{{cite book}}: |website=игнорируется ( помощь )