Альдольная реакция ( альдольное присоединение ) — это реакция в органической химии , которая объединяет два карбонильных соединения (например, альдегиды или кетоны ) с образованием нового β-гидроксикарбонильного соединения. Его простейшая форма может включать нуклеофильное присоединение енолированного кетона к другому:

Эти продукты известны как альдолы , от сочетания альдегид + спирт — структурного мотива, который можно увидеть во многих продуктах. Использование альдегида в названии связано с его историей: альдегиды более реакционноспособны, чем кетоны, поэтому реакция с ними была открыта первой. [2] [3] [4]
Альдольная реакция является парадигмой органической химии и, возможно, наиболее распространенным способом образования углерод-углеродных связей в органической химии . [5] [6] [7] Он дал свое название семейству альдольных реакций , и аналогичные методы анализа целого семейства реакций карбонильного α-замещения , а также конденсации дикетона . Когда нуклеофил и электрофил различны, реакция называется скрещенной альдольной реакцией ; и наоборот, когда нуклеофил и электрофил одинаковы, реакция называется альдольной димеризацией .
Альдольные структурные единицы обнаружены во многих важных молекулах, как природных, так и синтетических. [8] [9] Реакция используется в нескольких промышленных синтезах, в частности пентаэритрита , [10] триметилолпропана , пластификатора 2-этилгексанола и препарата Липитор ( аторвастатин , кальциевая соль). [11] Для многих коммерческих применений стереохимия альдольной реакции не важна, но эта тема представляет большой интерес для синтеза многих специальных химических веществ.

Альдольная реакция имеет один основной механизм, но в зависимости от pH она проявляется в разных формах: [12]

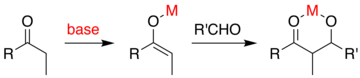
На первом этапе карбонильное соединение должно быть преобразовано в енол , обычно в виде эфира енола или енолята металла . Эти виды, нуклеофильные по α-углероду , могут атаковать другой реакционноспособный карбонил. Если катализатором является умеренное основание, такое как гидроксид- ион или алкоксид , альдольная реакция происходит посредством нуклеофильной атаки резонансно -стабилизированного енолята на карбонильную группу другой молекулы. Продукт представляет собой алкоксидную соль альдольного продукта. Затем образуется сам альдоль, который затем может подвергнуться дегидратации с образованием ненасыщенного карбонильного соединения. На схеме показан простой механизм катализируемой основаниями альдольной реакции альдегида с самим собой.

Хотя в некоторых случаях требуется только каталитическое количество основания, более обычной процедурой является использование стехиометрического количества сильного основания, такого как LDA или NaHMDS . В этом случае образование енолята является необратимым, и альдольный продукт не образуется до тех пор, пока алкоксид металла альдольного продукта не будет протонирован на отдельной стадии обработки.
При использовании кислотного катализатора начальная стадия механизма реакции включает катализируемую кислотой таутомеризацию карбонильного соединения в енол. Кислота также служит для активации карбонильной группы другой молекулы путем протонирования, что делает ее очень электрофильной. Енол является нуклеофильным по отношению к α-углероду, что позволяет ему атаковать протонированное карбонильное соединение, что приводит к образованию альдола после депротонирования . Некоторые из них могут также дегидратироваться помимо целевого продукта с образованием ненасыщенного карбонильного соединения посредством альдольной конденсации .

Несмотря на привлекательность альдольного многообразия, существует несколько проблем, которые необходимо решить, чтобы сделать процесс эффективным. Первая проблема носит термодинамический характер: большинство альдольных реакций обратимы. Кроме того, в случае простых альдегид-кетон-альдольных реакций равновесие также едва ли находится на стороне продуктов. [13] Если условия особенно суровые (например: NaOMe/MeOH/ рефлегмация ), может произойти конденсация, но этого обычно можно избежать с помощью мягких реагентов и низких температур (например, LDA (сильное основание), ТГФ, −78°). С). Хотя присоединение альдолов обычно происходит почти до завершения в необратимых условиях, изолированные альдольные аддукты чувствительны к индуцированному основанием расщеплению ретро-альдолов с возвратом исходных материалов. Напротив, ретро-альдольные конденсации редки, но возможны. [14] Это лежит в основе каталитической стратегии альдолаз класса I в природе, а также многочисленных низкомолекулярных аминных катализаторов. [15]
При реакции смеси несимметричных кетонов можно ожидать четыре продукта скрещенных альдолов ( присоединения ):

Таким образом, если кто-то желает получить только один из перекрестных продуктов, необходимо контролировать, какой карбонил становится нуклеофильным енолом/енолятом, а какой остается в своей электрофильной карбонильной форме. Самый простой контроль – это если только один из реагентов имеет кислые протоны и только эта молекула образует енолят. Например, при добавлении диэтилмалоната к бензальдегиду образуется только один продукт:

Если одна группа значительно более кислая, чем другая, наиболее кислый протон отрывается основанием, и на этом карбониле образуется енолят, в то время как менее кислый карбонил остается электрофильным. Этот тип контроля работает только в том случае, если разница в кислотности достаточно велика и основание является ограничивающим реагентом . Типичным субстратом для этой ситуации является ситуация, когда депротонируемое положение активируется более чем одной карбонильноподобной группой. Общие примеры включают группу CH 2 , фланкированную двумя карбонилами или нитрилами (см., например, конденсацию Кневенагеля и первые стадии синтеза малонового эфира и синтеза ацетоуксусного эфира ).
В противном случае наиболее кислые карбонилы обычно являются также и наиболее активными электрофилами: сначала альдегиды , затем кетоны , затем сложные эфиры и, наконец, амиды . Таким образом, реакции с перекрестными альдегидами обычно являются наиболее сложными, поскольку они могут легко полимеризоваться или реагировать неселективно, образуя статистическую смесь продуктов. [16]
Одним из распространенных решений является сначала образование енолята одного партнера, а затем добавление другого партнера под кинетическим контролем . [17] Кинетический контроль означает, что прямая реакция альдольного присоединения должна протекать значительно быстрее, чем обратная ретро-альдольная реакция. Для успеха этого подхода необходимо также выполнить два других условия; должна быть возможность количественно образовать енолят одного партнера, и прямая альдольная реакция должна быть значительно быстрее, чем передача енолята от одного партнера к другому. Обычные условия кинетического контроля включают образование енолята кетона с LDA при -78 ° C с последующим медленным добавлением альдегида.
Альдольная реакция объединяет две относительно простые молекулы в более сложную. Повышенная сложность возникает из-за того, что каждый конец новой связи может стать стереоцентром . Современная методология не только разработала высокопродуктивные альдольные реакции, но и полностью контролирует как относительную, так и абсолютную конфигурацию этих новых стереоцентров. [6]
Для описания относительной стереохимии α- и β-углеродов в старых статьях используется номенклатура эритро/трео химии сахаридов ; более современные статьи используют следующее соглашение син / анти . Когда пропионатные нуклеофилы (или нуклеофилы более высокого порядка) присоединяются к альдегидам, читатель визуализирует группу R кетона и группу R' альдегида, выстроенных в виде «зигзага» на бумаге (или экране). Расположение образовавшихся стереоцентров считается син- или анти -в зависимости от того, находятся ли они по одну или противоположные стороны основной цепи:
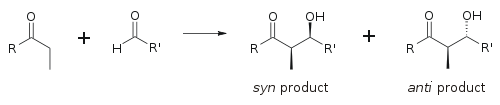
Основным фактором, определяющим стереоселективность альдольной реакции, является енолизирующий противоион металла . Более короткие связи металл-кислород «затягивают» переходное состояние и вызывают большую стереоселекцию. [18] Бор часто используется [19] [20] , поскольку длины его связей значительно короче, чем у других дешевых металлов ( лития , алюминия или магния ). Следующая реакция дает соотношение син:анти 80:20 при использовании енолята лития по сравнению с 97:3 при использовании енолята бибутилбора.

Если противоион определяет силу стереоиндукции , то енолят-изомер определяет ее направление . Изомеры E дают антипродукты , а Z - син : [21]


Если два реагента имеют карбонилы, соседние с ранее существовавшим стереоцентром, то новые стереоцентры могут образовываться с фиксированной ориентацией относительно старого . Этот «стереоконтроль на основе субстрата» широко изучался, и примеры изобилуют литературой. Во многих случаях стилизованное переходное состояние , называемое моделью Циммермана-Тракслера , может предсказать новую ориентацию на основе конфигурации 6-членного кольца . [22]
Если енол имеет соседний стереоцентр, то два стереоцентра, фланкирующие карбонил в продукте, всегда являются син : [23]

Однако основная механистическая причина зависит от изомера енола. Для енолята E стереоиндукция необходима, чтобы избежать 1,3- аллильного штамма , тогда как енолят Z вместо этого стремится избежать 1,3-диаксиальных взаимодействий: [24]

Еноляты E демонстрируют диастереофасную селекцию Фелкина , тогда как еноляты Z проявляют селективность против Фелкина. Общая модель представлена ниже: [25] [26]
Поскольку переходное состояние для енолятов Z должно содержать либо дестабилизирующее син -пентановое взаимодействие, либо анти-Фелькин -ротамер , Z -еноляты менее диастереоселективны: [27] [28]
Если и енолят, и альдегид содержат уже существующую хиральность, то результат альдольной реакции «двойного стереодифференцирования» можно предсказать с использованием объединенной стереохимической модели, которая учитывает все эффекты, обсуждавшиеся выше. [29] Вот несколько примеров: [28]
В конце 1970-х и 1980-х годах Дэвид А. Эванс и его коллеги разработали метод стереоселекции при альдольном синтезе альдегидов и карбоновых кислот . [30] [31] Этот метод работает путем временного добавления хирального вспомогательного оксазолидинона для создания хирального енолята. Ранее существовавшая хиральность вспомогательного вещества затем передается альдольному аддукту с помощью методов Циммермана-Тракслера, а затем оксазолидинон отщепляется.
Коммерческие оксазолидиноны относительно дороги, но их получают в два этапа синтеза из сравнительно недорогих аминокислот. (Экономичные крупномасштабные синтезы готовят вспомогательные вещества собственными силами.) Во-первых, боргидрид восстанавливает кислотную часть . Затем полученный аминоспирт дегидратационно циклизуется с простым эфиром карбоната, например диэтилкарбонатом.
Ацилирование оксазолидинона неофициально называют «загрузкой».
Антиаддукты , для которых требуется енолят Е , невозможно надежно получить методом Эванса. Однако еноляты Z , приводящие к синаддуктам , могут надежно образовываться с помощью бор-опосредованной мягкой енолизации: [32]
Часто один диастереомер можно получить путем одной кристаллизации альдольного аддукта.
Многие методы отщепляют вспомогательные: [33]
Обычным дополнительным киральным вспомогательным средством является тиоэфирная группа: [33] [34]
В тиазолидинетионовом подходе Кримминса [35] [36] тиазолидинетион является хиральным вспомогательным веществом [37] и может производить аддукты «син Эванса» или «син-не-Эванса», просто варьируя количество (-)-спартеина . Считается, что реакция протекает через шестичленные переходные состояния , связанные с титаном , аналогичные предполагаемым переходным состояниям для вспомогательного вещества Эванса.
В обычной модификации альдольной реакции используются другие функциональные группы, аналогичные эрзац- енолам. В альдольной реакции Мукаямы [ 38] эфиры силиленола присоединяются к карбонилам в присутствии катализатора кислоты Льюиса , такого как трифторид бора (в виде эфирата трифторида бора ) или тетрахлорид титана . [39] [40]
При енаминовом алкилировании по Сторку вторичные амины при воздействии кетонов образуют енамины . Эти енамины затем реагируют (возможно, энантиоселективно [ 41]) с подходящими электрофилами. Эта стратегия предлагает простой энантиоселектив без переходных металлов. В отличие от предпочтения синаддуктов , обычно наблюдаемого при присоединении альдолов на основе енолята, эти альдольные присоединения являются антиселективными .
В водном растворе енамин затем может быть гидролизован из продукта, что делает его катализатором на основе небольших органических молекул . Яркий пример: пролин эффективно катализирует циклизацию трикетона:
Эта комбинация представляет собой реакцию Хаджоса-Пэрриша [42] [43] [44] В условиях Хайоса-Пэрриша необходимо только каталитическое количество пролина (3 мол%). Нет опасности ахиральной фоновой реакции, поскольку временные промежуточные енаминовые соединения гораздо более нуклеофильны, чем их исходные кетоненолы.
Стратегия типа аиста также допускает сложные перекрестные реакции между двумя альдегидами. Во многих случаях условия достаточно мягкие, чтобы избежать полимеризации: [45]
Однако селективность требует медленного добавления желаемого электрофильного партнера, контролируемого шприцевым насосом, поскольку оба реагирующих партнера обычно имеют енолизируемые протоны. Если один альдегид не имеет енолизируемых протонов или альфа- или бета-разветвлений, можно достичь дополнительного контроля.
При обычном альдольном присоединении карбонильное соединение депротонируется с образованием енолята. Енолят добавляют к альдегиду или кетону, который образует алкоксид, который затем протонируется при обработке. В принципе, лучший метод позволил бы избежать необходимости многостадийной последовательности в пользу «прямой» реакции, которую можно было бы провести за одну стадию процесса.
Если один из партнеров сочетания предпочтительно енолизируется, то общая проблема заключается в том, что при добавлении образуется алкоксид, который гораздо более основной, чем исходные материалы. Этот продукт прочно связывается с енолизирующим агентом, не позволяя ему катализировать дополнительные реагенты:
Один из подходов, продемонстрированный Эвансом, заключается в силилировании альдольного аддукта. [46] [47] В реакцию добавляется кремниевый реагент, такой как TMSCl , который заменяет металл в алкоксиде, обеспечивая обмен металлического катализатора:
Элегантная демонстрация силы асимметричных органокаталитических альдольных реакций была раскрыта Макмилланом и его коллегами в 2004 году при синтезе дифференциально защищенных углеводов . В то время как традиционные синтетические методы осуществляют синтез гексоз с использованием вариаций итеративных стратегий снятия защиты , требующих 8–14 этапов, органокатализ может получить доступ ко многим из тех же субстратов, используя эффективный двухэтапный протокол, включающий катализируемую пролином димеризацию альфа-оксиальдегидов с последующей тандемной альдольной циклизацией Мукаямы.
Альдольная димеризация альфа-оксиальдегидов требует, чтобы альдольный аддукт, который сам является альдегидом, был инертным к дальнейшим альдольным реакциям. [48] Более ранние исследования показали, что альдегиды, содержащие альфа-алкилокси- или альфа- силилокси- заместители, подходят для этой реакции, в то время как альдегиды, содержащие электроноакцепторные группы, такие как ацетокси , нереакционноспособны. Защищенный продукт эритрозы затем можно было превратить в четыре возможных сахара путем добавления альдолов Мукаямы с последующим образованием лактола . Это требует соответствующего диастереоконтроля при присоединении альдолов Мукаямы и образовавшегося иона силилоксикарбения для предпочтительной циклизации, а не для дальнейшей альдольной реакции. В итоге были синтезированы глюкоза , манноза и аллоза :
Примеры альдольных реакций в биохимии включают расщепление фруктозо-1,6-бисфосфата на дигидроксиацетон и глицеральдегид-3-фосфат на четвертой стадии гликолиза , что является примером обратной («ретро») альдольной реакции, катализируемой ферментом. альдолаза А (также известная как фруктозо-1,6-бисфосфатальдолаза).
В глиоксилатном цикле растений и некоторых прокариот изоцитратлиаза образует из изоцитрата глиоксилат и сукцинат . После депротонирования ОН-группы изоцитратлиаза расщепляет изоцитрат на четырехуглеродный сукцинат и двухуглеродный глиоксилат посредством альдольной реакции расщепления. Это расщепление по механизму аналогично альдолазной реакции гликолиза.
Альдольная реакция была открыта независимо русским химиком (и композитором-романтиком) Александром Бородиным в 1869 году [49] и французским химиком Шарлем-Адольфом Вюрцем в 1872 году, который первоначально использовал для проведения реакции альдегиды. [2] [3] [4]
Говард Циммерман и Марджори Д. Трэкслер предложили свою модель стереоиндукции в статье 1957 года. [22]