
В химии оксид амина , также известный как амин- N -оксид или просто N -оксид , представляет собой химическое соединение , имеющее химическую формулу R 3 N + −O − . Он содержит ковалентную ковалентную связь азот - кислород с тремя дополнительными группами водорода и/или заместителя , присоединенными к азоту. Иногда его записывают как R 3 N→O или, альтернативно, [1] как R 3 N=O .
В строгом смысле термин оксид амина применяется только к оксидам третичных аминов . Иногда его также используют для аналогичных производных первичных и вторичных аминов.
Примеры оксидов аминов включают N -оксид пиридина , водорастворимое кристаллическое твердое вещество с температурой плавления 62–67 °C, и N -оксид N -метилморфолина , который является окислителем.
Оксиды аминов представляют собой поверхностно-активные вещества, обычно используемые в потребительских товарах, таких как шампуни, кондиционеры, моющие средства и средства для очистки твердых поверхностей. [2] Оксид алкилдиметиламина (длина цепи C10–C16) является наиболее коммерчески используемым оксидом амина. [3] Они считаются классом соединений с высоким объемом производства более чем в одной стране-члене Организации экономического сотрудничества и развития ( ОЭСР ); с годовым объемом производства более 26 000, 16 000 и 6 800 тонн (28 700, 17 600 и 7 500 коротких тонн) в США, Европе и Японии соответственно. [2] В Северной Америке более 95% оксидов аминов используются в чистящих средствах для дома. [4] Они служат стабилизаторами, загустителями, смягчающими средствами, эмульгаторами и кондиционерами с активными концентрациями в диапазоне 0,1–10%. [2] Остальная часть (< 5%) используется в средствах личной гигиены, в учреждениях, коммерческих продуктах [5] и для уникальных запатентованных целей, таких как фотография. [2]
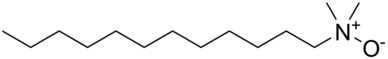
Оксиды аминов используются в качестве защитной группы для аминов и в качестве химических промежуточных продуктов. Длинноцепочечные алкиламинооксиды используются в качестве амфотерных поверхностно-активных веществ и стабилизаторов пены .
Оксиды аминов представляют собой высокополярные молекулы и имеют полярность , близкую к полярности четвертичных аммониевых солей . Малые оксиды аминов очень гидрофильны и обладают отличной растворимостью в воде и очень плохой растворимостью в большинстве органических растворителей .
Оксиды аминов представляют собой слабые основания с p K b около 4,5, которые образуют R 3 N + -OH , катионные гидроксиламины , при протонировании при pH ниже их p K b .
Почти все аминооксиды получают окислением либо третичных алифатических аминов, либо ароматических N - гетероциклов . Перекись водорода является наиболее распространенным реагентом как в промышленности, так и в научных кругах, однако перкислоты также важны. [6] Более специализированные окислители могут найти применение в своей нише, например, кислота Каро или м- CPBA . Спонтанные или катализируемые реакции с использованием молекулярного кислорода встречаются редко. Некоторые другие реакции также приводят к образованию оксидов аминов, например, элиминирование ретро-Коупа , однако они используются редко.
Оксиды аминов вступают в различные реакции. [7]
Оксиды аминов являются распространенными метаболитами лекарств и психоактивных веществ . Примеры включают никотин , золмитриптан и морфин .
Оксиды аминов противораковых препаратов были разработаны как пролекарства , которые метаболизируются в раковой ткани с дефицитом кислорода до активного лекарства.
Оксиды аминов (АО) не известны как канцерогены, кожные сенсибилизаторы или репродуктивные токсиканты. Они легко метаболизируются и выводятся из организма при приеме внутрь. При хроническом приеме внутрь кроликами наблюдалось снижение массы тела, диарея и помутнение хрусталика при самом низком наблюдаемом уровне побочных эффектов (LOAEL) в диапазоне 87–150 мг АО/кВт массы тела/день. Тесты воздействия на кожу человека показали, что через 8 часов в организм всасывается менее 1%. Раздражение глаз, вызванное оксидами аминов и другими поверхностно-активными веществами, является умеренным и временным, без длительных последствий. [2]
Было измерено, что оксиды аминов со средней длиной цепи 12,6 растворимы в воде при концентрации ~ 410 г/л. На основании данных log K ow для цепей с длиной менее C14 (коэффициент биоконцентрации <87%) считается, что они обладают низким потенциалом биоаккумуляции в водных видах. [2] Уровни АО в неочищенных сточных водах составляли 2,3–27,8 мкг/л, а в сточных водах – 0,4–2,91 мкг/л. Самые высокие концентрации сточных вод были обнаружены в окислительных канавах и очистных сооружениях с капельными фильтрами. В среднем удаление более 96% было обнаружено при вторичной обработке активным илом. [3] Острая токсичность для рыб, как показали 96-часовые тесты LC50, находится в диапазоне 1000–3000 мкг/л для углеродных цепей с длиной менее C14. Значения LC50 для цепей длиной более C14 варьируются от 600 до 1400 мкг/л. Данные о хронической токсичности для рыбы составляют 420 мкг/л. При нормализации к C12.9 NOEC составляет 310 мкг/л для роста и выводимости. [3]