Дефицит глюкозо-6-фосфатдегидрогеназы ( G6PDD ), который является наиболее распространенным дефицитом фермента во всем мире, [5] представляет собой врожденную ошибку метаболизма , которая предрасполагает к распаду эритроцитов . [1] В большинстве случаев у заболевших симптомы отсутствуют. [3] Вслед за конкретным триггером могут развиться такие симптомы, как желтоватая кожа , темная моча, одышка и чувство усталости. [1] [2] Осложнения могут включать анемию и желтуху новорожденных . [2] У некоторых людей симптомы никогда не проявляются. [3]
Это Х-сцепленное рецессивное заболевание, которое приводит к дефекту фермента глюкозо-6-фосфатдегидрогеназы . [1] Глюкозо-6-фосфатдегидрогеназа — это фермент, который защищает эритроциты, которые переносят кислород из легких в ткани по всему организму. Дефект фермента приводит к преждевременному разрушению эритроцитов. Такое разрушение эритроцитов называется гемолизом . [6] Распад эритроцитов может быть вызван инфекциями , некоторыми лекарствами, стрессом или такими продуктами, как фасоль . [1] [3] В зависимости от конкретной мутации тяжесть состояния может варьироваться. [2] Диагноз ставится на основании симптомов и подтверждается анализами крови и генетическим тестированием . [2]
Пострадавшим людям следует избегать пищевых триггеров, [3] особенно фасоли. [7] Это может быть сложно, так как конские бобы можно назвать «бобы», и они используются во многих продуктах питания, целиком или в виде муки. Фалафель , вероятно, самый известный, но фасоль также часто используется в качестве наполнителя в фрикадельках и других продуктах. Поскольку дефицит G6PD не является аллергией, правила в отношении пищевых продуктов в большинстве стран не требуют, чтобы фасоль была указана на этикетке как аллерген. [ нужна цитата ]
Лечение острых эпизодов может включать в себя прием противоинфекционных препаратов, прекращение приема вызывающих заболевание лекарств или переливание крови . [3] Желтуха у новорожденных можно лечить с помощью желчных ламп . [2] Людям рекомендуется пройти тестирование на G6PDD перед приемом определенных лекарств, таких как примахин . [2]
Во всем мире этим заболеванием страдают около 400 миллионов человек. [1] Это особенно распространено в некоторых частях Африки, Азии, Средиземноморья и Ближнего Востока . [1] Мужчины болеют чаще, чем женщины. [1] Считается, что в 2015 году от него погибло 33 000 человек. [4]
У большинства людей с дефицитом G6PD симптомы отсутствуют . [ нужна цитата ]
Большинство людей, у которых развиваются симптомы, — мужчины из-за Х-сцепленного типа наследования, но женщины-носители могут пострадать из-за неблагоприятной лионизации или искаженной Х-инактивации , когда случайная инактивация Х-хромосомы в определенных клетках создает популяцию G6PD. -дефицитные эритроциты сосуществуют с непораженными эритроцитами. У женщины с одной пораженной Х-хромосомой будет наблюдаться дефицит примерно половины ее эритроцитов. Однако в некоторых случаях, в том числе при двойном Х-дефиците, это соотношение может быть намного больше половины, что делает человека почти таким же чувствительным, как и мужчины. [ нужна цитата ]
Распад эритроцитов (также известный как гемолиз ) при дефиците G6PD может проявляться по-разному, в том числе следующим :
Фавизм — это гемолитическая реакция на употребление конских бобов, также известных как бобы. Хотя у всех людей с фавизмом наблюдается дефицит G6PD, не у всех людей с дефицитом G6PD наблюдается фавизм. Известно, что это заболевание чаще встречается у младенцев и детей, а генетический вариант G6PD может влиять на химическую чувствительность. [8] Помимо этого, особенности химической связи между фавизмом и G6PD недостаточно изучены. [ нужна цитата ]
Дефицит G6PD возникает в результате мутаций гена G6PD. Ген G6PD способствует выработке глюкозо-6-фосфатдегидрогеназы . Химические реакции с участием глюкозо-6-фосфатдегидрогеназы производят соединения, которые предотвращают накопление активных форм кислорода до токсичных уровней в эритроцитах. Если вследствие мутации гена G6PD происходит снижение количества глюкозо-6-фосфатдегидрогеназы или изменение структуры, фермент теряет свою защитную роль и приводит к накоплению активных форм кислорода и, следовательно, повреждению эритроцитов. [6]
У носителей основной мутации не проявляются никакие симптомы, если их эритроциты не подвергаются воздействию определенных триггеров, которые могут быть четырех основных типов:
Многие вещества потенциально вредны для людей с дефицитом G6PD. Вариации реакции на эти вещества затрудняют индивидуальные прогнозы. Противомалярийные препараты , которые могут вызвать острый гемолиз у людей с дефицитом G6PD, включают примахин , памахин , хлорохин и гидроксихлорохин . [11] Имеются данные о том, что другие противомалярийные препараты также могут усугублять дефицит Г6ФД, но только в более высоких дозах. Людям с дефицитом G6PD также следует избегать приема сульфонамидов (таких как сульфаниламид , сульфаметоксазол и мафенид ), тиазолсульфона, метиленового синего и нафталина , поскольку они противодействуют синтезу фолатов, а также некоторых анальгетиков (таких как феназопиридин и ацетанилид ) и некоторых не- сульфаниламидные антибиотики ( налидиксовая кислота , нитрофурантоин , изониазид , дапсон и фуразолидон ). [12] [13] [14] Известно, что хна вызывает гемолитический криз у младенцев с дефицитом G6PD. [15] Расбуриказа также противопоказана при дефиците G6PD. Также известно, что высокие дозы внутривенного витамина С вызывают гемолиз у носителей дефицита G6PD; [16] [17] поэтому тестирование на дефицит G6PD является рутинным перед инфузией доз 25 г или более.
Два варианта (G6PD A- и G6PD Mediterranean) наиболее распространены в человеческих популяциях. G6PD A- встречается у 10% африканцев и афроамериканцев, тогда как средиземноморский G6PD распространен на Ближнем Востоке. Известное распространение мутировавшего аллеля в основном ограничивается людьми средиземноморского происхождения (испанцы, итальянцы, греки, армяне, евреи-сефарды и другие семитские народы). [18] Считается, что оба варианта обладают сильным защитным действием против малярии Plasmodium falciparum и Plasmodium vivax . [19] Это особенно часто встречается среди курдского еврейского населения, где примерно каждый второй мужчина страдает этим заболеванием, и такое же количество женщин являются носителями. [10] Это также распространено у афроамериканцев , саудовцев , сардинцев , некоторых африканских групп населения и азиатских групп. [10]
Все мутации, вызывающие дефицит G6PD, обнаруживаются на длинном плече Х-хромосомы , в полосе Xq28. Ген G6PD охватывает около 18,5 тысяч оснований . [13] Хорошо известны и описаны следующие варианты и мутации:
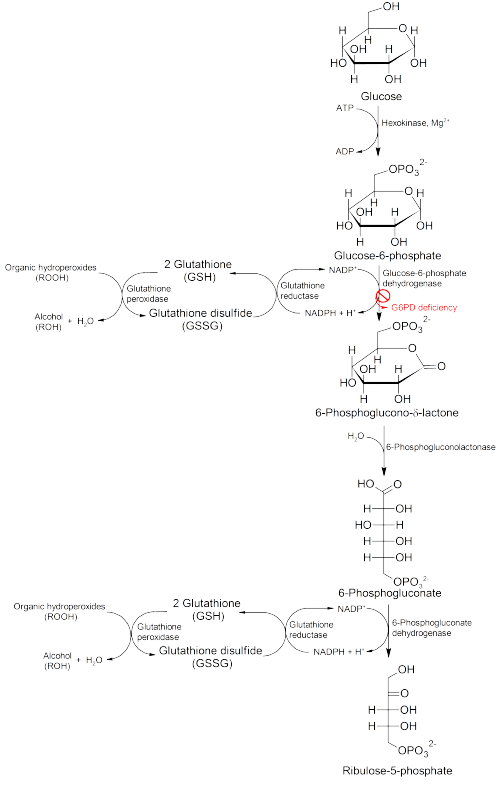
Глюкозо-6-фосфатдегидрогеназа (G6PD) представляет собой фермент пентозофосфатного пути (см. изображение, также известного как шунтирующий путь HMP). G6PD превращает глюкозо-6-фосфат в 6-фосфоглюконо-δ-лактон и является ферментом, лимитирующим скорость этого метаболического пути , который поставляет восстанавливающую энергию клеткам, поддерживая уровень восстановленной формы кофермента никотинамидадениндинуклеотидфосфата ( НАДФН). НАДФН поддерживает запасы восстановленного глутатиона в клетках, который используется для уничтожения свободных радикалов, вызывающих окислительное повреждение. Этот путь также стимулирует каталазу, антиоксидантный фермент. [20]
Путь G6PD/NADPH является единственным источником восстановленного глутатиона в красных кровяных тельцах ( эритроцитах ). Роль эритроцитов как переносчиков кислорода подвергает их существенному риску повреждения окисляющими свободными радикалами, за исключением защитного эффекта G6PD/NADPH/глутатиона. [20]
Таким образом, люди с дефицитом G6PD подвергаются риску гемолитической анемии в состоянии окислительного стресса . Окислительный стресс может возникнуть в результате инфекции, а также химического воздействия лекарств и некоторых продуктов питания. Кормовые бобы , например фасоль, содержат высокие уровни вицина , дивицина , конвицина и изоурамила , которые создают окислители . [21]
Когда весь оставшийся восстановленный глутатион расходуется, ферменты и другие белки (включая гемоглобин ) впоследствии повреждаются окислителями, что приводит к образованию поперечных связей и отложению белка в мембранах эритроцитов . Поврежденные эритроциты фагоцитируются и секвестрируются (выводятся из кровообращения) в селезенке . Гемоглобин метаболизируется до билирубина (при высоких концентрациях вызывая желтуху ). Эритроциты редко распадаются в кровотоке, поэтому гемоглобин редко выводится непосредственно почками , но в тяжелых случаях это может произойти, вызывая острое повреждение почек . [ нужна цитата ]
Дефицит G6PD в альтернативном пути вызывает накопление глюкозы и, следовательно, увеличение количества конечных продуктов гликирования (AGE). Дефицит также снижает количество НАДФН, необходимого для образования оксида азота (NO). Высокая распространенность сахарного диабета 2 типа и гипертонии среди афро-карибских жителей Запада может быть напрямую связана с частотой дефицита Г6ФД в этих группах населения. [22]
Хотя женщины-носители могут иметь легкую форму дефицита G6PD (в зависимости от степени инактивации непораженной Х-хромосомы – см. « Асимметричная Х-инактивация »), были описаны гомозиготные женщины; у этих женщин одновременно встречается редкое иммунное заболевание , называемое хронической гранулематозной болезнью (ХГБ). [ нужна цитата ]
Диагноз обычно подозревают, когда у пациентов определенных этнических групп (см. эпидемиологию) после проявления любой из вышеперечисленных причин развивается анемия , желтуха и симптомы гемолиза , особенно при наличии положительного семейного анамнеза. [23]
Как правило, тесты включают в себя: [ нужна ссылка ]
Когда есть достаточные основания подозревать G6PD, прямым тестом на G6PD является « тест флуоресцентного пятна Бейтлера », который в значительной степени заменил более старый тест (тест на обесцвечивание красителем Мотульского). Другими возможностями являются прямое тестирование ДНК и/или секвенирование гена G6PD. [24]
Флуоресцентный точечный тест Бейтлера — это быстрый и недорогой тест, который визуально идентифицирует НАДФН, вырабатываемый G6PD, в ультрафиолетовом свете . Если пятно крови не флуоресцирует, тест положительный; он может быть ложноотрицательным у пациентов с активным гемолизом. Поэтому это можно сделать только через 2–3 недели после гемолитического эпизода. [23]
Когда макрофаг в селезенке идентифицирует эритроцит с тельцем Гейнца, он удаляет осадок и небольшой кусочек мембраны, что приводит к образованию характерных « укусных клеток ». Однако если образуется большое количество телец Гейнца, как в случае дефицита G6PD, некоторые тельца Гейнца, тем не менее, будут видны при просмотре эритроцитов, окрашенных кристаллическим фиолетовым. Этот простой и недорогой тест может привести к первоначальному предположению о дефиците Г6ФД, который можно подтвердить с помощью других тестов. [ нужна цитата ]
Тестирование во время и в течение многих недель после гемолитического эпизода приведет к ложноотрицательным результатам, поскольку эритроциты с дефицитом G6PD будут выделены, а молодые эритроциты (ретикулоциты) еще не будут иметь дефицита G6PD. Ложноотрицательные результаты также вероятны после любого переливания крови. По этой причине во многих больницах после эпизода гемолитика выжидают 3 месяца, прежде чем проводить тестирование на дефицит Г6ФД. У женщин следует измерять активность G6PD с помощью количественного анализа, чтобы избежать неправильной классификации в ходе скрининговых тестов. [23]
Всемирная организация здравоохранения классифицирует генетические варианты G6PD на пять классов, первые три из которых являются состояниями дефицита. [25]
Дефицит 6-фосфоглюконатдегидрогеназы (6PGD) имеет схожие симптомы и часто ошибочно принимается за дефицит G6PD, поскольку пораженный фермент находится в одном и том же пути, однако эти заболевания не связаны между собой и могут быть обнаружены у одного и того же человека. [ нужна цитата ]
Самой важной мерой является профилактика – отказ от лекарств и продуктов, вызывающих гемолиз. Вакцинация против некоторых распространенных патогенов (например, гепатита А и гепатита В ) может предотвратить приступы, вызванные инфекцией. [26]
В острой фазе гемолиза может потребоваться переливание крови или даже диализ при острой почечной недостаточности . Переливание крови является важной симптоматической мерой, поскольку перелитые эритроциты, как правило, не имеют дефицита G6PD и живут в кровотоке реципиента в течение нормальной продолжительности жизни. Пострадавшим следует избегать приема таких препаратов, как аспирин . [ нужна цитата ]
Некоторым пациентам может помочь удаление селезенки ( спленэктомия ) [ 27] , поскольку это важный участок разрушения эритроцитов. Фолиевую кислоту следует использовать при любом заболевании, характеризующемся высоким оборотом эритроцитов. Хотя витамин Е и селен обладают антиоксидантными свойствами, их применение не уменьшает выраженность дефицита Г6ФД. [ нужна цитата ]
Было показано, что AG1, недавно обнаруженная небольшая молекула, увеличивает активность фермента G6PD при трех распространенных вариантах дефицита. Из-за отсутствия лекарств для лечения G6PD, AG1 является многообещающим предшественником в разработке фармакологического лечения, эффективного при множественных ферментопатиях G6PD. [28]
Лица с дефицитом Г6ФД, по-видимому, не заболевают какими-либо заболеваниями чаще, чем другие люди, и могут иметь меньший риск, чем другие люди, для приобретения ишемической болезни сердца и цереброваскулярных заболеваний . [29] Однако недавнее исследование показало, что дефицит G6PD увеличивает риск сердечно-сосудистых заболеваний до 70%. Риск, связанный с дефицитом G6PD, является умеренным по сравнению с воздействием первичных сердечно-сосудистых факторов риска. [30] Кроме того, в опубликованном обзоре выдвинута гипотеза о том, что дефицит G6PD может снизить антиагрегантную эффективность клопидогрела (резистентность к клопидогрелю). [31]
Дефицит G6PD является вторым наиболее распространенным дефектом ферментов человека после дефицита ALDH2 , он присутствует у более чем 400 миллионов человек во всем мире. [32] Дефицит G6PD привел к 4100 смертям в 2013 году и 3400 смертям в 1990 году . [33] Средиземноморский бассейн — это место, где фавизм наиболее распространен, особенно среди евреев-мизрахи , сардинцев , киприотов , греков , египтян и некоторых африканских групп населения, в том числе у кого есть эти предки. [34] [35] [36] Фавизм также был зарегистрирован за пределами Средиземноморского бассейна, в других странах Ближнего Востока и Восточной Азии, таких как Ирак, Иран, Болгария и Китай. На Сардинии зарегистрирована самая высокая частота фавизма: пять случаев на каждую 1000 человек. [34]
Побочным эффектом этого заболевания является то, что оно обеспечивает защиту от малярии , [37] в частности от формы малярии, вызываемой Plasmodium falciparum , самой смертельной формы малярии. Аналогичная связь существует между малярией и серповидноклеточной анемией . Одна из теорий, объясняющая это, заключается в том, что клетки, инфицированные паразитом Plasmodium , быстрее выводятся из организма селезенкой . Это явление может дать носителям дефицита G6PD эволюционное преимущество за счет повышения их приспособленности к эндемичным по малярии средам. Исследования in vitro показали, что Plasmodium falciparum очень чувствителен к окислительному повреждению. Это является основой для другой теории, которая заключается в том, что генетический дефект придает устойчивость из-за того, что хозяин с дефицитом G6PD имеет более высокий уровень окислительных агентов, которые, хотя обычно переносятся хозяином, смертельны для паразита. [38]
Современное понимание этого состояния началось с анализа пациентов, у которых была чувствительность к примахину . [39] Открытие дефицита G6PD во многом основывалось на тестировании заключенных-добровольцев в тюрьме штата Иллинойс , тип исследования, которое сегодня считается неэтичным и не может быть выполнено. Когда некоторым заключенным давали препарат примахин, у некоторых развилась гемолитическая анемия , а у других – нет. Несмотря на эти результаты, американские военные широко применяли этот препарат во время Корейской войны, чтобы предотвратить рецидив инфекции, вызванной гипнозоитами Plasmodium vivax . Многочисленные случаи гемолитической анемии наблюдались у американских солдат североафриканского и средиземноморского происхождения. [40]
После изучения механизма с помощью тестирования Cr 51 было убедительно показано, что гемолитический эффект примахина обусловлен внутренним дефектом эритроцитов. [41]
И в легендах, и в мифологии фавизм известен с древности. Жрецам различных культов греко-римской эпохи запрещалось есть или даже упоминать бобы, а у Пифагора было строгое правило: чтобы вступить в общество пифагорейцев, нужно было отказаться от бобов. [42] Этот запрет предположительно был вызван тем, что бобы напоминали мужские гениталии, но возможно, что это произошло из-за убеждения, что бобы и люди были созданы из одного и того же материала. [43]