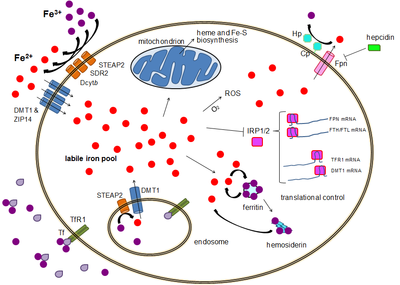
Метаболизм железа у человека представляет собой совокупность химических реакций, которые поддерживают гомеостаз железа у человека на системном и клеточном уровне. Железо одновременно необходимо организму и потенциально токсично. Контроль уровня железа в организме является критически важной частью многих аспектов здоровья и болезней человека. Гематологов особенно интересовал системный метаболизм железа , поскольку железо необходимо для эритроцитов , в которых содержится большая часть железа в организме человека. Понимание метаболизма железа также важно для понимания заболеваний, связанных с перегрузкой железом , таких как наследственный гемохроматоз , и дефицита железа , таких как железодефицитная анемия .

Железо является важным биоэлементом для большинства форм жизни, от бактерий до млекопитающих . Его важность заключается в его способности опосредовать перенос электронов. В двухвалентном состоянии (Fe 2+ ) железо выступает в роли донора электронов , а в трехвалентном состоянии (Fe 3+ ) — в качестве акцептора . Таким образом, железо играет жизненно важную роль в катализе ферментативных реакций, связанных с переносом электрона (восстановление и окисление, окислительно-восстановительный процесс ). Белки могут содержать железо в составе различных кофакторов , таких как железо-серные кластеры (Fe-S) и гемовые группы, которые собираются в митохондриях .
Человеческие клетки нуждаются в железе для получения энергии в виде АТФ в многоэтапном процессе, известном как клеточное дыхание, а точнее, в результате окислительного фосфорилирования в митохондриальных кристах . Железо присутствует в железо-серном кластере и гемовых группах белков цепи переноса электронов , которые генерируют протонный градиент , позволяющий АТФ-синтазе синтезировать АТФ ( хемиосмос ).
Гемовые группы входят в состав гемоглобина — белка, содержащегося в эритроцитах, который служит для транспортировки кислорода из легких в другие ткани. Гемовые группы также присутствуют в миоглобине для хранения и диффузии кислорода в мышечных клетках.
Человеческому организму железо необходимо для транспортировки кислорода. Кислород (O 2 ) необходим для функционирования и выживания почти всех типов клеток. Кислород транспортируется из легких в остальную часть тела, связанный с гемовой группой гемоглобина в эритроцитах. В мышечных клетках железо связывает кислород с миоглобином , который регулирует его высвобождение.
Железо также потенциально токсично. Его способность отдавать и принимать электроны означает, что он может катализировать превращение перекиси водорода в свободные радикалы . Свободные радикалы могут вызвать повреждение самых разных клеточных структур и в конечном итоге убить клетку. [1]
Железо, связанное с белками или кофакторами , такими как гем , безопасно. Также в клетке практически нет по-настоящему свободных ионов железа, поскольку они легко образуют комплексы с органическими молекулами. Однако некоторая часть внутриклеточного железа связана с комплексами с низким сродством и называется лабильным железом или «свободным» железом. Железо в таких комплексах может вызвать описанные выше повреждения. [2]
Чтобы предотвратить такого рода повреждения, все формы жизни, использующие железо, связывают атомы железа с белками . Это связывание позволяет клеткам получать пользу от железа, одновременно ограничивая его способность причинять вред. [1] [3] Типичные внутриклеточные концентрации лабильного железа у бактерий составляют 10-20 микромолярей, [4] хотя они могут быть в 10 раз выше в анаэробной среде, [5] где свободных радикалов и активных форм кислорода меньше. В клетках млекопитающих внутриклеточные концентрации лабильного железа обычно составляют менее 1 микромоляря, что составляет менее 5 процентов от общего количества клеточного железа. [2]

В ответ на системную бактериальную инфекцию иммунная система инициирует процесс, известный как «удержание железа». Если бактерии хотят выжить, им необходимо получать железо из окружающей среды. Болезнетворные бактерии делают это разными способами, в том числе высвобождают связывающие железо молекулы, называемые сидерофорами , а затем реабсорбируют их для восстановления железа или удаляют железо из гемоглобина и трансферрина . Чем усерднее бактериям приходится работать, чтобы получить железо, тем большую метаболическую цену им приходится платить. Это означает, что бактерии, лишенные железа, размножаются медленнее. Таким образом, контроль уровня железа является важной защитой от многих бактериальных инфекций. Некоторые виды бактерий разработали стратегии, позволяющие обойти эту защиту. Бактерии, вызывающие туберкулез , могут обитать в макрофагах , которые представляют собой среду, богатую железом, а Borrelia burgdorferi использует марганец вместо железа. Люди с повышенным количеством железа, как, например, при гемохроматозе, более восприимчивы к некоторым бактериальным инфекциям. [6]
Хотя этот механизм является элегантным ответом на кратковременную бактериальную инфекцию, он может вызвать проблемы, если длится так долго, что организм лишается железа, необходимого для производства эритроцитов. Воспалительные цитокины стимулируют печень вырабатывать белок-регулятор метаболизма железа гепсидин , который снижает доступность железа. Если уровни гепсидина повышаются из-за небактериальных источников воспаления, таких как вирусная инфекция, рак, аутоиммунные заболевания или другие хронические заболевания, то может возникнуть анемия хронического заболевания . В этом случае отказ от железа фактически ухудшает здоровье, препятствуя выработке достаточного количества эритроцитов, содержащих гемоглобин. [3]

Большинство хорошо питающихся людей в промышленно развитых странах имеют в организме от 4 до 5 граммов железа (~38 мг железа на кг массы тела у женщин и ~50 мг железа на кг массы тела у мужчин). [7] Об этом, по поводуВ гемоглобине, необходимом для переноса кислорода через кровь, содержится 2,5 г (около 0,5 мг железа на мл крови) [8] и большая часть остального (около 2 г у взрослых мужчин и несколько меньше у женщин детородного возраста). ) содержится в комплексах ферритина , которые присутствуют во всех клетках, но наиболее часто встречаются в костном мозге, печени и селезенке . Запасы ферритина в печени являются основным физиологическим источником резервного железа в организме. Запасы железа в промышленно развитых странах, как правило, ниже у детей и женщин детородного возраста, чем у мужчин и пожилых людей. Женщины, которым приходится использовать свои запасы железа для компенсации потери железа во время менструации , беременности или лактации , имеют более низкие запасы негемоглобина в организме, которые могут состоять из500 мг или даже меньше.
Из общего содержания железа в организме около400 мг посвящено клеточным белкам, которые используют железо для важных клеточных процессов, таких как хранение кислорода (миоглобин) или выполнение окислительно-восстановительных реакций, производящих энергию ( цитохромы ). Относительно небольшое количество (3–4 мг) циркулирует в плазме , связанное с трансферрином. [9] Из-за своей токсичности свободное растворимое железо сохраняется в организме в низкой концентрации.
Дефицит железа в первую очередь влияет на запасы железа в организме, и считается, что истощение этих запасов протекает относительно бессимптомно, хотя с ним связаны некоторые неопределенные и неспецифические симптомы . Поскольку железо в первую очередь необходимо для гемоглобина, железодефицитная анемия является основным клиническим проявлением дефицита железа. Люди с дефицитом железа страдают или умирают от повреждения органов задолго до того, как в их клетках закончится железо, необходимое для внутриклеточных процессов, таких как транспорт электронов.
Макрофаги ретикулоэндотелиальной системы накапливают железо в процессе расщепления и переработки гемоглобина из поглощенных эритроцитов. Железо также хранится в виде пигмента, называемого гемосидерином , который представляет собой нечеткое отложение белка и железа, создаваемое макрофагами, где присутствует избыток железа, локально или системно, например, у людей с перегрузкой железом из-за частого разрушения клеток крови и необходимые переливания крови, которых требует их состояние. Если корригировать системную перегрузку железом, со временем гемосидерин медленно резорбируется макрофагами.
Гомеостаз железа у человека регулируется на двух разных уровнях. Системный уровень железа уравновешивается контролируемым поглощением пищевого железа энтероцитами , клетками, выстилающими внутреннюю часть кишечника , а также неконтролируемой потерей железа в результате отслаивания эпителия, пота, травм и кровопотери. Кроме того, системное железо постоянно перерабатывается. Уровни клеточного железа по-разному контролируются разными типами клеток из-за экспрессии определенных регуляторных и транспортных белков железа.

Всасывание пищевого железа представляет собой переменный и динамичный процесс. Количество абсорбированного железа по сравнению с количеством потребляемого железа обычно невелико, но может варьироваться от 5% до 35% в зависимости от обстоятельств и типа железа. Эффективность поглощения железа варьируется в зависимости от источника. Как правило, лучше всего усваиваемые формы железа поступают из продуктов животного происхождения. Усвоение пищевого железа в форме солей железа (как и в большинстве добавок) несколько варьируется в зависимости от потребности организма в железе и обычно составляет от 10% до 20% потребления железа. Всасывание железа из продуктов животного происхождения и некоторых растительных продуктов происходит в форме гемового железа и является более эффективным, позволяя усваивать от 15% до 35% принятого количества. Гемовое железо у животных поступает из крови и гемсодержащих белков мяса и митохондрий, тогда как у растений гемовое железо присутствует в митохондриях всех клеток, использующих кислород для дыхания.
Как и большинство минеральных питательных веществ, большая часть железа, всасываемого из переваренной пищи или добавок, всасывается в двенадцатиперстной кишке энтероцитами слизистой оболочки двенадцатиперстной кишки. Эти клетки имеют специальные молекулы, которые позволяют им переносить железо в организм. Чтобы абсорбироваться, пищевое железо может усваиваться как часть белка, такого как гем-белок, или железо должно находиться в форме двухвалентного железа Fe 2+ . Фермент редуктаза железа на щеточной кайме энтероцитов , дуоденальный цитохром B ( Dcytb ), восстанавливает железо Fe 3+ до Fe 2+ . [10] Белок, называемый переносчиком двухвалентных металлов 1 ( DMT1 ), который может транспортировать несколько двухвалентных металлов через плазматическую мембрану, а затем транспортировать железо через клеточную мембрану энтероцита в клетку. Если железо связано с гемом, вместо этого оно транспортируется через апикальную мембрану белком-переносчиком гема 1 (HCP1). [11] Гем затем катаболизируется микросомальной гемоксигеназой в биливердин , высвобождая Fe 2+ . [12]
Клетки слизистой оболочки кишечника затем могут либо хранить железо в виде ферритина , что достигается за счет связывания Fe 2+ с апоферритином (в этом случае железо покидает организм, когда клетка умирает и выделяется с калом ), либо клетка может высвободить железо. он попадает в организм через единственный известный экспортер железа у млекопитающих — ферропортин . Гефестин , ферроксидаза , которая может окислять Fe 2+ до Fe 3+ и обнаруживается главным образом в тонком кишечнике, помогает ферропортину переносить железо через базолатеральный конец клеток кишечника. При попадании в кровоток Fe 3+ связывает трансферрин и циркулирует в тканях. Напротив, ферропортин посттрансляционно репрессируется гепсидином , пептидным гормоном, состоящим из 25 аминокислот. Организм регулирует уровень железа, регулируя каждый из этих этапов. Например, энтероциты синтезируют больше Dcytb, DMT1 и ферропортина в ответ на железодефицитную анемию. [13] Всасывание железа из рациона увеличивается в присутствии витамина С и снижается при избытке кальция, цинка или марганца. [14]
Скорость всасывания железа в организме человека, по-видимому, зависит от множества взаимозависимых факторов, включая общие запасы железа, степень выработки костным мозгом новых эритроцитов, концентрацию гемоглобина в крови и содержание кислорода в крови. кровь. Организм также поглощает меньше железа во время воспаления , чтобы лишить бактерии железа. Недавние открытия показывают, что гепсидиновая регуляция ферропортина ответственна за синдром анемии хронических заболеваний.
Большая часть железа в организме накапливается и перерабатывается ретикулоэндотелиальной системой, которая разрушает старые эритроциты. В отличие от поглощения и рециркуляции железа, физиологического механизма регуляции выведения железа не существует . Люди теряют небольшое, но постоянное количество из-за кровопотери в желудочно-кишечном тракте, потоотделения и отшелушивания клеток кожи и слизистой оболочки желудочно-кишечного тракта . Общий объем потерь для здоровых людей в развитых странах составляет в среднем около1 мг в день для мужчин и 1,5–2 мг в день для женщин с регулярными менструациями. [15] Люди с желудочно-кишечными паразитарными инфекциями, чаще встречающимися в развивающихся странах, часто теряют больше. [1] Те, кто не может достаточно хорошо регулировать всасывание, страдают от перегрузки железом. При этих заболеваниях токсичность железа начинает подавлять способность организма связывать и хранить его. [16]
Большинство типов клеток поглощают железо в основном посредством рецептор-опосредованного эндоцитоза через рецептор трансферрина 1 (TFR1), рецептор трансферрина 2 (TFR2) и GAPDH . TFR1 имеет в 30 раз более высокое сродство к железу, связанному с трансферрином, чем TFR2, и, таким образом, является основным игроком в этом процессе. [17] [18] Многофункциональный гликолитический фермент высшего порядка глицеральдегид-3-фосфатдегидрогеназа (ГАФДГ) также действует как рецептор трансферрина. [19] [20] Связанное с трансферрином трехвалентное железо распознается этими рецепторами трансферрина, вызывая конформационные изменения, которые вызывают эндоцитоз. Затем железо поступает в цитоплазму из эндосомы через импортер DMT1 после восстановления до двухвалентного состояния редуктазой семейства STEAP. [21]
Альтернативно, железо может проникать в клетку напрямую через импортеры двухвалентных катионов плазматической мембраны, такие как DMT1 и ZIP14 (Zrt-Irt-подобный белок 14). [22] Опять же, железо попадает в цитоплазму в двухвалентном состоянии после восстановления во внеклеточном пространстве редуктазой, такой как STEAP2, STEAP3 (в эритроцитах), Dcytb (в энтероцитах) и SDR2. [21]
Железо также может проникать в клетки через CD44 в комплексах, связанных с гиалуроновой кислотой во время эпителиально-мезенхимального перехода (ЕМТ). В этом процессе эпителиальные клетки трансформируются в мезенхимальные клетки с отрывом от базальной мембраны , к которой они обычно прикреплены, открывая путь для вновь дифференцированных подвижных мезенхимальных клеток, чтобы начать миграцию от эпителиального слоя. [23] [24]
Хотя ЕМТ играет решающую роль в физиологических процессах, таких как имплантация , когда она позволяет эмбриону проникать в эндометрий , чтобы облегчить прикрепление плаценты , ее нарушение регуляции также может способствовать распространению злокачественных опухолей , позволяя им проникать в окружающие ткани и образовывать отдаленные колонии ( метастазирование ). [24]
Злокачественные клетки часто демонстрируют повышенную потребность в железе, что способствует их переходу в более инвазивное мезенхимальное состояние. Это железо необходимо для экспрессии мезенхимальных генов, например тех, которые кодируют трансформирующий фактор роста бета (TGF-β), имеющий решающее значение для ЕМТ. Примечательно, что уникальная способность железа катализировать деметилирование белков и ДНК играет жизненно важную роль в этом процессе экспрессии генов. [23]
Обычные пути поглощения железа, например, использующие рецептор трансферрина 1 (TfR1), часто оказываются недостаточными для удовлетворения повышенных потребностей в железе в раковых клетках. В результате различные цитокины и факторы роста вызывают активацию CD44, поверхностной молекулы, способной усваивать железо, связанное с гиалуронановым комплексом. Этот альтернативный путь, основанный на CD44-опосредованном эндоцитозе, становится доминирующим механизмом поглощения железа по сравнению с традиционным TfR1-зависимым путем. [23] [24]
В цитоплазме двухвалентное железо находится в растворимом, хелатируемом состоянии, которое составляет пул лабильного железа (~0,001 мМ). [25] Считается, что в этом пуле железо связано с соединениями малой массы, такими как пептиды, карбоксилаты и фосфаты, хотя некоторые из них могут находиться в свободной гидратированной форме ( аква-ионы ). [25] Альтернативно, ионы железа могут быть связаны со специализированными белками, известными как металлочапероны . [26] В частности, поли-r(C)-связывающие белки PCBP1 и PCBP2 , по-видимому, опосредуют перенос свободного железа в ферритин (для хранения) и негемовые ферменты железа (для использования в катализе). [22] [27] Пул лабильного железа потенциально токсичен из-за способности железа генерировать активные формы кислорода. Железо из этого пула может поглощаться митохондриями через митоферрин для синтеза кластеров Fe-S и гемовых групп. [21]
Железо может храниться в ферритине в виде трехвалентного железа благодаря ферроксидазной активности тяжелой цепи ферритина. [28] Дисфункциональный ферритин может накапливаться в виде гемосидерина , что может быть проблематичным в случаях перегрузки железом. [29] Резервный пул железа ферритина намного больше, чем пул лабильного железа, и его концентрация варьируется от 0,7 до 3,6 мМ. [25]
Экспорт железа происходит в различных типах клеток, включая нейроны , эритроциты, макрофаги и энтероциты. Последние два особенно важны, поскольку от них зависит системный уровень железа. Существует только один известный экспортер железа — ферропортин . [30] Он транспортирует двухвалентное железо из клетки, обычно при помощи церулоплазмина и/или гефестина (в основном в энтероцитах), которые окисляют железо до трехвалентного состояния, чтобы оно могло связывать ферритин во внеклеточной среде. [21] Гепсидин вызывает интернализацию ферропортина, уменьшая экспорт железа. Кроме того, гепсидин, по-видимому, подавляет как TFR1, так и DMT1 посредством неизвестного механизма. [31] Еще одним игроком, помогающим ферропортину в экспорте клеточного железа, является GAPDH. [32] Специфическая посттрансляционно модифицированная изоформа GAPDH рекрутируется на поверхность клеток, нагруженных железом, где она рекрутирует апо-трансферрин в непосредственной близости от ферропортина, чтобы быстро хелатировать экструдированное железо. [33]

Экспрессия гепсидина, который происходит только в определенных типах клеток, таких как гепатоциты , жестко контролируется на уровне транскрипции и представляет собой связь между клеточным и системным гомеостазом железа благодаря роли гепсидина как «привратника» высвобождения железа из энтероцитов в остальные клетки. тела. [21] Эритробласты вырабатывают эритроферрон , гормон, который ингибирует гепсидин и таким образом увеличивает доступность железа, необходимого для синтеза гемоглобина. [35]
Хотя некоторый контроль существует на уровне транскрипции, регуляция уровня клеточного железа в конечном итоге контролируется на уровне трансляции с помощью белков, связывающих железо-чувствительные элементы IRP1 и особенно IRP2. [36] Когда уровень железа низкий, эти белки способны связываться с железо-чувствительными элементами (IRE). IRE представляют собой структуры «стебель-петля» в нетранслируемых областях (UTR) мРНК. [21]
И ферритин, и ферропортин содержат IRE в своих 5'-UTR, так что при дефиците железа их трансляция подавляется с помощью IRP2, предотвращая ненужный синтез запасного белка и вредный экспорт железа. Напротив, TFR1 и некоторые варианты DMT1 содержат 3'-UTR IRE, которые связывают IRP2 при дефиците железа, стабилизируя мРНК, что гарантирует синтез импортеров железа. [21]

Функциональный или фактический дефицит железа может возникнуть по разным причинам. Эти причины можно сгруппировать в несколько категорий:
Организм способен существенно уменьшить количество железа, которое оно поглощает через слизистую оболочку. Похоже, что полностью остановить процесс транспортировки железа не удастся. Кроме того, в ситуациях, когда избыток железа повреждает саму оболочку кишечника (например, когда дети едят большое количество таблеток железа, произведенных для потребления взрослыми), еще больше железа может попасть в кровоток и вызвать потенциально смертельный синдром перегрузки железом. Большое количество свободного железа в кровообращении приведет к повреждению критически важных клеток печени, сердца и других метаболически активных органов.
Токсичность железа возникает, когда количество циркулирующего железа превышает количество трансферрина, доступного для его связывания, но организм может энергично регулировать усвоение железа. Таким образом, токсичность железа при приеме внутрь обычно является результатом чрезвычайных обстоятельств, таких как чрезмерное потребление таблеток железа [1] [42] , а не изменений в диете . Острая токсичность, вызванная приемом железа, вызывает, помимо других проблем, серьезное повреждение слизистой оболочки желудочно-кишечного тракта.
Избыток железа связан с более высокими показателями заболеваемости и смертности. Например, пациенты с раком молочной железы с низкой экспрессией ферропортина (что приводит к более высоким концентрациям внутриклеточного железа) в среднем выживают в течение более короткого периода времени, тогда как высокая экспрессия ферропортина предсказывает 90% 10-летнюю выживаемость у пациентов с раком молочной железы. [43] Аналогичным образом, генетические вариации генов-переносчиков железа, которые, как известно, повышают уровень железа в сыворотке, также сокращают продолжительность жизни и среднее количество лет, проведенных в добром здравии. [44] Было высказано предположение, что мутации, которые увеличивают абсорбцию железа, такие как те, которые ответственны за гемохроматоз (см. Ниже), были выбраны во времена неолита , поскольку они обеспечивали селективное преимущество против железодефицитной анемии. [45] Увеличение системного уровня железа становится патологическим в пожилом возрасте, что подтверждает представление о том, что антагонистическая плейотропия или «гиперфункция» приводит к старению человека. [44]
Хроническая токсичность железа обычно является результатом более хронических синдромов перегрузки железом, связанных с генетическими заболеваниями, повторными переливаниями крови или другими причинами. В таких случаях запасы железа у взрослого могут достигать 50 граммов (в 10 раз больше нормального общего количества железа в организме) и более. Наиболее распространенными заболеваниями, связанными с перегрузкой железом, являются наследственный гемохроматоз (HH), вызванный мутациями в гене HFE , и более тяжелое заболевание, ювенильный гемохроматоз (JH), вызванный мутациями либо гемоювелина ( HJV ) [46] , либо гепсидина ( HAMP ). . Точные механизмы большинства различных форм гемохроматоза взрослых, которые составляют большую часть генетических нарушений перегрузки железом, остаются невыясненными. Таким образом, хотя исследователи смогли идентифицировать генетические мутации, вызывающие несколько вариантов гемохроматоза у взрослых, теперь они должны обратить свое внимание на нормальное функционирование этих мутировавших генов.